编者按:2025年10月31日,由北京大学人民医院雄安医工交叉转化研究院主办,国家血液系统疾病临床医学研究中心-北京大学血液病研究所承办的“2025国际细胞治疗及生物医学前沿大会”在河北雄安盛大召开。会上,国家血液系统疾病临床医学研究中心、北京大学血液病研究所黄晓军教授作了题为《Decoding Homeostasis Remodeling in Haplo-SCT: From HLA Mismatch to Immune Rebalancing》(解码单倍体造血干细胞移植中的稳态重塑:从HLA错配到免疫再平衡)的精彩报告,系统阐述了单倍体移植后免疫稳态的重塑机制及其临床启示。本刊特整理课件核心内容,以飨读者。
 黄晓军教授现场作报告
黄晓军教授现场作报告
尽管移植物抗宿主病(GVHD)仍是异基因造血干细胞移植后最常见的并发症之一,但近50%的患者在移植后能够实现无病、无药物、无复发的长期生存。这表明这些患者在移植后实际上已达到免疫稳态。过去,人类白细胞抗原(HLA)不匹配一直被视为移植的主要障碍。然而,近年来单倍体移植技术的进展表明,其可达到与HLA匹配同胞供体移植相当的结果。因此,HLA不匹配已不再是影响移植结局的关键因素,表明这一障碍已被有效克服。
造血干细胞移植与实体器官移植存在一定区别,特别是在单倍体移植后,患者可以实现免疫稳态。所谓免疫稳态是指免疫系统通过各种调节机制,保持自身平衡状态,避免过度激活或功能低下,从而维持机体健康的一种生理状态。实现免疫稳态的关键是建立中枢和外周免疫耐受性。那么,HLA障碍如何被克服以重建免疫稳态?在单倍体移植中,如何恢复外周和中枢免疫耐受性?这些科学问题均有待于进一步回答。
跨越HLA屏障的免疫稳态重建机制
单倍体移植跨越HLA障碍的机制包括两个方面:一是抑制外周T细胞激活,并引导其外周重建,建立外周免疫稳态;二是促进胸腺功能恢复,推动T细胞中枢重建,进而建立中枢免疫耐受。
在这一过程中,T细胞激活的调控是关键环节。若其未能得到效控制,则易诱发GVHD。为减少T细胞激活,目前采用了多种策略,如阻断共刺激信号或细胞因子通路等,以诱导T细胞失活,从而减少GVHD发生并促进外周免疫稳态的建立。
例如,黄晓军教授团队研究发现粒细胞集落刺激因子(G-CSF)可以重塑T细胞三维基因组结构,从而诱导T细胞低反应性。此外,其还可上调SOCS1,抑制JAK-STAT通路,从而促进外周T细胞耐受性。类似地,抗胸腺细胞球蛋白(ATG)可通过去除B细胞和T细胞,并诱导T调节细胞(T-reg)的扩增。移植后环磷酰胺(PT-Cy)也可通过扩增T调节细胞来诱导外周免疫耐受性。
中枢免疫稳态的建立与重塑
尽管临床观察到部分移植患者可以重塑免疫稳态,但稳态形成的机制并不清楚。例如,异基因造血干细胞移植后实现免疫稳态的患者,其细胞与分子特征如何?单倍体移植与HLA匹配同胞移植在免疫稳态重塑过程中是否表现出相似的模式?
为此,黄晓军教授团队开展了相关研究,选取了临床上已达免疫稳态的患者,即移植后超过1年无GVHD、无感染、无复发,且停用免疫抑制治疗的长期缓解者。通过单细胞转录组分析,对其免疫细胞亚群进行了系统比较。结果显示,供者来源所有免疫亚群在患者体内均完全重建,但占比分布不同。同时,单倍型与同胞全合移植有着不同的免疫稳态重塑模式。
1、特有型克隆与T细胞重建
具体而言,在单倍体移植后,受者的T细胞受体(TCR)谱系与供者之间存在显著差异;而在HLA匹配同胞移植中,受者的TCR构成与供者高度一致。将供受者间相同的TCR克隆定义为共享的共有型克隆,而仅存在于受者中的TCR克隆定义为特有型克隆。研究发现,与HLA匹配同胞供体移植相比,单倍体移植后特有型克隆的比例较高,而且这些特有型克隆高表达转录因子ZNF683以及胸腺选择信号通路相关基因,提示单倍体移植后T细胞更多通过中枢重建。
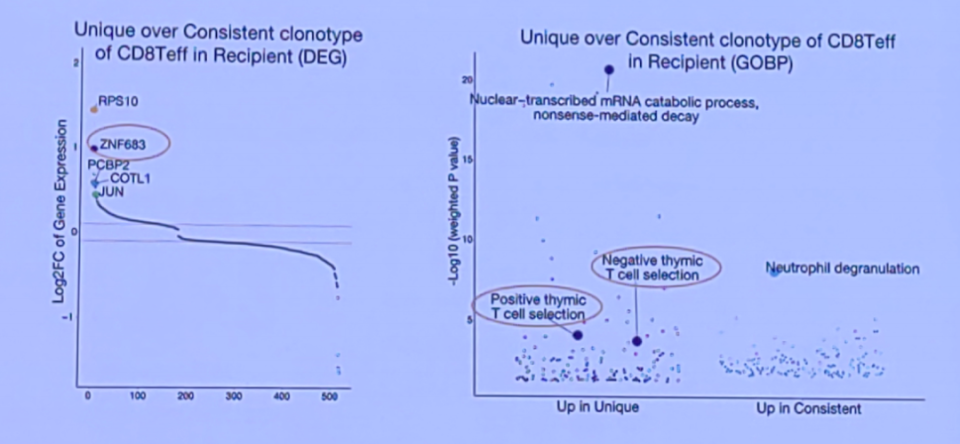 ZNF683以及胸腺选择信号通路相关基因在特有型克隆中呈高表达
ZNF683以及胸腺选择信号通路相关基因在特有型克隆中呈高表达
进一步分析显示,ZNF683主要于单倍体移植患者CD8 T细胞中特异性激活。ZNF683在效应CD8 T细胞中也呈高表达。结合临床观察与动物模型研究发现,抑制外周T细胞激活可促进中枢T细胞重建,而这对于维持免疫稳态尤为关键,尤其是在单倍体移植背景下。
此外,在达到免疫稳态的患者中,团队还观察到一种新型CD8调节性前体细胞的显著扩增。最新数据表明,该细胞亚群具备免疫调节功能,可有效抑制移植物抗宿主反应性T细胞,从而有助于外周免疫稳态的维持。综上,单倍体移植后存在独特的免疫重塑模式。
2、胸腺功能与免疫稳态
黄晓军教授团队的最新研究表明,HLA不匹配可独立损伤胸腺功能并影响T细胞恢复,这也是单倍体移植较为困难的主要原因。现有的治疗策略,无论是基于ATG还是PT-Cy的方案,在临床上均取得了良好疗效,因此其机制中一定包含对胸腺功能的修复,因为胸腺介导的中枢免疫稳态是单倍体移植后免疫重塑的核心。
在讨论中枢免疫稳态时,我们需要从胸腺发育及T细胞免疫耐受形成的机制中汲取经验。中枢免疫稳态的建立依赖多种细胞类型在胸腺中的协同作用,通过胸腺负选择等过程共同维持T细胞耐受性。单倍体移植为研究移植后T细胞的胸腺再教育提供了理想的平台。供者与受者来源的抗原呈递细胞(APC)如何分别呈递自身主要组织相容性复合体(MHC)分子,并协同调控阴性选择过程?临床干预如何修复胸腺功能,进而影响中枢免疫稳态的形成?这些问题的解决对于揭示单倍体移植后的免疫稳态机制具有重要意义。
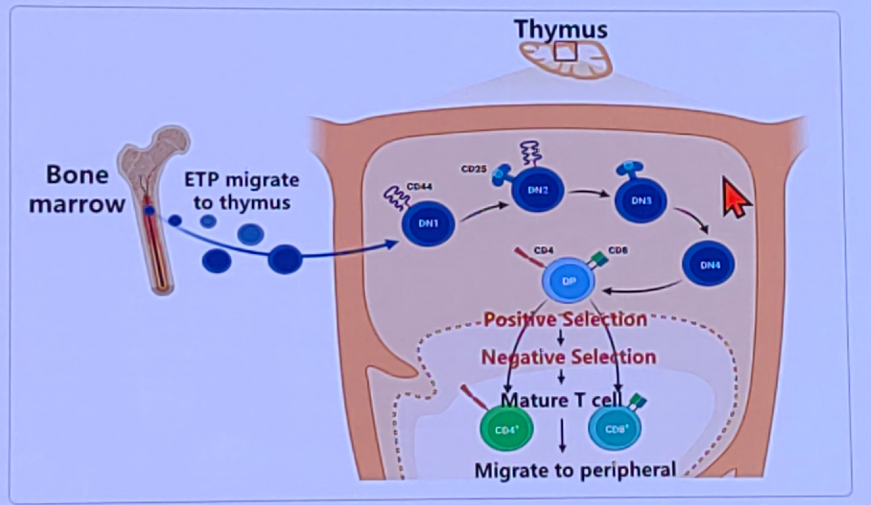 T细胞通过胸腺发育建立中枢耐受
T细胞通过胸腺发育建立中枢耐受
3、G-CSF在胸腺恢复中的作用
在黄晓军教授主导的“北京方案”中,G-CSF在促进单倍体移植成功中起着至关重要的作用。其团队未发布的数据表明,G-CSF能够改善胸腺微环境,促进中枢耐受性的建立。结合既往发表研究显示,G-CSF和ATG能够修复胸腺损伤并促进中枢T细胞通路重建。然而,高剂量的PT-Cy可诱导胸腺损伤,阻碍中枢T细胞通路重建。
 G-CSF、ATG 与PTCy方案对胸腺的影响
G-CSF、ATG 与PTCy方案对胸腺的影响
总之,通过抑制外周T细胞激活并调节其外周重建,可有效建立外周免疫稳态;同时,恢复胸腺功能并促进T细胞中枢重建,有助于进一步建立中枢免疫耐受。
总结
不同移植模型在免疫稳态重塑中呈现出显著差异。临床干预能够修复胸腺功能,并促进中枢耐受的形成,而对调节机制的深入理解对于揭示胸腺介导的免疫稳态形成过程至关重要。单倍体移植不仅是一种重要的临床治疗方案,也为研究免疫稳态重塑提供了理想模型。对免疫稳态重塑机制的深入研究,有助于指导实体器官移植后的免疫耐受策略,从而更好地促进免疫稳态的形成和维持。
专家简介

黄晓军 教授
国家血液系统疾病临床医学研究中心、北京大学血液病研究所
中国工程院院士,主任医师,博士生导师
国家血液系统疾病临床医学研究中心主任
北京大学血液病研究所所长
北京大学人民医院血液科主任
北京大学人民医院医工交叉转化研究院院长
荣获何梁何利科学技术与进步奖、光华工程科技奖、树兰医学奖、国际血液与骨髓移植研究中心与美国移植及细胞治疗学会共同颁发的杰出服务奖、国际临床血液学会颁发的国际合作贡献奖等。