前言:2026年欧洲血液与骨髓移植协会(EBMT)年会将于3月22日-25日在西班牙马德里隆重举行,现已公布摘要内容。在急性白血病领域,治疗策略正朝着更精准、更高效的方向飞速演进。本届年会的急性白血病(I)专场(OS03)将带来8项重磅口头报告,内容涵盖新型CAR-T疗法的探索、移植前后靶向治疗的优化、表观遗传药物的免疫代谢新机制,以及供者选择策略的深度比较。这些研究从不同维度揭示了改善急性白血病,尤其是难治复发患者结局的最新方向。以下为会议核心内容的抢先速递。
本届EBMT年会急性白血病(I)专场展现了细胞治疗与移植领域的多项重要进展:在CAR-T治疗方面,Rapcabtagene autoleucel和Obe-cel为R/R B-ALL提供了新的治疗选择,缓解深度决定长期预后;在Ph+ ALL优化方面,二三代TKI诱导联合移植后维持治疗显著改善生存,且独立于MRD状态;在移植机制研究方面,地西他滨通过H3K4me3-ACOD1-衣康酸轴免疫代谢重编程预防AML复发,揭示了表观遗传-免疫代谢交叉调控新机制;在供者选择策略方面,单倍型移植十年实践持续优化,年轻单倍型供者可替代年长同胞供者,UM171扩增技术突破脐血细胞剂量限制,而CIBMTR大数据证实MSD/MUD仍是首选。这些研究成果将进一步推动急性白血病个体化治疗的发展,为更多患者带来治愈机会,以下为各项研究精要。
PART.1
新型CAR-T治疗R/R B-ALL:Rapcabtagene autoleucel的I期评估
意大利贝尔加莫大学的Alessandro Rambaldi带来了“评估rapcabtagene autoleucel (YTB323)在成人复发/难治B细胞急性淋巴细胞白血病患者中安全性与疗效的1期研究”(OS03-01)。该1期多中心研究评估了基于T-Charge平台快速制备的新一代CD19 CAR-T疗法rapcabtagene autoleucel在成人R/R B-ALL患者中的表现。在35例接受治疗的患者中(中位年龄41岁,66%有移植史),研究探索了四个剂量水平。数据显示,该疗法在DL2(5×10⁶ CAR+细胞)及以上剂量时显示出较高的细胞扩增和持久的疗效。最佳总缓解率在DL3剂量(7.5×10⁶)达到92%(CR率50%),且中位缓解持续时间尚未达到(中位随访22个月)。安全性方面,剂量限制性毒性主要发生在较低剂量组,DL3及DL4组安全性更可控。研究表明,rapcabtagene autoleucel,特别是在DL3剂量下,在重度经治的成人R/R B-ALL患者中展现出令人鼓舞的疗效与可管理的安全性,其快速制造工艺为急需治疗的患者提供了潜在优势。
PART.2
Ph+ ALL移植优化:二三代TKI联合移植后维持治疗
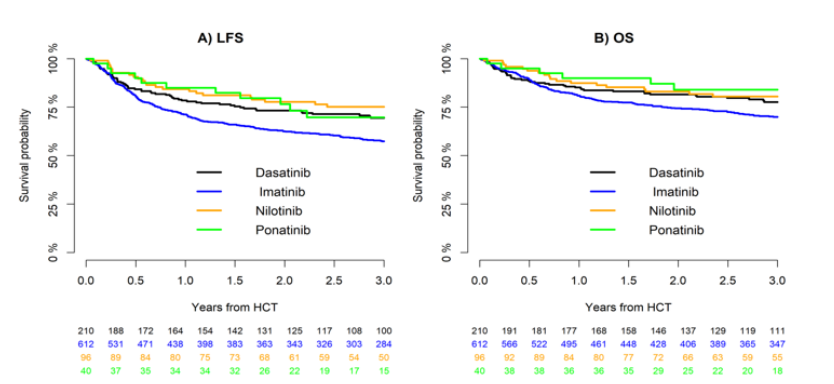
EBMT急性白血病工作组的Iman Abou Dalle报告了“移植前使用二/三代TKI联合移植后预防性维持优化费城染色体阳性急性淋巴细胞白血病移植结局”(OS03-02)。这项EBMT大型回顾性研究旨在明确不同代TKI在Ph+ ALL患者异基因移植前后的应用对长期结局的影响。研究纳入958例在首次缓解期接受移植的患者。结果显示,与使用伊马替尼相比,移植前诱导治疗采用达沙替尼、尼洛替尼或泊那替尼等二代/三代TKI,能显著改善无白血病生存。更重要的是,移植后采用TKI预防性维持治疗,可显著提升无白血病生存和总生存,且这一获益与移植前的微小残留病状态无关。多变量分析确认,移植后TKI预防是生存获益的独立有利因素。该研究强有力地支持,在Ph+ ALL的移植管理中,应优先选用更强效的二代/三代TKI进行诱导,并常规采用移植后TKI预防策略以优化长期结局。
PART.3
Obe-cel治疗R/R B-ALL:FELIX研究长期随访
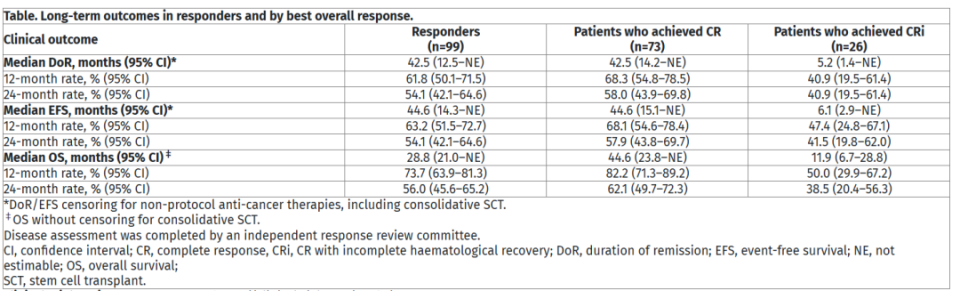
美国德克萨斯大学MD安德森癌症中心的Elias Jabbour展示了“FELIX研究中接受obe-cel治疗后获得缓解的成人R/R B-ALL患者的临床结局”(OS03-03)。该分析聚焦于CAR-T疗法obecabtagene autoleucel(obe-cel)在关键FELIX研究中获得缓解的患者的长期结局。在127例输注患者中,78%获得缓解,其中74例达到完全缓解,26例为血细胞计数不完全恢复的完全缓解。中位随访近33个月,缓解患者的中位缓解持续时间达44.6个月,中位总生存期为28.8个月。获得CR的患者预后显著优于CRi患者,其中位总生存期是后者的近4倍。尽管部分患者接受了巩固性干细胞移植,但相当大比例的患者(38.4%)在未接受其他抗癌治疗的情况下持续缓解。这表明obe-cel能为应答者带来持久的生存获益,而达到深度完全缓解是长期预后的关键。
PART.4
地西他滨预防移植后复发:免疫代谢重编程新机制
陆军军医大学第二附属医院(新桥医院)高蕾教授团队的Yutong Xie汇报了“地西他滨通过H3K4me3-ACOD1-衣康酸轴对巨噬细胞进行免疫代谢重编程以预防急性髓系白血病移植后复发”(OS03-04)。这项研究深入揭示了地西他滨维持治疗降低AML移植后复发风险的新机制。通过前瞻与回顾队列的多组学分析,研究者发现,地西他滨能通过降低组蛋白修饰H3K4me3在ACOD1基因启动子区的富集,抑制其表达,从而减少代谢物衣康酸的生成。这一过程重塑了骨髓巨噬细胞的代谢状态,使其从促肿瘤的M2型向抗肿瘤的M1型复极化。在AML小鼠模型中,地西他滨治疗显著提高了M1/M2巨噬细胞比例,降低了肿瘤负荷并延长了生存期。该研究首次从免疫代谢角度阐明了地西他滨的免疫调节作用,将表观遗传调控、免疫细胞代谢与肿瘤微环境重塑相联系,为ACOD1成为预防移植后复发的新靶点提供了理论依据。
PART.5
AML单倍型移植十年变迁:实践与结局演变
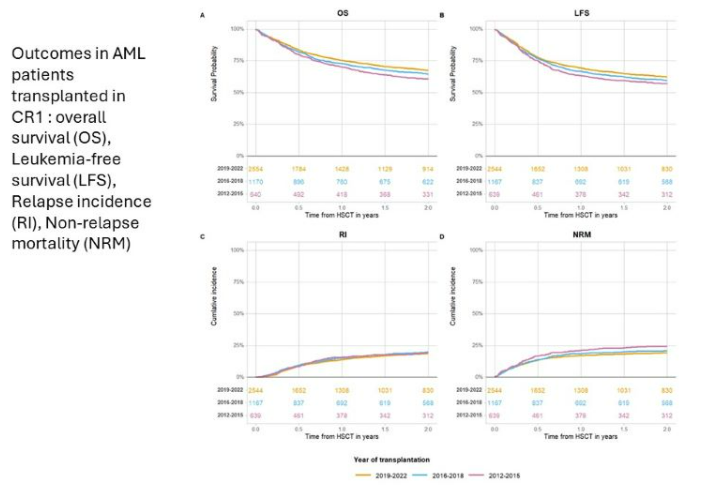
EBMT急性白血病工作组的Eolia Brissot分析了“急性髓系白血病单倍体移植的十年变迁:实践模式与结局”(OS03-05)。这项涵盖2012-2022年6818例患者的大型研究,清晰描绘了十年来AML单倍体移植的演变趋势:临床实践发生了显著变化——患者年龄更大、更多使用减低强度预处理、更多患者在首次缓解期移植、外周血干细胞成为绝对主导的移植物来源,并且以移植后环磷酰胺为基础的GVHD预防方案使用率大幅增加。
这些临床实践的优化直接转化为了结局的改善:在首次缓解期移植的患者中,2019-2022年间的2年总生存率、无白血病生存率较2012-2015年显著提升,非复发死亡率显著下降。多变量分析证实,移植时期越近,生存结局越好。研究表明,单倍体移植已成为AML的成熟治疗选择,其持续优化的实践模式不断改善着患者预后,但复发仍是未来需要攻克的主要挑战。
PART.6
继发性AML供者选择:年轻单倍型供者 vs 年长同胞供者
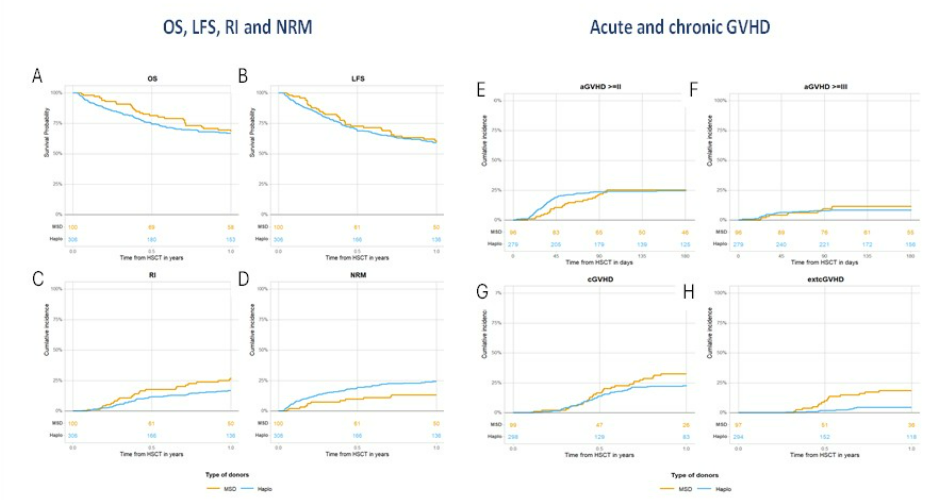
以色列拉马特甘的Arnon Nagler比较了“使用移植后环磷酰胺时,治疗继发性急性髓系白血病:年长同胞供者 vs. 年轻单倍体供者”(OS03-06)。对于接受移植后环磷酰胺预防的继发性AML患者,选择年轻单倍体供者还是年长同胞供者一直存在争议。这项EBMT研究对406例患者进行了比较,结果显示,两组在2年总生存、无白血病生存、复发率及无GVHD无复发生存方面均无显著差异。然而,具体并发症谱存在差异:年轻单倍体供者组有更高的非复发死亡率和稍慢的中性粒细胞植入,但广泛型慢性GVHD发生率显著更低;而年长同胞供者组广泛型慢性GVHD更高。这表明,在PTCy平台下,两种供者来源为继发性AML患者提供了总体可比的生存结局,但毒性谱不同,临床选择需权衡非复发死亡率与慢性GVHD风险,进行个体化决策。
PART.7
UM171扩增脐血移植:高危白血病安全有效新选择
加拿大蒙特利尔的Sandra Cohen介绍了“UM171扩增脐血作为高危白血病和骨髓增生异常综合征安全且强效的移植物来源,带来持久长期生存”(OS03-07)。研究评估了UM171体外扩增脐血移植治疗高/极高危白血病或MDS的疗效。60例患者中,57%符合极高危标准,30%为移植后复发。研究者选择了HLA 5/8相合、甚至细胞剂量原本不足的脐血单位进行扩增。结果显示,中性粒细胞植入中位时间仅17天,植入率高达92%。尤其令人瞩目的是,在长期随访中,患者2年总生存率达63.7%,无进展生存率达57.0%,且年轻患者(<43岁)的非复发死亡率为0%。这对于伴有TP53突变、非缓解状态等传统上预后极差的群体而言,是前所未有的突破。研究表明,UM171扩增技术能克服传统脐血移植的瓶颈,为缺乏合适供者的高危患者提供了一种具有强大抗白血病活性且GVHD风险可控的卓越选择。
PART.8
当代GVHD预防时代供者类型2年结局:CIBMTR分析
美国CIBMTR的Steven M. Devine分析了“在当代GVHD预防背景下,不同供者类型的2年患者结局是否有差异?”(OS03-08)。这项基于CIBMTR数据库、涵盖超过1.3万例患者的大型回顾性研究,系统比较了在当代GVHD预防策略下,不同供者类型移植治疗急性白血病/MDS的2年结局。在移植后环磷酰胺广泛应用的时代,全相合同胞供者和8/8全相合无关供者仍展现出最佳且相似的总生存和无GVHD无复发生存。7/8不相合无关供者和单倍体供者的结局与之可比,且显示出更低的复发率,但被略高的非复发死亡率所部分抵消。传统脐血移植的总体结局相对较差。该研究为临床供者选择提供了清晰的等级参考:优先选择全相合同胞或无关供者,其次考虑7/8不相合无关供者或单倍体供者,最后是脐血。这一定位对移植决策具有重要指导价值。
总 结
本届EBMT急性白血病(I)专场的8项研究,从微观机制到宏观策略,全方位展现了该领域的前沿动态。核心进展可归纳为三个层面:首先,治疗武器持续革新,无论是基于新平台快速制备的CAR-T疗法,还是UM171扩增脐血这类新型移植物,都为难治患者带来了新的治愈希望。其次,治疗方案深度优化,研究明确了Ph+ ALL中更强效TKI序贯移植后预防的价值,并厘清了不同供者类型在当代平台下的优先次序,使临床决策有据可依。最后,基础与临床紧密结合,对地西他滨作用机制的深度剖析,揭示了免疫代谢调控在预防复发中的关键作用,为开发新靶点奠定了基础。总体而言,这些研究共同推动急性白血病治疗步入一个更精准、更多元、疗效也更可期的新阶段。