尽管酪氨酸激酶抑制剂(TKIs)治疗极大改善了慢性髓系白血病(CML)患者的预后,但CML治疗仍面临一些挑战,比如耐药问题、如何实现无治疗缓解(TFR)以及基因突变对TKIs疗效的影响等。在刚刚结束的第65届美国血液学会(ASH)年会上,多项研究针对这些问题进行了深入探讨,为优化完善CML治疗带来参考。本期《肿瘤瞭望-血液时讯》特别邀请到北京协和医院段明辉教授,精选会议上CML方面的重磅研究,进行精彩解读。
01
【摘要号:870】达沙替尼联合和不联合维奈克拉(Venetoclax)治疗早期慢性期慢性髓系白血病(ECP-CML)的Ⅱ期研究
背景
ECP-CML患者的治疗目标是酪氨酸激酶抑制剂(TKIs)治疗达持续深度分子学缓解(DMR),最终实现无治疗缓解(TFR)。然而,仅有少部分患者可维持BCR::ABL1IS 4.0-4.5 log下降(MR4.5)3年以上。临床前研究显示,BCL-2是CML干细胞/祖细胞的关键存活因子。因此,TKIs和维奈克拉(Venetoclax)联合同时靶向BCR::ABL1和BCL-2,或有望显著改善DMR和随后的TFR率。本研究的目的是评估TKIs联合维奈克拉用药的安全性和有效性。
方法
主要入选标准:(1)ECP-CML或加速期CML(仅发生克隆演变);(2)既往TKI治疗< 1个月。入组患者前3个月接受达沙替尼(Dasatinib)50 mg/d单药治疗,从第4个月起,接受达沙替尼50 mg/d治疗的同时,每个月的第1~14天接受维奈克拉治疗,持续3年。前16例患者接受维奈克拉的剂量为200 mg/d,采用每日快速梯度递增,即第1天50 mg,第2天100 mg,第3天及以后200 mg。由于维奈克拉200 mg/d连续给药观察到中性粒细胞减少症,因此从17例患者开始,方案修订为每个月第1~14天维奈克拉200 mg/d治疗,直至达到MR4.5后,维奈克拉减量至100 mg/d,每个月第1~7天给药。完成3年联合治疗后,患者继续接受达沙替尼单药治疗,DMR持续3年以上可尝试停药。
研究的主要终点是联合治疗12个月的主要分子学缓解(MMR)率,次要终点包括12个月的MR4.5率和累计总MR4.5率;联合治疗6个月、12个月、18个月、24个月和36个月的MR4.5率;持续MR4.5≥3年的患者比例;TFR率;总生存期;以及联合治疗的安全性。治疗失败作为累计反应率的一个竞争性事件。无失败生存(FFS)指从开始治疗到主要细胞遗传学缓解(MCyR)丧失、进展为加速期或急变期,以及除TFR或死亡以外的任何原因终止治疗。
结果
在2018年4月至2021年8月期间,共入组65例患者接受治疗。开始治疗时的中位年龄为46(范围23~73)岁,57%的患者为女性。21例(32%)患者患有脾肿大,46例(71%)患者Sokal积分低危,3例(5%)患者Sokal积分高危(如表1)。联合用药12个月后,85%的患者达到MMR及以上缓解。从开始TKI治疗到MMR、MR4和MR4.5的中位时间分别为6.2个月、13个月和23.9个月。中位随访25.7(范围8.7~48.1)个月后,2例患者因不良事件(胃肠道不耐受和胸腔积液)终止治疗;2年的FFS率为96%。1例患者由于18个月内未达到完全细胞遗传学缓解(CCyR)而更换其他TKI治疗;未观察到CCyR丧失、进展为加速期或急变期以及死亡事件。然后,我们将联合用药的结果与单药达沙替尼治疗的85例患者结果进行比较。自启动TKI治疗,达沙替尼单药组和达沙替尼联合维奈克拉治疗组的12个月累计MMR率分别为78%和79%。24个月累计CCyR、MMR、MR4和MR4.5率汇总于表2。达沙替尼单药组,3例患者分别由于12个月未达到MCyR、18个月未达到CCyR和发生ABL1突变而更换其他TKI治疗;3例患者因丧失CCyR而更换TKI治疗;2例患者在治疗期间死亡(死亡与CML无关)。治疗1年内,达沙替尼单药组和达沙替尼联合维奈克拉组1/2级中性粒细胞减少(绝对中性粒细胞计数在1.0×109/L至正常值下限)的发生率分别为21%和52%(P<0.001);3/4级中性粒细胞减少(绝对中性粒细胞计数低于1.0×109/L)的发生率分别为8%和17%(P<0.001)。达沙替尼联合维奈克拉组未发生中性粒细胞减少性发热。
结论
达沙替尼50 mg/d联合维奈克拉治疗ECP-CML患者安全有效。中位随访2年,达沙替尼联合维奈克拉的累计缓解率与达沙替尼单药相似,未增加明显的毒性。需要进一步的随访来评估TFR。
02
【摘要号:866】在ASC4MORE研究的长期随访中,Asciminib(ASC)联合伊马替尼(IMA)表现出持续高治疗率和深度分子学缓解(DMRs)
背景
随着酪氨酸激酶抑制剂(TKIs)治疗可使慢性髓系白血病慢性期(CML-CP)应答患者的预期寿命接近普通人群,人们开始越来越重视生活质量和达到无治疗缓解(TFR)的可能。然而,这需要在早线治疗中探索能够使更多患者安全实现持久DMRs的Tx策略,作为TFR的准入标准。ASC是唯一被批准的靶向ABL肉豆蔻酰口袋(STAMP)的BCR::ABL1抑制剂。ASC联合ATP竞争性TKIs的临床前研究提示,联合治疗可能会增强BCR::ABL1抑制。在ASC4MORE (NCT03578367)研究的初步(第48周)分析中,ASC联合伊马替尼(IMA)可导致快速和深度的反应,与单独ASC治疗观察到的结果相比,安全性方面没有新的或恶化的发现。本研究报告了ASC联合IMA或持续IMA治疗或更换尼洛替尼(NIL)治疗的结果,以及在96周的Tx治疗后从持续IMA治疗更换为用ASC联合治疗的患者结果,这些患者使用IMA作为首个TKI治疗,且IMA治疗≥1年未达到DMR(截止日期:2023年3月6日)。
方法
在这项定性试验中,符合条件的CML-CP成人患者以1:1:1:1的比例随机分组,分别接受ASC(40 mg或60 mg每日一次[QD])联合IMA 400 mg QD,或继续IMA 400 mg QD,或更换用NIL 300 mg每日两次治疗。根据欧洲白血病网(ELN)2013标准,患者必须仅接受IMA 400 mg QD治疗≥1年,作为他们的首个TKI治疗,且在随机分组时BCR::ABL1IS >0.01%至≤1%,任何时点均未达到DMR,也没有Tx失败。将第48周和第96周的分子学反应(MR) 4.5 (MR4.5, BCR::ABL1IS≤0.0032%)分别作为研究的主要终点和次要终点。IMA治疗第48周时未达到MR4.5的患者可加用ASC 60 mg QD。ASC单药治疗vs. ASC联合IMA的安全性和有效性将在未来的分析中进行评估。
结果
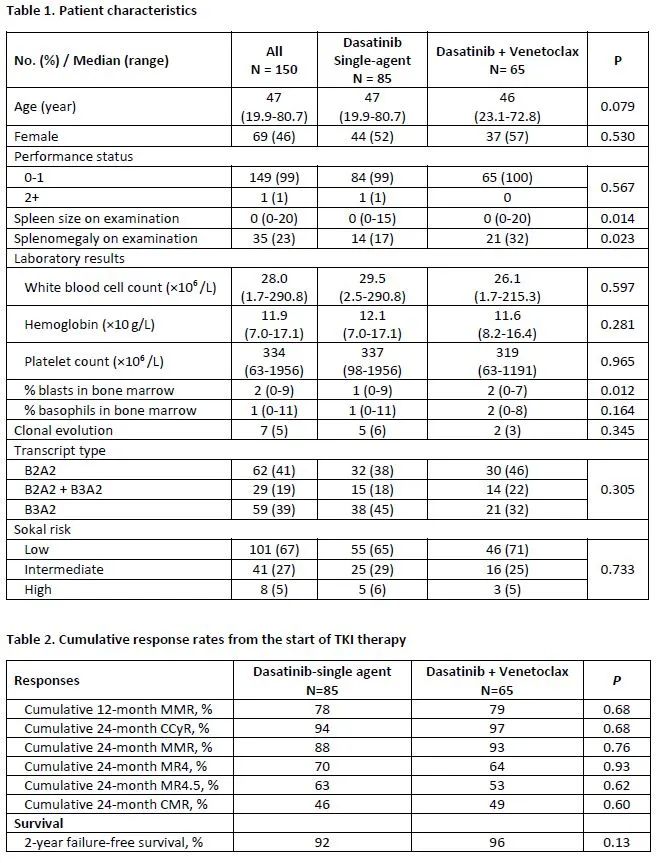
患者(N=84)被随机(每个Tx组N=21)分配,分别接受ASC 40 mg、ASC 60 mg、IMA和NIL治疗,中位暴露时间(范围)分别为141.7(27~203)、124.3(1~192)、53.4(50~186)和110.1(1~189)周,完成随机Tx治疗的患者比例分别为85.7%、76.2%、19.0%和52.4%。停药的主要原因是患者决定停药(ASC 40 mg联合治疗组为9.5%)、不良事件(ASC 60 mg联合治疗组和NIL治疗组AEs发生率分别为14.3%和33.3%),以及医生的决定(IMA治疗组为66.7%,所有这些患者更换用ASC 60 mg联合治疗)。在第96周,40 mg ASC联合治疗组、60 mg ASC联合治疗组、IMA组和NIL组分别有19.0%、19.0%、4.8%和9.5%的患者达到MR4.5,分别有38.1%、23.8%、9.5%和28.6%的患者达到MR4 (BCR::ABL1IS≤0.01%)(如图)。第96周达到MR4.5的累计发生率分别为28.6%、28.6%、9.5%和19.0%。在第24、48和96周,从IMA治疗更换为ASC 60 mg联合治疗的患者分别有14.3%、21.4%和14.3%达到MR4.5。随着随访时间的延长,ASC联合IMA治疗的安全性没有新的或恶化的发现(如表)。尽管ASC联合治疗的中位持续时间较长,但与更换用NIL(33.3%)治疗相比,较少的患者出现可导致ASC 40 mg(4.8%)和60 mg(14.3%)联合治疗停药的不良反应。与初步分析相比,ASC联合治疗的停药率并没有因随访时间的延长而增加。NIL组发生1例动脉闭塞事件(AOE);ASC联合治疗组未发生AOE。与ASC 40 mg(14.3%)和60 mg(19.0%)治疗组相比,NIL(23.8%)治疗组严重不良反应的发生率较高。自初步分析以来,未发生新的死亡病例。
结论
在IMA治疗≥1年后未达到DMR的患者中,96周时ASC联合IMA治疗达到MR4.5的患者比例高于继续IMA治疗或更换用NIL治疗。从IMA治疗更换用ASC 60 mg联合治疗的患者仍然能够达到DMRs。ASC联合IMA治疗耐受性良好,与ASC单药相比,没有新的或恶化的安全性发现。尤其值得关注的是,在研究>2年后,完成ASC联合的随机Tx治疗患者比例高达75%以上,与完成NIL治疗的患者比例(52.4%)形成对比。这些患者有望达到高DMRs率,值得进一步研究。该研究关于ASC单药治疗的未来分析,将评估ASC单独治疗是否可以提供与ASC联合IMA治疗相似的反应。
摘要号870和866研究点评
随着TKIs治疗可使CML-CP患者的预期寿命接近普通人群,人们越来越重视生活质量和达到无治疗缓解(TFR)的可能。深度分子学缓解(DMR)是实现TFR的先决条件,因此,探索能够使更多患者安全实现持久DMR的治疗策略,成为提高TFR率的重要措施。为了达成高DMR率,可以考虑多种措施,例如加强早期治疗的依从性管理、及时监测疗效、联合干扰素治疗等。此外,将高强度TKI作为一线治疗也是重要措施,在2023年度ASH会议中已有研究尝试将三代TKI药物ponatinib作为一线治疗。为加强一线治疗的强度,除将高强度TKIs用于一线治疗外,还可考虑以TKI单药为基础的联合治疗,以获得更好的DMR率。
本次ASH会议中,研究者们对达沙替尼联合维奈克拉(摘要号:870)和伊马替尼联合Asciminib(摘要号:866)两种联合方式都进行了有益的尝试。在摘要号为870的研究中,达沙替尼联合维奈克拉是一线用药,而在摘要号为866的研究中,Asciminib则作为伊马替尼治疗1年无法达成DMR时增加的联合用药。两个研究都是对照性研究,因此结果具有较高的参考价值。联合用药通常需要先保障安全性,因此,在摘要号为870的研究中对药物剂量强度进行了调整,达沙替尼的剂量降至50 mg/日,维奈克拉则在达沙替尼治疗第4个月才开始联合用药。遗憾的是,在目前随访25.7个月,MMR和DMR等多个研究终点与对照组相比未见到显著差异。尽管维奈克拉联合达沙替尼组3/4级中性粒细胞减少症发生率比对照组显著增高,但是并未显著增加粒缺伴发热的情况,由此可见,联合治疗安全性是有保证的,只是尚未表现出DMR的优势。对于联合治疗目前未能提高DMR的现状,需要考虑的因素有很多,例如维奈克拉的剂量是否还有上调空间;维奈克拉联合治疗时间是否太晚;联合治疗的随访时间是否足够长。
在摘要号为866的研究中,伊马替尼≥1年,BCR::ABL1IS>0.01%且≤1%者随机分4组,分别用Asciminib两个剂量组联合、伊马替尼不变和更换尼洛替尼治疗,4组患者第96周达到MR4.5的累计发生率分别为28.6%、28.6%、9.5%和19.0%。4组完成随机治疗患者的比例分别为85.7%、76.2%、19.0%和52.4%,主要停药原因在联合Asciminib组为患者决定和不良事件,伊马替尼组为医生决定,尼洛替尼组为不良事件。由此可见,伊马替尼治疗≥1年未达DMR的患者,联合Asciminib治疗比继续伊马替尼或转换为尼洛替尼治疗获得更高的DMR率,而且,联合治疗组的安全性良好,75%以上的患者可以完成预计治疗,从而有可能最终增加可进入TFR尝试的患者数量。
上述两个研究的着眼点都是联合用药,希望通过不同机制药物的联合获得更高的DMR率,从而争取更多的TFR机会。虽然研究规模和随访时间有限,但是已经取得一些初步成果。首先,TKI联合STAMP抑制剂的治疗可能优于单药的分子学疗效,而TKI联合维奈克拉目前尚未显示出显著效果。其次,尽管两种联合治疗的安全性数据都较好,但是TKI联合STAMP抑制剂的安全性更加令人鼓舞。因此,进一步改良联合治疗方案,包括将联合用药的时间点提前、将伊马替尼改为疗效和安全性更好的氟马替尼等,均有望进一步提高联合治疗的DMR率,从而增加TFR成功率。
目前,国际上针对TKI治疗后获得持续稳定DMR的CML-CP患者是否可以尝试TFR的意见已基本达成一致,从而将如何提高TFR率作为研究的主要方向。而国内目前依然对TFR能否实施存在较多顾虑和争议,其中最大的顾虑是停药后的复发。实际上,虽然符合TFR实施标准的患者停药后复发率高达50%左右,但是这些患者在重启TKIs治疗几乎均可以恢复到TFR实施前的分子学缓解状态,由于停药尝试导致疾病进展者极为罕见。由此可见,TFR实施的安全性非常高,国内的研究重点也应尽快从争议TFR是否可行转向如何提高TFR率,以期与国际主流研究方向保持一致。
03
【摘要号:449】ASCEMBL试验中使用≥2种酪氨酸激酶抑制剂(TKIs)后血液肿瘤相关基因突变对慢性髓系白血病慢性期(CML-CP)患者临床结局的影响
简介
在慢性髓系白血病加速期(CML-AP)经常检测到血液肿瘤相关基因的体细胞突变。最常见的突变基因是RUNX1、ASXL1、IKZF1(亚显微缺失)和BCR::ABL1(激酶结构域突变)。ASXL1是CML诊断中最常检测到的突变(≈9%)。然而,由于基因组研究主要集中在诊断或进展阶段的患者,因此在先前接受≥2种TKIs治疗的CML-CP患者中血液肿瘤相关基因突变的发生率和影响尚未被描述。ASCEMBL Ⅲ期研究在大于2年的随访中,Asciminib (ASC)在既往接受≥2种TKIs治疗CML-CP患者中继续表现出优于博舒替尼(Bosutinib,BOS)的疗效,对该人群中癌症基因体细胞突变的分析有可能揭示患者对研究治疗的反应或在后线治疗中的疾病特征。在这里,我们对ASCEMBL研究患者人群中的变异进行了描述性分析,包括突变频率、共突变发生情况以及突变与临床结局的关联,特别是主要分子学缓解(MMR)和治疗失败(TF,定义为由于缺乏疗效或不耐受而停药)。
方法
纳入的CML-CP成人患者既往接受≥2种TKIs治疗,且最后一次TKI治疗不耐受或根据2013年欧洲白血病网(ELN)建议为缺乏疗效,无BCR::ABL1基因T315I或V299L突变。这些患者以2:1的比例随机分至ASC 40 mg每日2次治疗组或BOS 500 mg每日1次治疗组。在基线(BL)和治疗结束(EOT,定义为因任何原因终止治疗或研究完成)时采集血液,分离DNA。涵盖89个血液肿瘤常见突变基因的下一代基因检测panel,包括ABL1和IKZF1缺失,用于检测符合致病性标准的体细胞突变。仅检测BCR::ABL1IS≥2%的样本,该水平已被证明可以检测白血病细胞的突变。采用多变量Cox比例风险回归模型进行分析,调整年龄、性别、治疗和先前TKI停药的原因(不耐受vs. 缺乏疗效),以确定基线时突变的预后判断价值。
结果
共有233例患者被随机分至ASC组(n=157)或BOS组(n=76)。162例患者(ASC, n=110;BOS, n=52)有基线时的测序数据;102例有≥1个突变,其中ASC组有69例(63%),BOS组有33例(63%)。总体而言,在基线时23个基因中检测到159个突变,每例患者有0~5个突变。中位变异等位基因频率(VAF)为19.6%(范围为0.9%~58%)。ASXL1(31%的患者)和ABL1激酶结构域(17%的患者)突变最常见。在基线时,27例患者有≥1个ABL1突变,85%的患者有≥1个其他癌症基因突变。在基线时,162例患者中有12例(7.4%)同时出现ASXL1和ABL1突变,高于预期的基于该数据集中这些基因的个体频率2.9%。在基线时RUNX1和IKZF1突变在CML-CP中罕见。
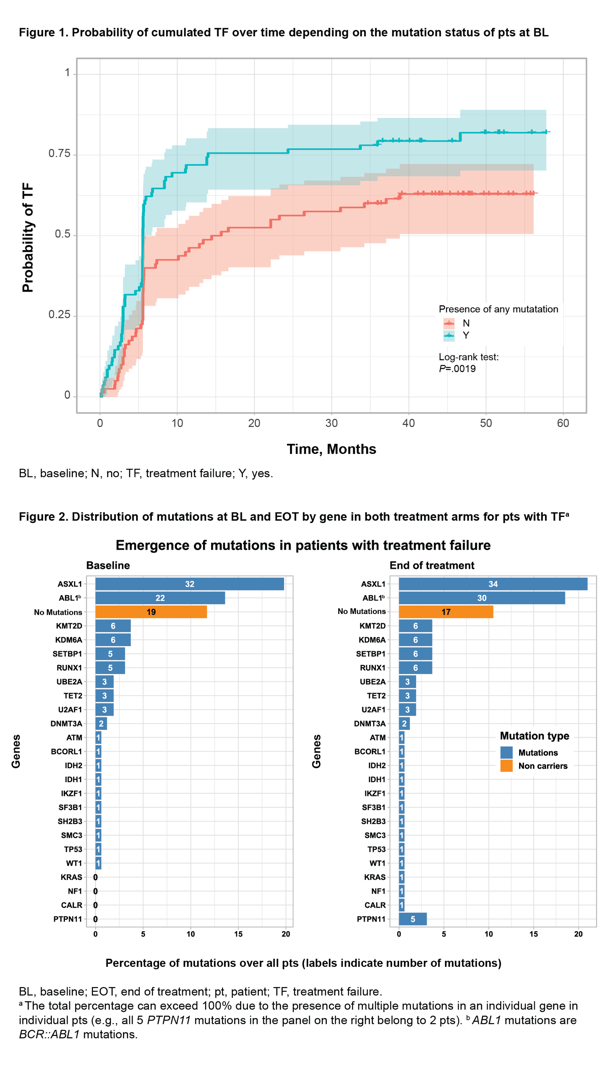
在基线时有162例患者接受检测,73例患者治疗失败且在治疗结束时有可用于分析的样本,只有3例患者因疾病进展而终止治疗。在总队列的162例患者中,基线时任何突变的存在都是治疗失败的显著预后判断因素(如图1)。在未经调整的分析中,基线时存在ASXL1突变且VAF>5%是治疗失败的预后判断因素。在73例治疗失败的患者中,大多数基线时的突变也在治疗结束时检测到(48/54例携带者中有110/116个突变)(如图2)。在治疗结束时发生≥1个突变的15例患者中,有9例发生ABL1突变。在个体或基因水平上没有单一突变是MMR的预后判断因素。当患者通过ASC或BOS的指定治疗进行检测时,突变不能预测MMR或治疗失败。
结论
ASXL1突变最常在CML诊断中检测到,在本研究中这种突变在先前接受过≥2种TKIs治疗的CML-CP患者基线时富集,这与TKI的耐药作用相一致。RUNX1和IKZF1突变与CML的加速期或急变期进展相关,在该研究患者人群中非常罕见,这支持它们在CML疾病进展中的作用。在CML-CP中,BCR::ABL1突变与血液肿瘤基因突变的高频率共存是一个重要的发现,因为癌症基因突变可以改变患者个体对TKIs的反应。基线时任何体细胞血液肿瘤突变的存在是治疗失败的预后判断因素。这些突变可作为潜在的生物标志物,帮助识别在后线治疗中可能具有较高治疗失败风险的患者。
摘要号449研究点评
在慢性髓系白血病(CML)可以检测到血液肿瘤相关基因的体细胞突变,最常见的突变基因是RUNX1、ASXL1、IKZF1和ABL1激酶结构域等,ASXL1是CML诊断中最常检测到的突变(≈9%)。这些突变在疾病进展时尤为常见,而且对TKI治疗效果可能有不利影响,其程度受两方面因素影响:一方面,受具体基因突变类型和位点的影响,有研究发现表观遗传学相关基因突变对疗效影响较轻,髓系肿瘤转录因子相关通路的基因突变则对疗效有显著影响;另一方面,治疗药物不同,基因突变对疗效的影响也有显著差异,尼洛替尼类二代药物有可能克服部分基因突变所致的疗效不佳,但是无法克服ASXL1突变的影响。
Asciminib是首个STAMP抑制剂,这些突变对STAMP抑制剂的疗效是否也会产生影响是一个值得关注的问题。ASCEMBL Ⅲ期研究纳入的是先前接受≥2种TKIs治疗的CML-CP患者,改用Asciminib治疗后的疗效和安全性,本研究对其中患者的肿瘤相关基因突变情况进行了描述性分析。有基线测序数据的162例患者中,102例(63%)具有≥1个突变,ASXL1(31%的患者)和ABL1激酶结构域(17%的患者)突变最常见。在基线时,27例患者有≥1个ABL1突变,85%的患者有≥1个其他癌症基因突变,12例(7.4%)同时出现ASXL1和ABL1突变。与既往未经治疗的患者数据相比,本研究纳入的多线治疗后患者突变率明显增高,这是患者筛选所致的富集结果,还是治疗诱导的结果值得探讨。本研究结果提示,极有可能是富集的结果,因为在73例治疗失败的患者中,大多数基线时的突变也在治疗结束时检测到。治疗结束后的最终结果显示,基线时任何突变的存在都显著提示治疗失败,基线时存在ASXL1突变且VAF>5%是治疗失败的预后判断因素。由于本研究试验组与对照组比例为2:1,因此,推测Asciminib很有可能也难以克服血液肿瘤相关基因所致的耐药。
本研究再一次证实血液肿瘤相关基因对CML-CP靶向药物治疗效果的不利影响,传统TKIs和新的STAMP抑制剂可能都无法克服这种影响,因此,何时检测这类基因突变成为令人关注的问题。研究证实多数这类基因突变很有可能不是治疗诱导产生,而是基线时已经存在,并在治疗过程中,随着难治病例的出现而逐渐富集。由于未治疗患者这类基因突变率偏低,且目前TKIs一线治疗的有效率较高,因此,未治疗患者一线检测这类基因突变依然未被推荐。从经济成本和提高检出率的平衡考虑,一线治疗3个月疗效不佳患者进行相关检查可能是比较合适的时机,此外,治疗早期出现严重血液学不良反应的患者也应该进行相关检测。但是,即使完成检测,如何克服检测阳性者的耐药性目前还缺乏研究,理论上提高服药依从性、选择强效TKIs、考虑不同机制药物的联合治疗都是可行的策略。最后,血液肿瘤相关基因突变还有可能成为独立的预后预测指标,最终被纳入更新的预后预测模型体系。
专家简介
段明辉教授

北京协和医院血液科主任医师北京医学会血液学分会第一届青委会副主委中华医学会血液学分会造血干细胞应用学组委员中国医药教育协会MPN/MDS分会副主任委员中国抗癌协会血液肿瘤专业委员会中国MDS和MPN工作组专家委员会委员中国临床肿瘤学会抗白血病联盟专家委员会委员中华慈善总会格列卫等患者援助项目血液领域专家委员会副主任委员卫生部临床医生科普项目医学科普专家重点方向是造血干细胞移植、淋巴瘤、白血病、MPN、MDS擅长各种血液科疑难罕见病的诊断治疗等