编者按:外周T细胞淋巴瘤(PTCL)是一组起源于成熟T细胞或NK细胞前体的异质性侵袭性淋巴瘤,占成人非霍奇金淋巴瘤的15%以下。根据世界卫生组织(WHO)及国际共识分类,其常见亚型包括间变性大细胞淋巴瘤(ALCL)、滤泡辅助T细胞(TFH)淋巴瘤、外周T细胞淋巴瘤-非特指型(PTCL-NOS)等。近年来,随着对PTCL分子机制的深入探索,靶向治疗策略显著改善了患者预后。其中,CD30抗体药物偶联物维布妥昔单抗(BV)凭借ECHELON-2试验的突破性数据,已成为CD30阳性PTCL的一线治疗基石。此外,组蛋白去乙酰化酶抑制剂(HDACi)、EZH2抑制剂、度维利塞(duvelisib)、芦可替尼及阿扎胞苷等新型药物在初治及复发/难治性(R/R)PTCL中的研究亦在推进,为分层治疗提供了新方向。
PTCL-NOS、ALCL及TFH淋巴瘤等结节型PTCL在欧美人群中最为常见,亦是本综述的核心焦点。根据WHO分类,TFH淋巴瘤需通过免疫组织化学检测至少表达两种标志物(BCL6、CD10、PD-1、CXCL13及ICOS)以确诊,并根据组织学特征进一步分为血管免疫母细胞型、滤泡型及非特指型。分子层面,TFH淋巴瘤常伴TET2、IDH2、DNMT3A及RHOA等表观遗传调控基因突变,提示其生物学机制的趋同性。而PTCL-NOS目前仍属排除性诊断,但随着对预后相关分子亚型(如TBX21、GATA3突变)的深入解析,其分类体系正逐步完善。
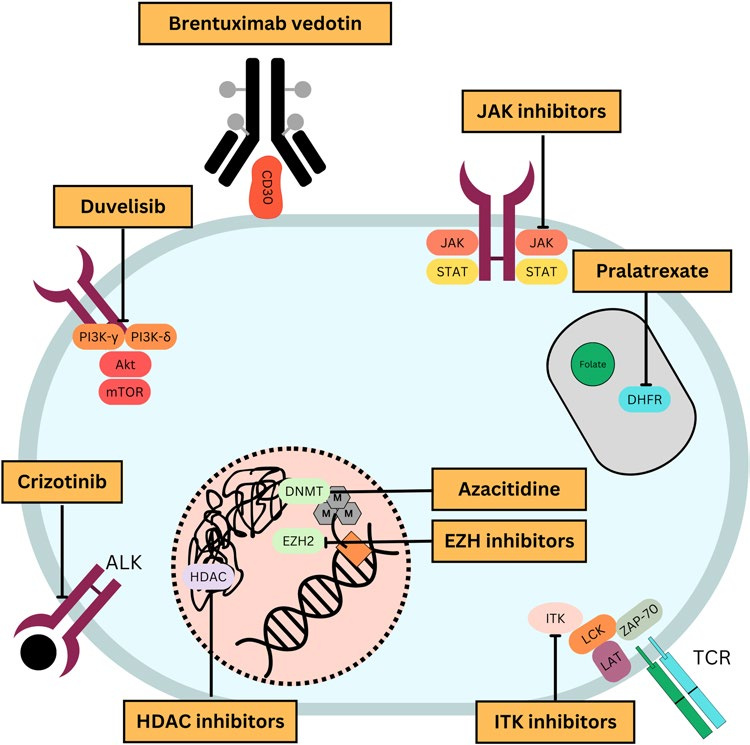 常用新型治疗PTCLs药物的作用机制
常用新型治疗PTCLs药物的作用机制
基于对PTCL生物学特征的深化认知,临床治疗模式正经历从传统化疗向靶向精准治疗的转型。目前,针对一线及复发/难治性(R/R)场景的新型药物研究已取得显著进展。以CD30抗体偶联药物BV为例,其联合化疗方案(BV-CHP)在CD30阳性PTCL患者中展现出优于传统CHOP的生存获益,标志着生物标志物驱动治疗策略的突破。此外,表观遗传调节剂(如HDACi、EZH2抑制剂)、PI3K抑制剂及JAK抑制剂等靶向药物的临床研究数据,亦为个体化治疗提供了新方向。以下将系统梳理当前新型药物在PTCL治疗中的整合路径,重点探讨其在初治及R/R患者中的应用前景。
 在一线或复发/难治性PTCLs治疗中研究过的一些新型药物
在一线或复发/难治性PTCLs治疗中研究过的一些新型药物
临床案例——STEP 1
患者男性,52岁,主诉乏力、盗汗、皮疹及多发淋巴结肿大。实验室检查显示贫血(血红蛋白9.2 g/dL)及血清乳酸脱氢酶升高(380 U/L)。PET/CT示腋窝、纵隔、腹股沟及腹膜后2-3 cm淋巴结肿大。淋巴结活检见CD3、CD5、CD10、BCL6、PD-1及ICOS阳性非典型淋巴细胞浸润,骨髓受累约10%,确诊为淋巴结滤泡辅助性T细胞淋巴瘤,血管免疫母细胞型(nTFHL-AI)。
Q:该患者一线治疗应如何选择?
PTCL一线治疗的现状与进展
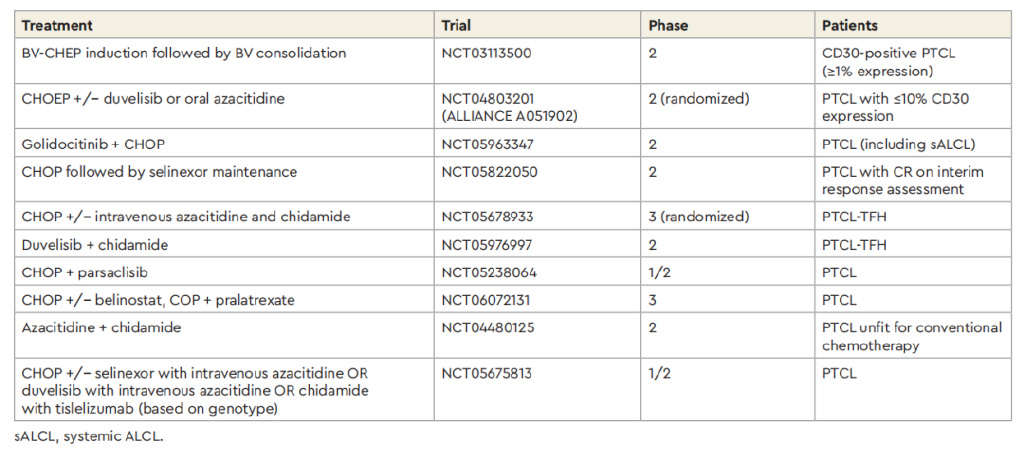 在PTCL一线治疗中使用新型药物的研究
在PTCL一线治疗中使用新型药物的研究
传统CHOP方案(环磷酰胺+多柔比星+长春新碱+泼尼松)仍是初治PTCL的一线标准治疗,但其疗效有限,5年总生存率(OS)仅35%。ECHELON-2研究通过将BV联合CHP方案(BV-CHP),显著提升了CD30表达≥10%患者的生存获益:5年无进展生存率(PFS)从43.0%提升至51.4%,5年OS从61.0%提升至70.1%,且未显著增加毒性。BV-CHP的疗效优势在ALCL亚型中尤为突出,但PTCL-NOS或AITL中CD30表达异质性较高,BV-CHP方案获益仍存争议。因此,BV-CHP目前仅推荐作为ALCL的标准治疗,其他亚型仍以CHOP为基础。
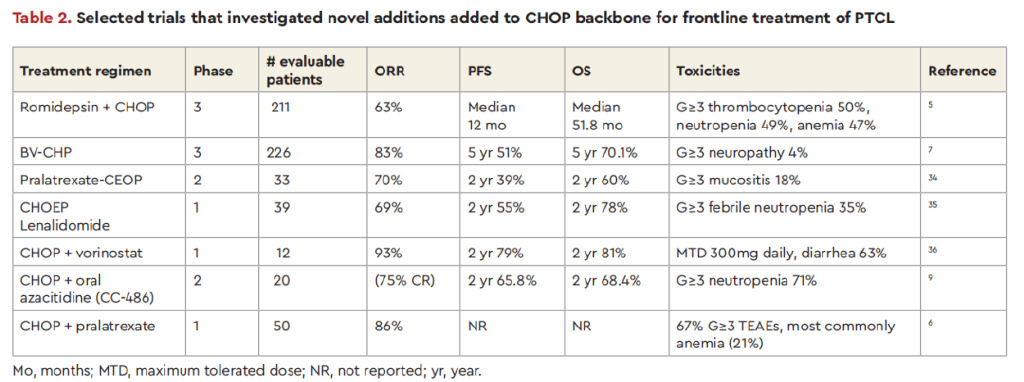 以CHOP为基础的方案中用于PTCL一线治疗的部分试验
以CHOP为基础的方案中用于PTCL一线治疗的部分试验
针对非ALCL亚型的探索中,一项II期研究尝试在CD30低表达(≥1%)PTCL中采用BV联合CHOEP方案(BV-CHEP),并序贯BV维持治疗,结果显示总缓解率(ORR)达90%以上,且安全性可控。此外,罗米地辛等HDACi联合CHOP的III期试验虽未显著改善整体预后,但亚组分析显示其在TFH淋巴瘤中可延长中位PFS(19.5个月 vs 10.6个月),提示HDACi在该亚型中的潜在价值。针对CD30阴性PTCL,小规模I/II期研究尝试在CHOP方案中联用口服阿扎胞苷等药物,结果显示TFH淋巴瘤患者的CR率达75%,目前美国多中心研究(NCT04803201)正在评估阿扎胞苷或度维利塞联合CHOP的疗效。
临床案例——STEP 2
患者完成6周期CHOEP方案(环磷酰胺+表柔比星+长春新碱+依托泊苷+泼尼松)治疗后,影像学评估显示完全代谢缓解。12个月后出现新发腋窝淋巴结肿大,PET/CT提示双侧腋窝及腹膜后淋巴结代谢活跃,左腋窝淋巴结穿刺活检证实为nTFHL-AI复发,CD30表达率为10%。
Q:该患者复发方案应如何选择?
R/R PTCL的新型治疗策略
复发/难治性PTCL预后极差,中位OS仅约9个月,现有治疗方案在缓解率及持续应答方面均存在显著局限。目前美国食品药品监督管理局(FDA)已批准的治疗药物包括罗米地辛、贝利司他、普拉曲沙、BV及克唑替尼(表4)。除ALCL外,其他亚型R/R PTCL尚无标准疗法。异基因造血干细胞移植虽可使近50%患者获得潜在治愈机会,但受限于疾病控制难度、供体匹配、年龄及合并症等因素,其临床应用受限。部分研究探索了自体移植巩固治疗的价值,但其具体作用仍需进一步验证。
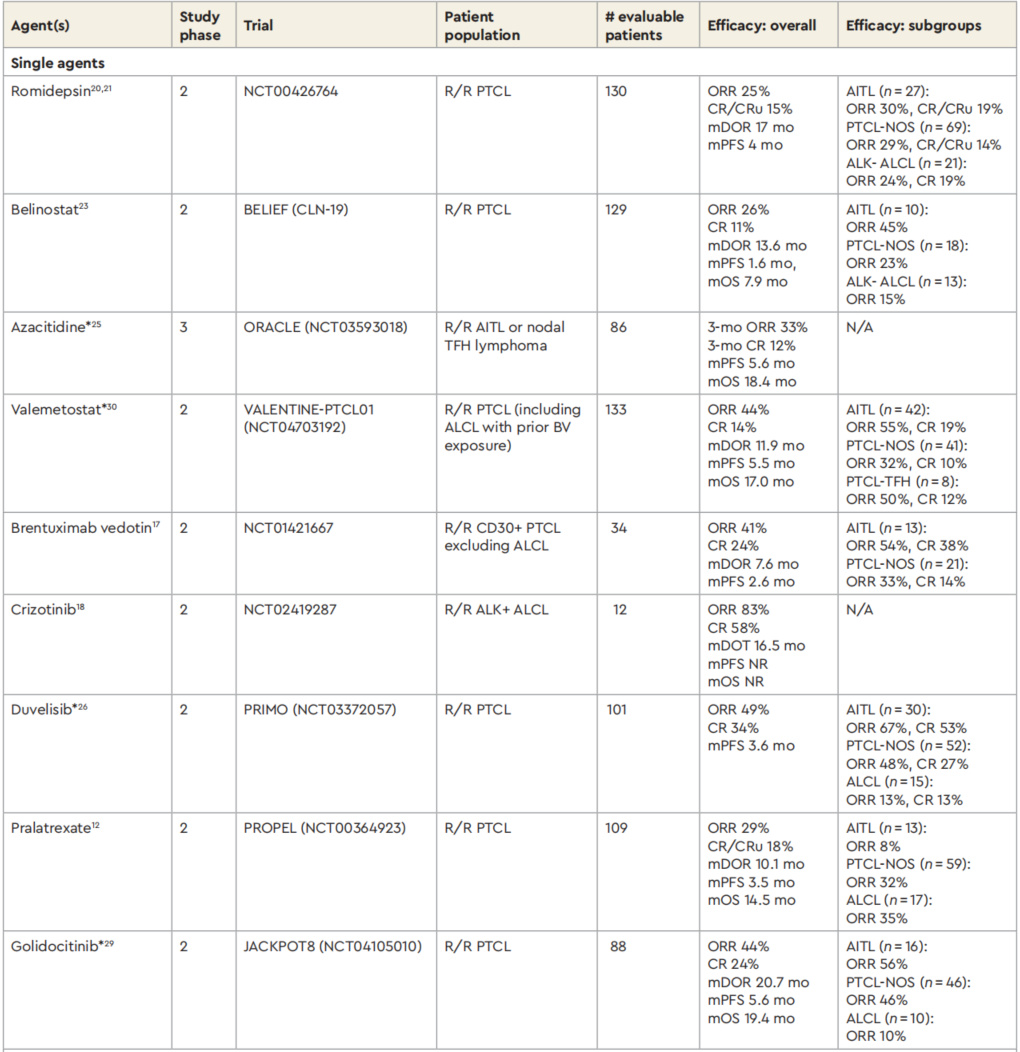 R/R PTCL的新药研究(单药)
R/R PTCL的新药研究(单药)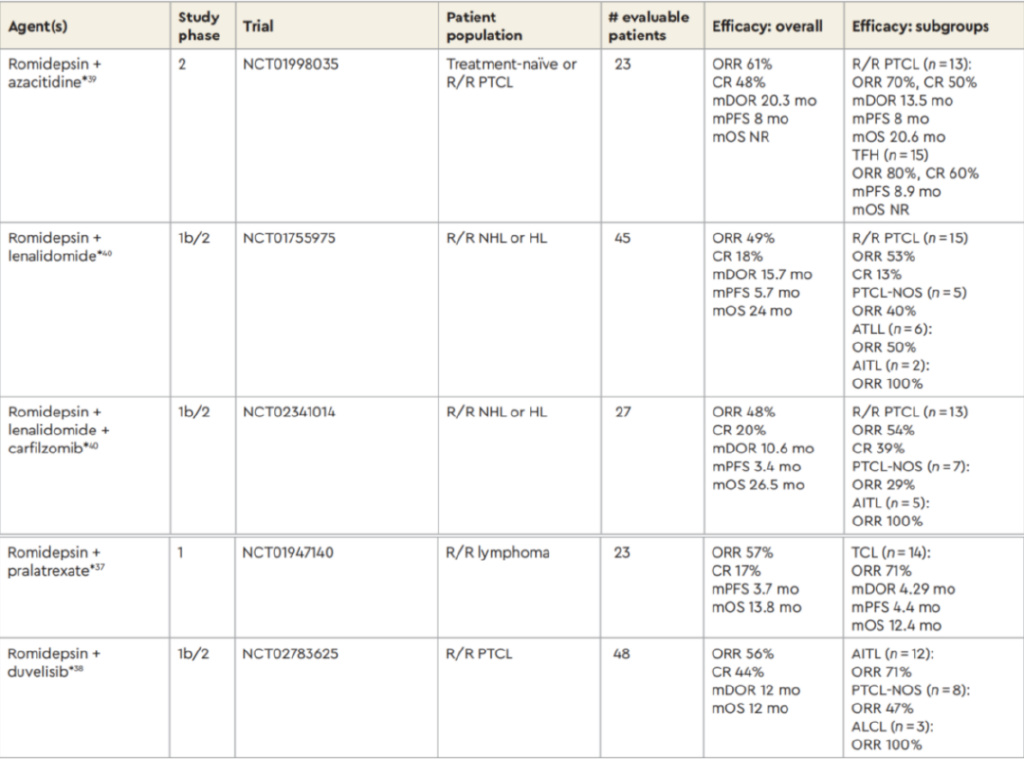 R/R PTCL的新药研究(联合)
R/R PTCL的新药研究(联合)
01、化疗方案
单药化疗方案在复发/难治性PTCL中仍为标准选择,其疗效优于联合化疗。抗叶酸类似物普拉曲沙的ORR为29%,中位PFS与OS分别为3.5个月和14.5个月。尽管初始研究采用30 mg/m²每周给药(7周为一周期)的方案,但因皮疹、血细胞减少及黏膜炎发生率较高,后续调整为每4周周期中的3周给药并加用亚叶酸钙以降低毒性。亚组分析显示,AITL患者缓解率较低(8%)。其他单药化疗方案包括吉西他滨及苯达莫司汀,而联合化疗方案(如ESHAP、ICE及GDP)虽可短期缓解,但应答持续时间有限。
同样,常用于复发/难治性侵袭性淋巴瘤的联合化疗方案,包括依托泊苷、甲基泼尼松龙、高剂量阿糖胞苷和顺铂(ESHAP)、异环磷酰胺、卡铂和依托泊苷(ICE)以及吉西他滨、地塞米松和顺铂(GDP),也可考虑使用,但缓解持续时间有限。
02、CD30靶向治疗
在获批一线治疗前,BV已在R/R ALCL及CD30阳性PTCL中显示出活性。AITL及PTCL-NOS患者的ORR分别为54%和33%,mDOR分别为6.7个月和1.6个月。值得注意的是,部分CD30低表达甚至阴性患者仍可获益。目前针对CD30的CAR-T及双特异性抗体研究正在进行,有望进一步扩展靶向治疗的应用范围。
03、ALK抑制剂
对于ALK阳性ALCL患者,ALK抑制剂是重要的治疗选择。克唑替尼基于儿童肿瘤学组研究数据获批,其ORR达88%,CR率81%,22%患者持续缓解≥12个月。第二代ALK抑制剂阿来替尼也在复发/难治性ALK阳性ALCL中显示出活性,并且可以作为克唑替尼的替代品,特别是在有中枢神经系统受累的患者中。
04、表观遗传调节剂
HDACi及去甲基化药物因PTCL中表观遗传调控基因突变高发(约75%)而备受关注,其中TFH淋巴瘤患者更常伴TET2、RHOA、DNMT3A及IDH2突变。罗米地辛作为首个在R/R PTCL中显示疗效的HDACi,其国际II期研究显示ORR为25%,CR率15%,中位mDOR达28个月。AITL亚组(n=27)ORR为33%,mDOR未达到。尽管罗米地辛于2021年退市,但其在皮肤T细胞淋巴瘤(CTCL)中仍保留临床应用。贝利司他在II期研究中ORR为25.8%,CR率10.8%,中位mDOR为13.6个月,AITL患者缓解率显著高于PTCL-NOS(45% vs 23%)。西达本胺在中国获批用于PTCL,其多中心II期研究显示AITL患者缓解更优。
去甲基化药物阿扎胞苷在TFH淋巴瘤中展现出潜力,III期研究显示其相较于研究者选择方案(苯达莫司汀、吉西他滨或罗米地辛)可延长中位PFS(5.6 vs. 2.8个月)及OS(18.4 vs. 10.3个月),尽管未达到主要终点,但其联合策略仍具探索价值。
临床案例——STEP 3
该患者接受BV治疗后,PET/CT评估显示部分缓解。但2个月后复查发现腹膜后新发大体积FDG高摄取淋巴结。
Q:该患者后续治疗应选择?
其他新型药物及未来方向
01、磷脂酰肌醇3激酶(PI3K)抑制剂
PI3K信号通路异常活化在PTCL中广泛存在。口服δ/γ亚型PI3K抑制剂度维利塞在PRIMO II期研究中显示出显著疗效:ORR达49%,CR率34%,中位无PFS为3.6个月。亚组分析显示AITL和PTCL-NOS患者获益更显著,ORR分别达67%和48%,中位PFS分别为9.1个月和3.5个月。需注意该药可能存在转氨酶升高、结肠炎、皮疹和感染的风险。
中国自主研发的PI3K-γ选择性抑制剂林普利塞(Linperlisib)在复发/难治性PTCL中ORR达48%,且腹泻(14%)及肝毒性(20-23%)发生率较低,国际多中心研究正在进行。
02、JAK/STAT通路抑制剂
基础研究证实JAK/STAT通路异常活化参与PTCL发病机制。JAK1/2抑制剂芦可替尼的II期研究显示,在JAK/STAT通路激活突变或pSTAT3过表达患者中,ORR分别达36%、37%,显著优于无通路激活组(7%)。新型高选择性JAK1抑制剂戈利昔替尼(Golidocitinib)在88例复发/难治性PTCL患者中ORR达44.3%,CR率为20.5%,中位缓解持续时间20.7个月,AITL亚组ORR提升至56.3%。中位PFS和OS分别为5.6个月和19.4个月。虽约55%的患者出现了3级或以上的治疗相关不良事件,但大多数为血液学事件。
03、EZH2抑制剂
EZH抑制剂是抑制EZH1或EZH2组蛋白甲基转移酶活性的小分子,在PTCL中具有治疗前景。多种EZH2抑制剂在PTCL中显示出活性,包括valemetostat、tulmimetostat和HH2853。在一项针对复发/难治性PTCL的国际II期单臂研究中,valemetostat的ORR为43.7%,AITL亚组提升至54.8%;CR率14.3%,中位DOR为11.9个月。Valemetostat耐受性良好,58%的患者出现≥3级不良事件,主要是血液学不良事件。同样,其他EZH2抑制剂(NCT04390737、NCT04104776)在PTCL中也显示出活性和耐受性。鉴于疗效和安全性,valemetostat作为单药和联合用药都具有前景,但目前在日本以外尚未获批用于标准治疗。
04、ITK抑制剂
白细胞介素-2诱导激酶(ITK)是 T 细胞受体信号传导的重要介质。研究表明,在AITL和其他结内TFH淋巴瘤中,ITK表达上调或异常激活。一种ITK抑制剂soquelitinib在一项I/Ib期临床试验中,在多线治疗失败PTCL患者中显示出活性,III期研究正在筹备。
05、免疫检查点抑制剂
尽管免疫检查点抑制剂在其他淋巴瘤(如皮肤T细胞淋巴瘤和NK/T细胞淋巴瘤)中具有疗效,但它们并非复发/难治性PTCL标准治疗的一部分。在PTCL中应用免疫检查点抑制剂的多项研究显示了超进展(定义为在1个周期内进展)的发生率。在单药纳武利尤单抗(n=12)和帕博利珠单抗(n=13)的研究中,ORR均为33%。
06、联合治疗策略
虽然新型药物主要作为单药治疗进行研究,但已评估了多种新型药物的联合应用或新型药物与化疗的联合应用。某些基于罗米地辛的联合方案在TFH淋巴瘤中显示出疗效。因此,新型药物的联合应用可能是未来重要的治疗模式。
展望
PTCLs的治疗格局已经开始随着新型药物的引入而转变。虽然最初是在复发/难治性环境中进行研究的,但现在一些新型药物正在被研究用于一线治疗方案。许多新型药物旨在利用PTCL亚型之间的生物学差异取得突破,包括ALCL和TFH淋巴瘤。对PTCL生物学的更深入理解将继续引领该领域的进一步发展,涉及检查点抑制剂、双特异性抗体、CAR-T细胞疗法和新型单克隆抗体的治疗仍在开发中。尽管进展众多,但多数患者预后仍不理想,亟须通过临床试验推动更多突破。