
免疫球蛋白轻链(AL)淀粉样变性是一种由单克隆浆细胞分泌的不稳定游离轻链异常沉积引发的难治性疾病,其治疗核心在于通过深度血液学缓解改善或逆转器官功能障碍。传统治疗方案已无法充分满足AL患者需求,而针对恶性浆细胞或淀粉样蛋白的靶向治疗正在显著改善预后。基于2024年美国血液学会(ASH)年会最新报告,发表在Journal of Hematology & Oncology上的文章系统阐述了AL淀粉样变性的靶向治疗进展。
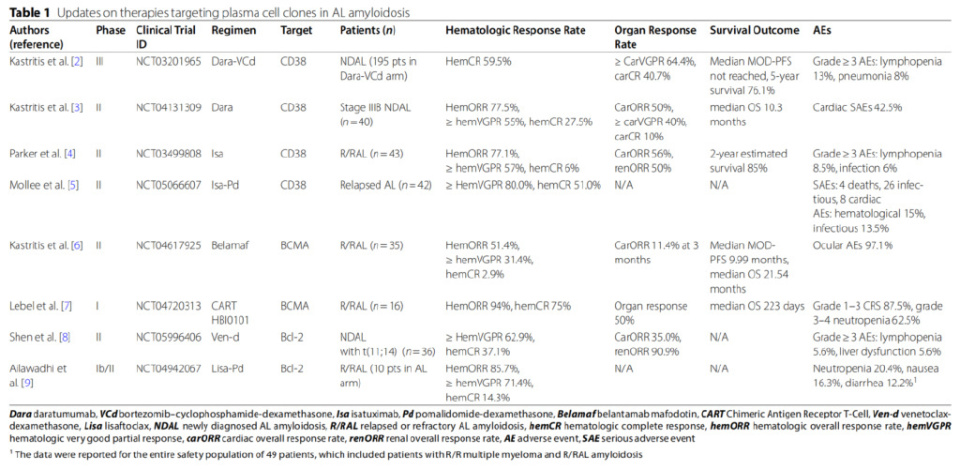
针对AL淀粉样变性中浆细胞克隆的最新治疗进展
CD38靶向治疗药物突破
01、达雷妥尤单抗
基于ANDROMEDA研究中观察到的优异应答率,达雷妥尤单抗(Daratumumab)联合硼替佐米、环磷酰胺和地塞米松(Dara-VCd)方案成为首个且唯一获美国食品药品监督管理局(FDA)加速批准用于AL的靶向疗法。Kastritis等研究者公布的ANDROMEDA研究最终分析显示,中位随访61.4个月时,Dara-VCd组较VCd组显著延长新诊断(ND)AL淀粉样变性患者的中位主要器官恶化无进展生存期(NR vs. 30.2个月,P<0.0001),及5年总生存率(76.1% vs. 64.7%,P=0.0121)。
针对ⅢB期心功能不全ND患者的EMN22研究显示,达雷妥尤单抗单药治疗初治IIIB期患者血液学总体缓解率(hemORR)达77.5%,其中27.5%实现了血液学完全缓解(hemCR)和血液学非常好的部分缓解(hemVGPR)。此外,在40例患者中,有50%观察到心脏应答,有望使严重心脏功能障碍患者受益。然而,该研究也提出了一些担忧,即这些超高风险患者的早期死亡率为27.5%,严重不良事件(SAE)致死率为42.5%,提示需严格评估获益风险比。
02、艾沙妥昔单抗
SWOG S1702研究评估了另一种抗CD38单克隆抗体艾沙妥昔单抗(Isatuximab),作为复发或难治性(R/R)AL淀粉样变性的单药治疗疗效——实现了77.1%的hemORR,其中57%达到hemVGPR或以上,56%的患者出现心脏缓解,50%的患者出现肾脏缓解。
在ISAYP研究中,当艾沙妥昔单抗与泊马度胺和地塞米松联合治疗复发AL淀粉样变性时,80%的患者在6个周期后达到hemVGPR或以上,包括51.0%的hemCR。最常见的不良事件是血细胞减少和感染。值得注意的是,研究方案规定泊马度胺的剂量为每天4毫克,但由于中性粒细胞减少或皮疹,35%的患者需要将剂量调整为每天3毫克。
BCMA靶向疗法进展
01、抗体偶联药物
抗BCMA抗体偶联药物(ADC)belantamab mafodotin(belamaf)在EMN27研究中单药治疗35例R/R AL淀粉样变性患者,hemORR达51.4%(31.4%≥hemVGPR),中位总生存期(OS)和MOD-PFS分别为21.54和9.99个月,最常见的≥3级不良事件是眼部毒性。
02、嵌合抗原受体T细胞
在一项1a/b期研究中,Lebel等研究者纳入了16例中位接受过4线既往治疗的R/R AL淀粉样变性患者,以评估抗BCMA嵌合抗原受体T细胞(CAR-T)HBI0101的疗效。尽管14/16(88%)例患者为三重难治性(triple-refractory),6/16(38%)例患者为belamaf难治性,但15/16(94%)例患者实现了hemORR,12/16(75%)例患者达到hemCR。14例可评估患者中,9例达到微小残留病(MRD,10-5)阴性,表明深度血液学应答疗效。虽然未报告与治疗相关的死亡,但在随访期间有7例患者死亡,其中3例处于血液学缓解状态。
Bcl-2通路抑制剂探索
一项II期研究评估了维奈克拉作为一线治疗t(11;14) AL淀粉样变性的疗效。在29例可评估应答的患者中,观察到62.9%的患者达到hemVGPR或以上,hemCR率为37.1%。6个月时,35.0%的患者出现心脏缓解,而90.9%的患者出现肾脏缓解。
Lisaftoclax是一种新型选择性Bcl-2抑制剂,每日口服剂量范围为400至1000毫克,在1b/2期研究中尝试与泊马度胺和地塞米松联合治疗R/R AL淀粉样变性。结果显示hemORR为85.7%,71.4%的可评估患者达到hemVGPR或以上,2例患者出现心脏缓解。
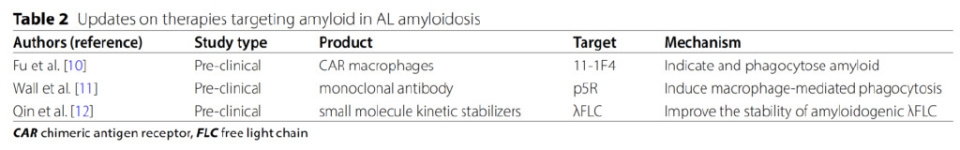
针对AL型淀粉样变性中淀粉样蛋白的最新治疗进展
淀粉样蛋白靶向治疗
CD34+造血干细胞来源的11-1F4-CAR巨噬细胞在体外及人源化AL淀粉样瘤小鼠模型中均显示出有前景的淀粉样物质靶向和吞噬作用。
AT-02是一种在研的人源化IgG1肽融合蛋白,含有泛淀粉样蛋白反应肽 (p5R)。该单克隆抗体可通过肽相互作用与淀粉样物质结合,激活巨噬细胞吞噬作用,并诱导补体激活,有望清除沉积的淀粉样物质并逆转器官功能障碍。
此外,一项临床前研究调查了通过增强淀粉样变性蛋白的动力学和热力学稳定性来减轻毒性的小分子动力学稳定剂。
这些淀粉样物质靶向疗法亟需更多的临床证据以评估其在人类患者中的应用可行性。
总结与展望
综上所述,2024年ASH年会揭示了AL靶向治疗的多维度进展,从浆细胞清除到淀粉样蛋白直接靶向形成全面布局。此外,尽管新型单克隆抗体CEAL-101和Birtamimab等疗法未在本次会议报告,其初步临床结果已显露出潜力。未来,需通过大规模前瞻性研究深化认知,提供进一步的临床证据,以推动AL淀粉样变性治疗范式革新。
参考文献:
1. Kastritis E, Palladini G, Minnema MC, Wechalekar AD, Jaccard A, Lee HC, Sanchorawala V, Gibbs S, Mollee P, Venner CP, et al. Daratumumab-Based treatment for Immunoglobulin Light-Chain amyloidosis. N Engl J Med. 2021;385(1):46–58.
2. Kastritis E, Palladini GO, Minnema MC, Wechalekar AD, Jaccard A, Lee HC, Sanchorawala V, Mollee P, Lu J, Schönland S, et al. Subcutaneous daratumumab (DARA) + Bortezomib, cyclophosphamide, and dexamethasone (VCd) in patients with newly diagnosed light chain (AL) amyloidosis: overall survival and final major organ deterioration Progression-Free survival results from the phase 3 Andromeda study. Blood. 2024;144(Supplement 1):891.
3. Kastritis E, Minnema MC, Dimopoulos M-A, Merlini G, Theodorakakou F, Fotiou D, Huart A, Belhadj Merzoug K, Golfinopoulos S, Antoniou N, et al. Efficacy and safety of daratumumab monotherapy in newly diagnosed patients with stage 3B light chain amyloidosis: A phase 2 study by the European myeloma network. Blood. 2024;144(Supplement 1):1979.
4. Parker TL, Rosenthal A, Sanchorawala V, Landau HJ, Campagnaro EL, Kapoor P, Neparidze N, Girnius S, Hagen P, Scott EC, et al. Isatuximab in relapsed AL amyloidosis: results of a prospective phase II trial (SWOG S1702). Blood. 2024;144(Supplement 1):3378.
5. Mollee P, Huart A, Mortona O, Queru K, Leyronnas C, Stephanie H, Sidiqi H, Desport E, Vincent L, Macro M, et al. Efficacy and safety of isatuximab, Pomalidomide and dexamethasone in relapsed AL amyloidosis: interim results of the Isamyp phase 2 joint study from the IFM and ALLG. Blood. 2024;144(Supplement 1):892.
6. Kastritis E, Palladini GO, Dimopoulos M-A, Jaccard A, Merlini G, Theodorakakou F, Fotiou D, Minnema MC, Wechalekar AD, Golfinopoulos S, et al. Efficacy and safety of Belantamab Mafodotin monotherapy in patients with relapsed or refractory light chain amyloidosis: an updated analysis of a phase 2 study by the European myeloma network. Blood. 2024;144(Supplement 1):1927.
7. Lebel E, Asherie N, Assayag M, Elias S, Grisariu S, Avni B, Kfir-Erenfeld S, Dubnikov-Sharon T, Alexander-Shani R, Bessig N, et al. Efficacy and safety of Anti-BCMA chimeric antigen receptor T-Cell (CART) for the treatment of relapsed and refractory AL amyloidosis. Blood. 2024;144(Supplement 1):894.
8. Shen K, Guan A, Wu Y, Sun C, Zhong L, Luo J, Li J. Venetoclax plus dexamethasone as First-Line treatment for t(11; 14) Light-Chain Amyloidosis: Preliminary Result of a Phase II Prospective, Multicenter, Single-Arm Study. Blood. 2024;144(Supplement 1):893.
9. Ailawadhi S, Chanan-Khan AA, Khouri J, Yannakou CK, Chen Z, Wang Y, Guo H, Wang H, Li M, Ahmad M, et al. Lisaftoclax (APG-2575) combined with novel therapeutic regimens in patients (pts) with relapsed or refractory multiple myeloma (R/R MM) or Immunoglobulin Light-Chain (AL) amyloidosis. Blood. 2024;144(Supplement 1):1022.
10. Fu J, Ma H, Li S, Hughes MS, Kalantarov G, Liu G, Mapara M, Lentzsch S. Development of Anti-Amyloid 11-1F4- CAR phagocytes for treatment of AL amyloidosis. Blood. 2024;144(Supplement 1):360.
11. Wall JS, Kennel SJ, Stuckey A, Richey T, Williams AD, Balachandran M, Hancock T, Jackson JW, Wooliver DC, Macy S, et al. Characterization of AT02 bioactivity and an assessment of its potential use as an Amyloid-Clearing therapeutic for AL amyloidosis. Blood. 2024;144(Supplement 1):4641.
12. Qin B, Jackman AB, Li Y-C, Wang J, Qiu H, Onpaeng N, Wilkens S, Grant V, Stanfield RL, Wilson I, et al. Small molecule kinetic stabilizers reduce amyloidogenicity of free light chain proteins of diverse sequences in Λ light chain amyloidosis. Blood. 2024;144(Supplement 1):3372.