编者按:2025年美国临床肿瘤学会(ASCO)年会于5月30日-6月3日在美国芝加哥圆满召开。作为全球临床肿瘤领域最具规模与影响力的学术盛会,ASCO年会汇聚世界顶尖肿瘤学专家,共同聚焦前沿研究与临床难题,推动全球癌症治疗持续进步。在本届大会上,浙江大学医学院附属第一医院金洁教授团队多项研究入选壁报展示,涵盖EZH2抑制剂、JAK/ACVR1双重抑制剂、SIRPα融合蛋白等新型药物在淋巴瘤、骨髓纤维化和CMML中的最新临床应用。本文遴选三项代表性研究进行集中介绍,展现中国团队在血液肿瘤精准治疗领域的最新探索与临床贡献。

1
摘要号:6571
标题:An exploratory analysis of myelofibrosis (MF) patient subgroups by baseline hemoglobin levels in the gecacitinib phase 3 trial
中文标题:基于基线血红蛋白水平的骨髓纤维化(MF)患者亚组探索性分析:来自 Gecacitinib Ⅲ期临床试验的数据
第一作者:Yi Zhang
背景
贫血是骨髓纤维化(MF)的关键预后指标。在双盲、随机的Ⅲ期ZGJAK016试验中,吉卡昔替尼(Gecacitinib,GCA)——一种双重JAK/ACVR1抑制剂,相较于羟基脲,在脾脏反应方面表现出优越性,并在JAK抑制剂初治患者(pts)中显示出改善MF相关贫血及症状的趋势。为了进一步明确GCA对贫血的影响,我们对该试验的数据进行了事后分析,依据贫血的严重程度对患者进行分组。
方法
在GCA组中,根据基线血红蛋白(Hb)水平对患者进行事后亚组划分:低于100 g/L(中重度贫血)、100 g/L至正常值下限(LLN)(轻度贫血)、LLN至正常值上限(ULN)(正常),以及超过ULN(Hb升高)。主要终点是在第24周时脾脏体积较基线减少≥35%的患者比例(SVR35)。次要终点包括第24周时总症状评分(TSS)降低≥50%的患者比例(TSS50),以及输血非依赖(TI)率(在第24周前的最后12周内未输注红细胞且Hb水平不低于80 g/L)。
结果
在71例随机分配至GCA治疗的意向治疗(ITT)人群患者中,47例(66.2%)基线时为中重度贫血(包括16例[22.5%]重度贫血患者,即Hb水平低于80 g/L),11例(15.5%)为轻度贫血,13例(18.3%)为非贫血(包括3例[3.8%]Hb水平高于ULN的患者)。在中重度贫血亚组中,较高比例的患者被归类为DIPSS高危、输血依赖,且基线时诊断为原发性骨髓纤维化。轻度贫血组的大多数患者为非输血依赖,而非贫血亚组的所有患者均为非输血依赖。三例Hb升高的患者均患有继发于真性红细胞增多症后的骨髓纤维化。所有GCA亚组的平均Hb水平在第2周时上升,随后在贫血亚组中保持稳定,或在正常亚组中略有下降但仍高于110 g/L,在Hb升高亚组则显著下降。除Hb升高亚组外,各亚组的平均血小板计数在第2周时下降,之后保持稳定。在中重度和轻度贫血亚组中,在基线时为非输血依赖的36例患者中有24例(66.7%)在第24周维持了非输血依赖状态,基线时输血依赖的22例患者中有8例(36.4%)在第24周达到了非输血依赖。各亚组在第24周的SVR35率和TSS50率相似,与ITT人群观察到的结果一致。
结论
综上所述,对于基线时患有轻度、中重度或无贫血的JAK抑制剂初治MF患者,尤其是基线Hb水平低于LLN的患者,GCA在脾脏和症状管理以及贫血方面提供了三重益处。
2
摘要号:7053
标题:A phase I study of the EZH2 inhibitor TR115 in patients with relapsed/refractory non-Hodgkin's lymphomas and advanced solid tumors.
中文标题:EZH2 抑制剂 TR115 治疗复发/难治性非霍奇金淋巴瘤和晚期实体瘤的I 期研究
第一作者:金洁
背景
EZH2功能获得性突变及其过度表达可导致H3K27me3水平异常升高,进而驱动肿瘤的发生与转移,广泛见于多种B细胞及T细胞淋巴系统恶性肿瘤,并与不良预后密切相关。TR115是一种新型、高选择性、口服给药的EZH2抑制剂,在临床前模型中展现出显著的抗肿瘤活性。本项I期研究旨在评估TR115在复发/难治性非霍奇金淋巴瘤(NHL)及晚期实体瘤患者中的安全性、耐受性及初步疗效。
方法
剂量爬坡起始于200 mg(每日两次),最高递增至1600 mg(每日两次)。患者以28天为一个治疗周期口服TR115,直至疾病进展、出现不可接受的不良反应或患者主动退出。不良事件(AEs)按照NCI-CTCAE v5.0标准进行分级。疗效评估依据Lugano 2014标准(淋巴瘤)和RECIST v1.1标准(实体瘤)进行。
结果
截至2025年1月10日,共入组20例患者,包括:血管免疫母细胞性T细胞淋巴瘤(AITL,4例)、弥漫大B细胞淋巴瘤(DLBCL,4例)、卵巢癌(4例)、ALK阴性间变性大细胞淋巴瘤(ALCL,2例)、非特指型的外周T细胞淋巴瘤(PTCL-NOS,2例)、蕈样肉芽肿(1例)、滤泡性淋巴瘤(FL,1例)、黏膜相关淋巴组织淋巴瘤(MALT,1例)及乳腺癌(1例)。中位年龄为61岁(范围37-77岁),男女性别比例为1:1。大多数患者已接受过多线治疗(中位治疗线数为2)。
最常见的治疗相关不良事件(TRAEs)(所有级别/≥3级)包括:血小板减少(50%/15%)、白细胞减少(45%/10%)、贫血(40%/15%)、中性粒细胞减少(35%/10%)、高甘油三酯血症(35%/5%)、肌酐升高(35%/0%)、乳酸脱氢酶升高(25%/0%)、低钾血症(25%/5%)、高胆红素血症(20%/0%)、乏力(20%/5%)、低蛋白血症(20%/0%)、上呼吸道感染(10%/5%)。
在11例可评估疗效的NHL患者中,总缓解率(ORR)为63.6%,疾病控制率(DCR)为81.8%。其中6例PTCL患者的ORR达100%,4例仍在接受TR115治疗。1例PTCL-NOS患者达完全缓解(CR),目前已进入第16周期治疗。药代动力学数据显示AUC0–24h和Cmax呈剂量依赖性变化,中位Tmax为2小时。
结论
TR115在复发/难治性非霍奇金淋巴瘤患者中展现出良好的安全性和初步疗效,尤其在PTCL亚型中疗效突出。后续研究应进一步探索TR115的单药潜力及其在关键治疗组合中的应用前景(NCT05650580)。
3
摘要号:6577
标题:Updated results of a phase 2 study: Timdarpacept (IMM01) combined with azacitidine (AZA) as the first-line treatment in adults with chronic myelomonocytic leukemia (CMML)
中文标题:Timdarpacept(IMM01)联合阿扎胞苷(AZA)用于初治慢性粒单核细胞白血病(CMML)成人患者的一线治疗:Ⅱ期研究最新结果
第一作者:佟红艳
背景
Timdarpacept是一种重组信号调节蛋白α(SIRPα)IgG1融合蛋白,通过阻断“不要吃我”信号并激活“吃我”信号,诱导强效的抗体依赖性细胞吞噬作用(ADCP)从而发挥抗肿瘤活性。
方法
本研究(NCT05140811)旨在评估Timdarpacept联合AZA作为初治CMML患者一线治疗的安全性与有效性。Timdarpacept 2.0 mg/kg,每周静脉注射一次;AZA 75 mg/m2,第1-7天皮下注射,每28天为一个周期。
结果
截至2024年12月31日,共纳入24例患者,中位年龄62岁,男性占62.5%,ECOG评分≥1者占75.0%。其中33.3%为CMML-1,66.7%为CMML-2。多数患者基线血液学状况较差,中位血红蛋白(Hb)为69.5(32–132)g/L,中位血小板计数(PLT)为73.5(5–667)×109/L。中位随访时间为21.0个月(95%CI:19.3–23.3)。
在22例可评估疗效的患者中,总缓解率(ORR)为72.7%,包括完全缓解(CR)27.3%,伴血液学改善(HI)的骨髓CR(mCR)13.6%,单纯HI 4.5%,单纯mCR 27.3%。中位起效时间(TTR)为1.8个月,中位缓解持续时间(DoR)为16.9个月(95%CI:5.1–未达)。中位CR所需时间(TTCR)为3.7个月,中位CR持续时间(DoCR)为13.6个月(95%CI:5.7–未达)。中位无进展生存期(PFS)为17.8个月(95%CI:5.3–未达),12个月PFS估算值为59.0%(95%CI:33.4–77.6)。中位总生存期(OS)尚未达到。
常见的≥3级治疗相关不良事件(TRAEs,发生率≥10%)包括淋巴细胞减少(66.7%)、白细胞减少(62.5%)、中性粒细胞减少(58.3%)、血小板减少(50.0%)、贫血(29.2%)和肺炎(16.7%)。在未使用低剂量诱导方案的前提下,1例患者(4.2%)出现≥3级溶血。
结论
在未使用低剂量诱导治疗下,Timdarpacept与AZA联合用于初治CMML患者具有良好的耐受性。与既往AZA单药治疗的历史数据相比,该联合方案在CMML-1和CMML-2初治人群中展现出良好的疗效,值得进一步研究。
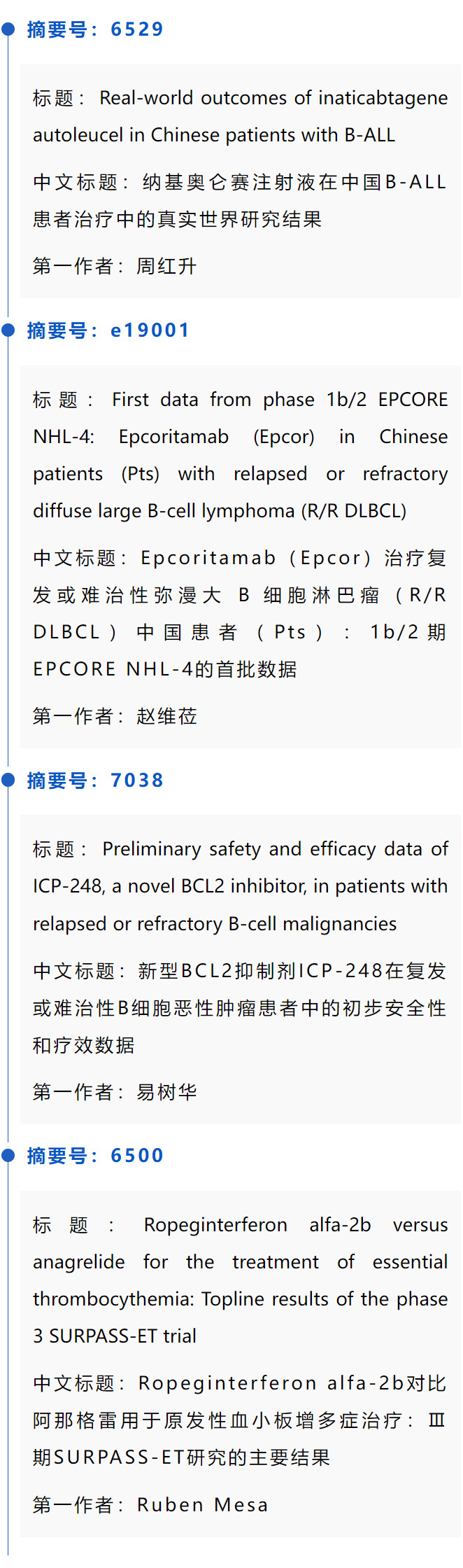
其他合作入选研究
专家简介

金洁 教授
浙江大学医学院附属第一医院
主任医师,博士生导师浙江大学医学院附属第一医院血液科荣誉科主任、学科带头人浙大一院淋巴瘤中心主任享受国务院特殊政府津贴浙江大学血液肿瘤(诊治)重点实验室主任浙江大学医学院血液学教研室主任卫生部国家临床重点建设单位学科带头人浙江省重点创新团队白血病基础与临床研究创新团队带头人中国女医师协会血液学专委会主任委员抗癌协会血液疾病转化医学主任委员CSCO中国抗白血病联盟副主任委员中国医师协会整合血液学会副主任委员