第30届欧洲血液学会年会(EHA 2025)于6月12日至15日在意大利米兰盛大召开。作为全球血液学领域的顶尖学术盛会之一,本届大会全面聚焦血液学及其各亚专科的最新进展,深入探讨循证诊疗新方法,发布临床与转化研究的重磅成果,呈现创新技术、精准诊断工具与风险评估策略的最新突破。在本届大会上,经过严格的评审过程,中国医学科学院血液病医院(中国医学科学院血液学研究所)共有4篇高质量的摘要脱颖而出,入选口头报告。其中1篇口头报告更是入选了LBA。此外,还有48篇摘要入选壁报展示。《肿瘤瞭望-血液时讯》特别整理4篇口头报告的具体内容。
口头报告一
LBA专场
摘要号:LB4004
英文标题:SAFETY AND EFFICACY OFCM313IN ADULTS WITH IMMUNE THROMBOCYTOPENIA: A RANDOMIZED, PLACEBO-CONTROLLED TRIAL
中文标题:CM313用于成人免疫性血小板减少症的安全性与疗效:一项随机、安慰剂对照试验
汇报人:Yanmei Xu(张磊教授团队)
报告时间:6月15日 10:00-10:15(当地时间)
报告地点:Gold Hall
研究背景
原发性免疫性血小板减少症(ITP)是一种复发性自身免疫性疾病,通常需要多线治疗。CM313是一种新型抗CD38单克隆抗体,可选择性耗竭表达CD38的细胞(包括浆细胞)。
研究目的
本研究是一项II期、多中心、随机、双盲、安慰剂对照试验,旨在评估CM313在持续性或慢性ITP成年患者中的有效性和安全性。入组患者需满足:糖皮质激素治疗失败或复发,且既往对标准一线治疗有应答。
研究方法
受试者随机分配接受静脉注射CM313(16 mg/kg)或安慰剂,每周一次,共8周。主要终点为第8周的客观缓解率(ORR),定义为连续至少两次血小板计数≥30×10?/L,即血小板计数较基线翻倍,且无出血症状。
研究结果
2024年1月16日至6月11日期间,共入组45例患者,按2:1的比例随机分配接受CM313(n=30)或安慰剂(n=15)治疗。第8周时,CM313组达到ORR的患者比例(83%)显著高于安慰剂组(20%),绝对差异达63%(95%CI:33.7-81.3;P<0.0001)。CM313组患者血小板计数≥50×109/L的中位时间为1周,而安慰剂组在同期未达到该阈值(P<0.0001)。此外,CM313组血小板计数维持≥50×109/L的中位累积持续时间为18周,显著长于安慰剂组的3周(P=0.0035)。CM313组和安慰剂组不良事件的发生率分别为83%和80%,最常见的不良事件为输注相关反应和瘀点,未观察到意外安全信号。
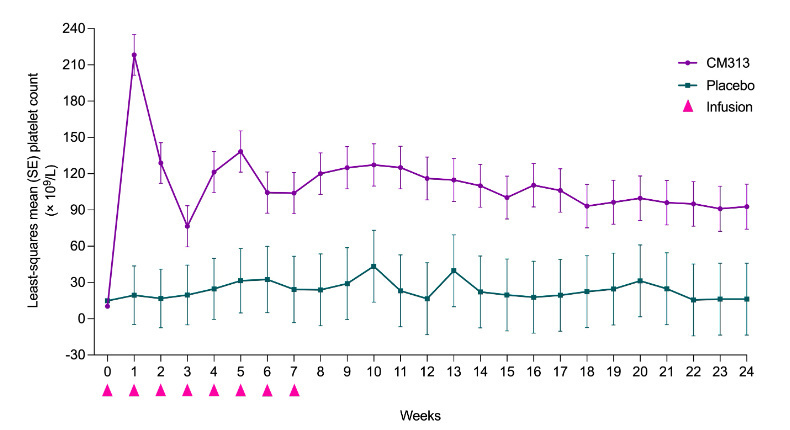
研究结论
CM313耐受性良好,并显示出具有临床意义的疗效,表现为血小板计数快速升高、疗效持久且出血风险降低。
口头报告二
AML的新型治疗与FLT3抑制剂专场
摘要号:S143
英文标题:LONG-TERM FOLLOW-UP OF PREDOMINANTLY ASIAN PATIENTS WITH RELAPSED/REFRACTORY FLT3-MUTATED ACUTE MYELOID LEUKEMIA TREATED WITH GILTERITINIB VERSUS SALVAGE CHEMOTHERAPY IN THE PHASE 3 COMMODORE TRIAL
中文标题:Ⅲ期COMMODRE试验中接受吉瑞替尼与挽救化疗治疗的复发/难治性FLT3突变急性髓系白血病患者(以亚洲患者为主)的长期随访
汇报人:王建祥教授
报告时间:6月15日11:45-12:00(当地时间)
报告地点:Coral 4+5
研究背景
针对亚洲复发/难治性(R/R)FMS样酪氨酸激酶(FLT3)突变(FLT3mut+)急性髓系白血病(AML)患者使用吉瑞替尼的随机对照试验长期数据有限。
研究目的
COMMODORE Ⅲ期研究(NCT03182244)评估了吉瑞替尼对比挽救化疗(SC)在中国、东南亚及俄罗斯R/R FLT3mut+ AML患者中的有效性和安全性。本文报告其长期随访结果。
研究方法
本项III期、开放标签、多中心研究纳入中国、马来西亚、泰国、新加坡和俄罗斯48个研究中心的 R/R FLT3mut+ AML患者,按1:1随机分配至吉瑞替尼(120 mg/日)或挽救化疗组[低剂量阿糖胞苷;米托蒽醌+依托泊苷+中剂量阿糖胞苷;或氟达拉滨+大剂量阿糖胞苷+粒细胞集落刺激因子]。入组标准包括:原发性AML或继发于骨髓增生异常综合征的AML成年患者(年龄≥18岁或符合当地规定),其一线治疗后仍为R/R,中心检测结果为FLT3mut+,且东部肿瘤协作组(ECOG)体能状态评分≤2。排除标准包括:急性早幼粒细胞白血病、急变期慢性髓性白血病、化疗诱导AML或活动性中枢神经系统疾病。长期随访期间,患者每3个月进行一次评估,自结束治疗访视起最长随访3年。主要终点为总生存期(OS),次要终点包括无事件生存期(EFS)、完全缓解(CR)率、输血率(仅吉瑞替尼组)、复合完全缓解(CRc)率、造血干细胞移植(HSCT)率,其他疗效终点包括总体缓解率。
研究结果
共入组 276 例患者(吉瑞替尼组 137 例,挽救化疗组 139 例)。截至 2023 年 12 月 25 日,所有患者均已完成最终评估。研究结束分析显示,243 例(88.0%)为亚洲患者。吉瑞替尼组和挽救化疗组的中位OS随访时间分别为 37.6个月(95%CI:35.0, 42.0)vs 34.1个月(95% CI:17.2, 34.4)。中位 OS 分别为 10.3个月(95%CI:8.8, 12.7)vs 5.4个月(95%CI:4.1, 8.1) [风险比(HR)0.61,95%CI:0.45-0.83]。中位 EFS分别为2.1个月(95%CI:<0.1, 3.2)vs 0.6个月(95%CI:0.2, 1.2)(HR 0.59,0.44-0.79)。吉瑞替尼组较挽救化疗组的CR率(20.4% vs. 11.5%)、CRc率(53.3% vs. 22.3%)和总体缓解率(67.9% vs. 27.3%)更高。吉瑞替尼组和挽救化疗组达到CR中位时间为3.7个月(1-19)vs 1.1个月(1-2);达到CRc中位时间分别为1.8个月(1-8)vs. 1.0个月(1-2)。研究期间,吉瑞替尼组31例(22.6%)和挽救化疗组11例(7.9%)患者接受HSCT(包括治疗后序贯HSCT)。吉瑞替尼组25例(18.2%)接受HSCT的患者中,其中18例(72.0%)患者在接受HSCT后恢复吉瑞替尼治疗。吉瑞替尼组输血转换率为47/101(46.5%),维持率为17/24(70.8%)。安全性结果与主要分析一致,未发现新安全性问题。
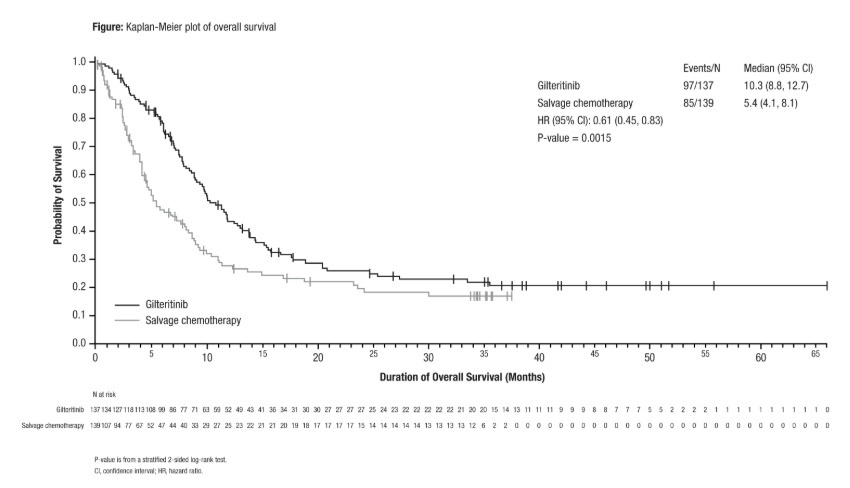
研究结论
中位随访超过3年的数据显示,在以亚洲人群为主的R/R FLT3mut+ AML患者中,吉瑞替尼较挽救化疗改善临床结局且耐受性良好,与主要分析结果一致,进一步支持其长期应用。
口头报告三
MDS的细胞和分子治疗靶向专场
摘要号:S170
英文标题:SINGLE-CELL ATLAS OF PEDIATRIC NRAS-MUTANT MYELOID NEOPLASMS REVEALS MYELOID LINEAGE BIAS AND IDENTIFIES POTENTIAL THERAPEUTIC TARGETS
中文标题:儿童NRAS突变髓系肿瘤的单细胞图谱揭示髓系谱系偏倚并识别潜在治疗靶点
汇报人:Suyu Zong(竺晓凡教授团队)
报告时间:6月12日17:00-17:15(当地时间)
报告地点:Brown Hall 2
研究背景
RAS基因突变在造血系统疾病中较为常见,包括幼年型粒单核细胞白血病(JMML)、骨髓增生异常综合征(MDS)以及儿童急性髓系白血病(AML)。然而,目前尚不清楚RAS基因突变导致不同疾病的机制,且临床上缺乏有效的RAS靶向治疗。
研究目的
通过单细胞RNA测序(scRNA-seq)技术阐明由NRAS基因突变驱动的JMML和MDS的发病机制,并确定儿童NRAS突变型髓系肿瘤中潜在的治疗靶点。
研究方法
我们对13份骨髓穿刺样本进行了scRNA-seq分析:其中4份来自健康捐献者,4份来自确诊时的JMML患者,5份来自新诊断的MDS患者。此外,我们通过将Mx1-Cre诱导性NrasG12D/+基因敲入小鼠与Cdkn2a+/-基因敲除小鼠杂交,构建了NRAS突变型髓系肿瘤的小鼠模型。分别在起始期、进展中期、终末期谱系阴性的骨髓细胞进行scRNA-seq分析,以追踪肿瘤的演变过程。通过整合人类和小鼠的数据,以识别关键基因和通路,并在体外和体内进行功能验证。
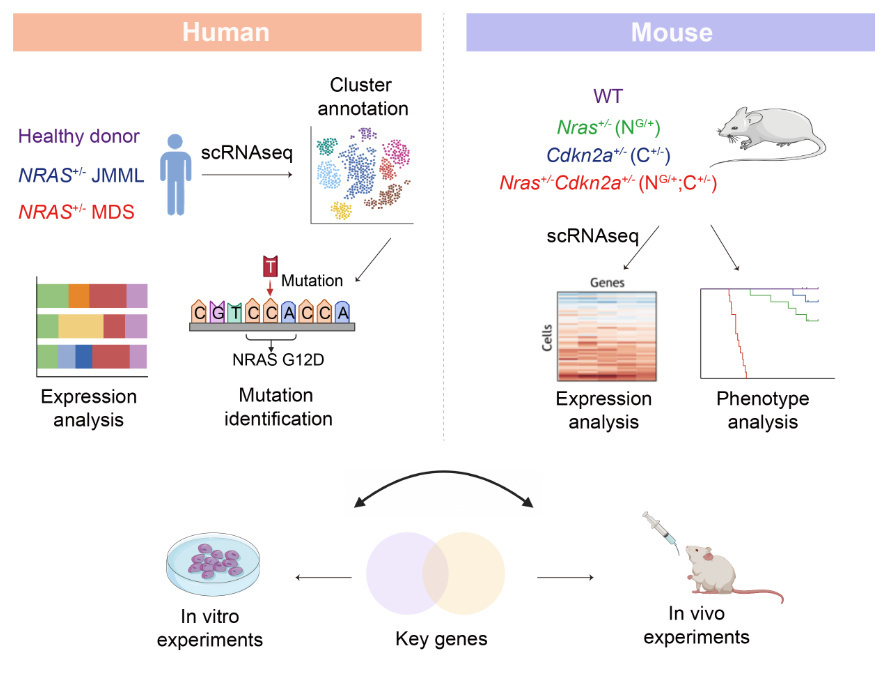
研究结果
我们的分析发现,MDS患者的造血干细胞(HSPCs)存在分化阻滞,其特征是在淋巴髓系祖细胞(LMprog)阶段停滞,而JMML患者和健康供体的HSPCs则显示出更广泛的分化能力。JMML患者的LMprog细胞在细胞周期和细胞激活通路中富集,而MDS患者的LMprog细胞则在髓系分化和NF-κB信号通路中富集,同时在淋巴分化和细胞衰老通路中出现耗竭。
我们成功建立了由NRAS突变驱动的髓系肿瘤小鼠模型。NrasG12D/+;Cdkn2a+/-小鼠与对照组小鼠相比,中位生存时间显著缩短,出现肝脾肿大,血红蛋白和血小板水平降低以及白细胞增多。骨髓和脾脏分析显示髓系细胞比例增加,并且存在广泛的髓系肿瘤细胞浸润。移植试验进一步证实,NrasG12D/+;Cdkn2a+/-细胞能够在受体动物中复制原发病的表型,并诱导致死性髓系肿瘤的发生。
在小鼠的三个阶段中进行的单细胞转录组分析显示,在NrasG12D/+;Cdkn2a+/-小鼠的终末期,未成熟髓系祖细胞(IMPs)显著增加。NrasG12D/+;Cdkn2a+/-小鼠的IMPs基因分析表明,细胞周期、造血和NF-κB信号通路的基因表达富集,而细胞衰老通路则出现耗竭。通过整合人类和小鼠的单细胞数据,我们识别了数个潜在的治疗靶点,包括FLT3、CDK6、SCD2、LCN2和RUNX1。随后,我们在NRAS突变型肿瘤细胞系以及体内模型中验证了这些靶点的功能作用。
研究结论
我们构建了首个携带NRAS突变的儿童JMML和MDS患者HSPC单细胞图谱。研究结果显示,与健康供体和JMML患者相比,MDS患者的HSPCs存在异常的髓系偏向性。通过整合人类和小鼠的数据并进行功能验证,我们确定了NRAS突变型造血系统恶性肿瘤潜在的治疗靶点。
口头报告四
干细胞移植——专场2
摘要号:S261
英文标题:AUTONOMOUS AI-DRIVEN INTENSIFIED PROPHYLAXIS OF SEVERE ACUTE GRAFT-VERSUS-HOST DISEASE IN HAPLOIDENTICAL TRANSPLANTS: A SINGLE-CENTRE, PROOF-OF-CONCEPT, PHASE 2 TRIAL
中文标题:自主人工智能驱动的单倍体移植中严重急性移植物抗宿主病的强化预防:一项单中心、概念验证、II期试验
汇报人:Yigeng Cao(姜尔烈教授团队)
报告时间:6月13日17:15-17:30(当地时间)
报告地点:Brown Hall 3
研究背景
自主人工智能(AI)的前瞻性试验相对较少,尤其是在肿瘤诊断后的治疗路径中。此外,将多模态患者精准变量直接整合到患者治疗中,对于成功实施自主人工智能至关重要。然而,鉴于某些地区医院信息系统(HIS)的分散性和复杂性,这一目标是否能够广泛实现目前尚不确定。对于半相合(Haplo)或人类白细胞抗原(HLA)不匹配的非亲缘供者(MMUD)来源的造血细胞移植而言,3-4级的严重急性移植物抗宿主病(aGVHD)依然是一个严重的风险因素。
研究目的
本研究旨在探讨使用 daGOAT 模型指导精准时机和剂量,剂量添加低剂量芦可替尼预防Haplo或MMUD移植中严重aGVHD的安全性和有效性。主要终点是前瞻性试验队列中移植后+100天(含)前严重aGVHD的总发生率。次要终点包括移植后+100天(含)前各器官aGVHD的发生率、100天无GVHD且无复发生存率(GRFS)以及180天总生存率。
研究方法
我们开展了一项概念验证研究,将之前开发的AI模型(daGOAT)整合到HIS中,并在单中心使用该模型对严重aGVHD的Haplo移植患者进行自主强化预防(NCT05600855)。daGOAT可自动监测141个常见临床协变量的动态数据,以预测即将发生的严重aGVHD。对于模型判定为高危受试者,建议预先使用低剂量芦可替尼。
研究结果
在59名被预测为即将发生严重aGVHD的受试者中,有52名(88%)对芦可替尼模型指定的给药时间和剂量的依从性良好。前瞻性试验队列中严重aGVHD的总发生率为6%(7/115),显著低于对照组(16% [46/280];P=0.008)。100天无GVHD且无复发生存率为92%(95%CI:87%-97%;HR=0.39),显著优于对照组(81% [95% CI:77%-86%];P=0.007)。daGOAT的应用并未导致与芦可替尼相关的不良事件发生率增加。对62名参与临床医生的调查显示,总体而言医生们对该模型的接受度较高,但许多人对监测芦可替尼安全性表示担忧。
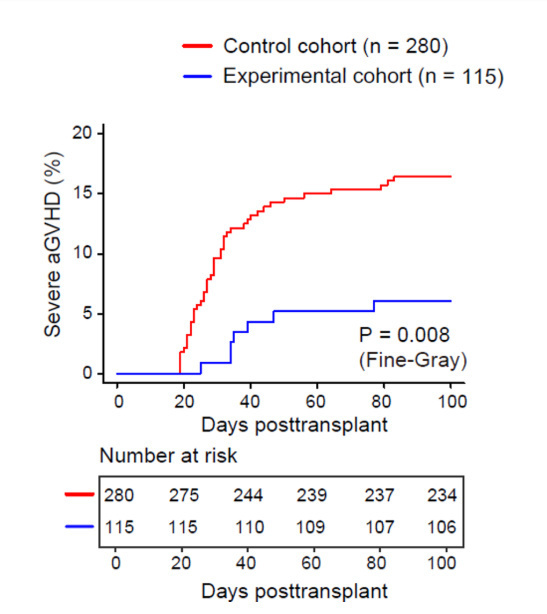
研究结论
综上所述,本研究结果表明,使用机器学习模型指导针对严重aGVHD的预防性干预的精准时机和剂量是可行的。