六月上海似锦,浦江潮涌映晖。2025年6月27日至29日,2025血液学转化和创新大会暨第十届上海淋巴细胞疾病学术研讨会在上海正式召开。淋巴瘤分类体系的构建始终是临床病理学领域最具挑战性的课题之一。随着分子生物学技术的突破性进展和国际学术合作的深化,淋巴瘤分类系统经历了从简单形态学观察到综合多学科特征分析的范式转变。会议期间,北京协和医院李剑教授以《朗格汉斯细胞组织细胞增多症共识解读》为题带来精彩讲座,为临床医师提供了极具价值的规范化诊疗思路。《肿瘤瞭望-血液时讯》现将核心内容整理成文,以飨读者。
朗格汉斯细胞组织细胞增多症(LCH)作为一种罕见的组织细胞肿瘤性疾病,自2018年被纳入国家卫生健康委员会发布的《第一批罕见病目录》以来,其临床诊疗日益受到重视。该病以组织细胞异常增生为特征,可累及骨骼、皮肤、肺、垂体等多个器官系统,临床表现高度异质,易导致误诊漏诊。北京协和医院数据显示,成人LCH患者中位年龄为32岁(范围18-79岁)。李剑教授以《中国成人朗格汉斯细胞组织细胞增生症诊疗专家共识(2025版)》为基,详细分享了LCH的病理特征、临床表现、诊断路径及治疗策略,旨在为临床医师提供规范化诊疗参考。
一、临床表现
LCH是一种可累及全年龄段以及全身多系统的异质性疾病。流行病学数据显示,LCH在儿童中相对多见(年发病率约5/百万),成人发病率约2/百万,男性略多于女性(男女比2:1)。
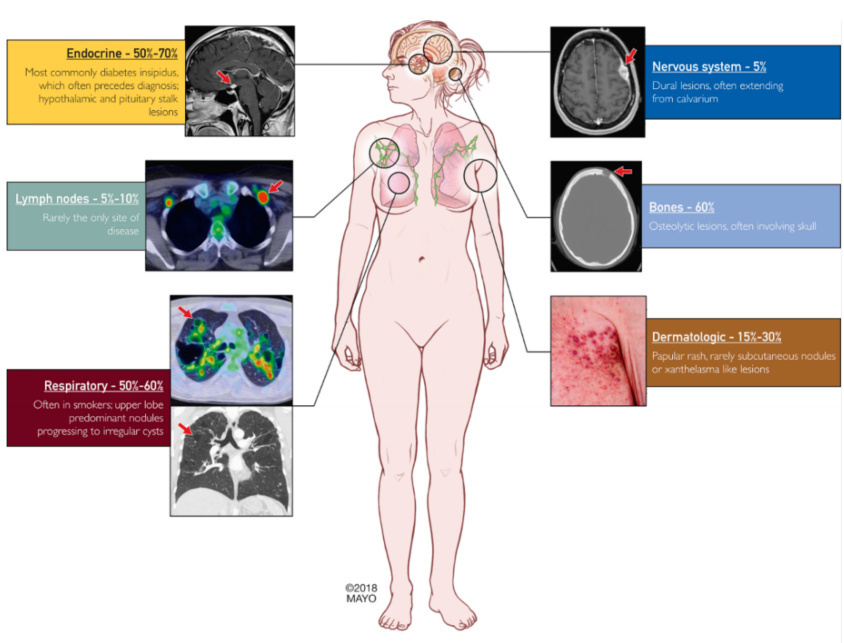
LCH临床表现多样化,容易诊和误诊。首发症状多样,以尿崩、骨痛、皮疹最为常见,B症状(发热、体重减轻)亦较为常见。主要受累器官包括骨骼、肺、垂体等。骨骼受累以溶骨性破坏为主要表现,颅骨、四肢长骨及骨盆为好发部位,可表现为单发或多发骨质缺损。肺部受累的典型影像学表现为双肺弥漫性薄壁囊样变及肺大泡、气胸,成人单纯肺受累较为常见。吸烟是LCH肺病的重要危险因素。皮肤病变呈现异质性皮疹,最常见的表现为糜烂及破溃,累及生殖器或肛周黏膜时容易被误诊为尖锐湿疣等疾病。
二、诊断路径
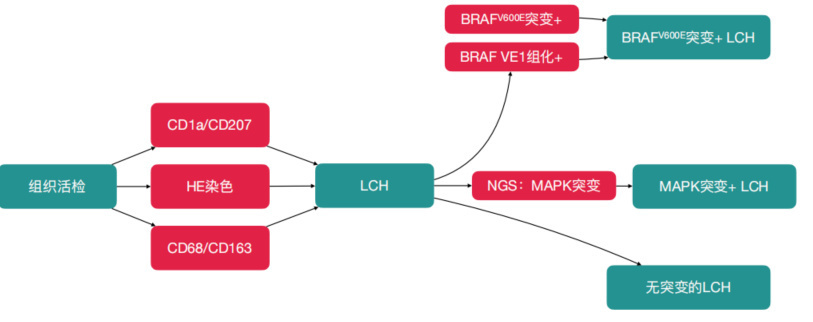
当患者同时出现≥2项关键症状(如气胸、皮疹、尿崩、溶骨性改变、骨痛、碱性磷酸酶升高、肝大)时需高度怀疑LCH。确诊主要依赖组织病理学检查,主要特点包括:1)大量炎症细胞背景中的朗格汉斯细胞浸润(8%,<1%~75%);2)LC的组化特征:CD68+/CD163+的组织细胞,同时还表达CD1a+和/或langerin(CD207)+ ;3)电镜: Birbeck颗粒+。
LCH是以丝裂原活化蛋白激酶(MAPK)信号通路激活为主要分子特征。在LCH中,约50%患者存在着BRAFV600E突变,其他包括MAP2K1基因突变、MAP3K基因突变等。
LCH的分类主要基于病变部位、受累部位的数量以及是否累及危险器官(肝脏、脾脏、骨髓或中枢受累)将LCH分为:①单系统单病灶(SS-s):仅有单一系统或单一病灶受累;②单系统多病灶(SS-m):单个器官或系统>1个病灶;③多系统(MS):指>2个器官或系统受累,可根据是否合并肝、脾、骨髓受累分为有危险脏器受累和无危险脏器受累。
骨骼受累推荐筛查PET-CT(头至足)或骨扫描;肺部建议行高分辨CT+肺功能(通气+弥散);垂体处进行增强MRI+垂体功能评价(抗利尿激素/生长激素/ACTH/TSH/LH/FSH);骨骼极少受累,可常规涂片+活检;不常规筛查肝脏,仅当碱性磷酸酶或胆红素升高时行MRCP/超声评估;
三、个体化治疗策略的制定

目前,成人LCH治疗面临多重困境,既缺乏标准化治疗方案,也鲜见前瞻性临床研究,多借鉴儿童LCH治疗经验,回顾性研究数据亦稀缺,且疗效评价无统一标准,增加了治疗效果评估难度。
LCH的治疗需根据疾病分型、器官受累程度及基因突变状态制定个体化方案。对于单系统单病灶型,以病变刮除、手术、放疗等局部治疗为主。患有孤立性肺LCH的成年吸烟患者需要严格戒烟。研究显示,中位随诊38m,单系统单病灶的3年无事件生存期(EFS)为63%;3年总生存率(OS)为97%。
单系统多病灶或多系统型需系统治疗,现有方案如下:
MA方案(甲氨蝶呤+阿糖胞苷)一线治疗疗MS或SS-m型LCH的II期前瞻性研究显示,客观缓解率(ORR)为88%,预计3年OS达98%。但需注意,该方案血液学毒性显著,3级肝脏毒性2%,需要进一步改进。
小剂量阿糖胞苷单药(LdAraC)一线治疗61例LCH(75.4%为MS型),ORR达93.4%,预计3年OS达100%,EFS达58.5%。
梅奥诊所开展的克拉曲滨单药治疗研究共纳入38例患者,其中初治患者29例,既往接受过治疗的患者9例,中位治疗疗程为4个(1 - 9个)。研究结果显示,ORR为79%,其中初治患者的ORR为 83%,5 年OS和EFS分别为75%和58%。
一项II期单中心、单臂前瞻性研究中,采用TCD方案(沙利度胺、环磷酰胺、地塞米松)治疗RR-LCH,共纳入32例患者,其中29例为MS型,所有患者既往均接受过基于AraC的治疗方案。中位随访时间为22个月,ORR达到87.5%,CRR为56.3%,PRR为31.3%,2年EFS为64%。
BRAF抑制剂:针对BRAFV600E突变阳性LCH患者,梅奥诊所开展了BRAF抑制剂单药治疗的回顾性研究,6例患者中初治4例,二线2例,接受维洛菲尼或达拉菲尼治疗。维洛菲尼组中,CR、PR、SD各1例;达拉菲尼组中,1例CR,2例PR。中位随访时间为 13 个月,2例患者死亡(1例死于肺炎,1例死于硬化性胆管炎)。在4例CNS-LCH患者中,2例PR,1例CR。此外,II 期VE-BASKET研究评估了维洛菲尼治疗BRAFV600E突变且既往经治患者,总ORR为61.5%,2 年OS和PFS率分别为96%和86%。
MEK抑制剂:考比替尼相关研究中纳入LCH、Erdheim-Chester病(ECD)、Rosai-Dorfman病(RDD)患者。基于PET疗效评价,总体ORR为89%,CR为72%,PR为17%。中位随访时间为 11.9 个月,15/18例患者存在各类 MAPK 通路突变。另一项研究中,芦沃美替尼在LCH、ECD等患者中,基于PET疗效评价,ORR为 82.8%,CR为72%,PR为17%,12个月PFS为74.4%。
BRAF抑制剂联合MEK抑制剂:病例报道显示,携带BRAFV600E突变的LCH患者,在长春碱联合泼尼松治疗失败后,给予达拉非尼150mg每日2次联合曲美替尼2 mg每日1次的治疗方案,FDG-PET/CT观察到患者病灶代谢程度较前减低。
四、疗效评价
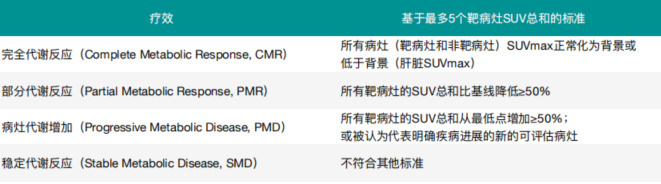
传统影像学(CT/MRI)对LCH疗效评估价值有限,尤其对肺部病变等病灶形态学改变及垂体功能改善等器官损害情况。目前,推荐采用PET应答评估标准(PRC)。靶病灶最多选择5个(每器官≤2个),要求SUVmax >1.5倍肝脏SUVmean(肝受累者>2倍纵隔血池SUVmean)。每个靶病灶的18F-FDG摄取值(SUV)计算方法为靶病灶SUVmax – 肝脏SUVmax,如果结果为负数,定义为0。
结 语
综上所述,LCH是一种由MAPK通路突变驱动的罕见组织细胞肿瘤,临床异质性强且易误诊。诊断需结合病理形态、免疫组化及分子检测,治疗策略应根据分型分层制定。随着靶向药物的发展,基于分子特征的精准治疗有望成为一线选择。疗效评价推荐采用PET-CT代谢标准以客观反映治疗反应。相信随着基础研究的深入及新型治疗手段的涌现,LCH的临床管理将迎来新的发展机遇。





专家简介

李剑 教授
北京协和医院
北京协和医院血液内科主任,主任医师,博士生导师
中华医学会血液学分会常委
北京医学会血液学分会副主任委员
北京医师协会血液科医师分会副会长
中华医学会血液学分会罕见病学组组长
中华血液学杂志编委