编者按:2025年中国临床肿瘤学会年度进展研讨会(BOC)暨Best of ASCO 2025 China(BOC/BOA)于7月4日至5日在南京盛大召开。此次会议汇聚了国内外肿瘤学领域的顶尖专家,共同回顾并探讨过去一年中国临床肿瘤学的重大进展,并分享刚刚落幕的美国临床肿瘤学会(ASCO)年会的前沿成果。在本次会议中,CSCO白血病专委会主任委员、中国医学科学院血液病医院(中国医学科学院血液学研究所)姜尔烈教授分享了两项急性髓系白血病(AML)领域的突破性研究,并在接受采访时进一步解读了这两项研究的重要意义与临床价值。
重磅研究一
地西他滨-西达尿苷(DEC-C)联合维奈克拉(VEN)全口服方案用于不适合强化诱导化疗的新诊断急性髓系白血病(AML)患者:来自101例患者的Ⅱ期队列研究结果(摘要号:6504)
背景:对于年龄≥75岁且不适合接受诱导化疗的AML患者,BCL-2抑制剂维奈克拉(VEN)联合阿扎胞苷(AZA)已获批准,该批准基于III期VIALE-A临床试验(完全缓解率[CR]为36.7%;中位CR持续时间为17.5个月;中位总生存期[OS]为14.7个月)。然而,患者需每月接受为期7天的阿扎胞苷静脉注射直到疾病进展,这给患者带来了较大负担。此外,多项校正后比较研究显示,阿扎胞苷与地西他滨的临床疗效相似。口服DEC-C(地西他滨35 mg,塞西达尿苷100 mg)的药代动力学(PK)曲线下面积与静脉注射地西他滨相当。本项Ⅰ/Ⅱ期临床试验旨在评估口服DEC-C联合维奈克拉治疗年龄≥75岁或因合并症无法接受一线强化诱导化疗的AML患者(NCT04657081)。本文报告了该试验Ⅱ期部分的结果。
方法:符合条件的患者在28天周期内接受口服DEC-C(1-5天)和维奈克拉400 mg/d治疗,第一周期维奈克拉剂量逐步增加(第1天100 mg,第2天200 g,第3天及之后400 g)。第一周期骨髓检查为可选,依据疗效和血细胞恢复情况调整维奈克拉和/或DEC-C的剂量。主要终点为完全缓解(CR)率,基于欧洲白血病网(ELN)2017年的疗效标准。
结果:截至2024年9月30日,共有101名患者入组并完成了中位4个周期(范围:1-15周期)治疗。患者中位年龄为78岁。根据ELN 2017年分类,预后良好、中等和不良的患者分别占31.7%、33.7%和29.7%。中位随访时间为11.2个月。CR率和CR/CR伴不完全血液学恢复率分别为46.5%(95%CI:36.5%–56.7%)和63.4%(95%CI:53.2%–72.7%)。中位CR达成时间为2.4个月。中位CR持续时间未达到;在达到CR的患者中,80.0%在6个月时保持CR,75.3%在12个月时保持CR。中位总生存期为15.5个月(95% CI:7.6–无法估算)。
98.0%的患者报告了≥3级的治疗相关不良事件,最常见的是发热性中性粒细胞减少症(49.5%)、贫血(38.6%)和中性粒细胞减少症(35.6%)。30天和60天死亡率分别为3.0%和9.9%。药代动力学数据显示口服DEC-C与维奈克拉之间不存在药物相互作用。
结论:对于不适合接受强化诱导化疗的初诊AML患者,DEC-C联合VEN的全口服方案与静脉注射阿扎胞苷联合维奈克拉方案的安全性、缓解率和生存率相当。这些数据支持DEC-C联合维奈克拉可作为该类患者的治疗选择。
专家解读
姜尔烈教授:该方案是目前首个用于急性髓系白血病(AML)患者,特别是老年AML患者的全口服治疗方案。
根据目前Ⅱ期研究结果,该方案的血液学缓解率接近50%,而整体缓解率则更高,接近70%。研究中入组的患者均为老年人,且中位年龄超过70岁。疗效方面,研究显示该方案能够实现显著的缓解,并且在生存期方面也表现出显著的临床获益,患者的中位总生存期达到15个月以上。
在安全性方面,患者的主要不良反应为血液学毒性,三级及以上的血小板减少和中性粒细胞减少的发生率约为20%,这一数据表明,从安全性角度来看,该治疗方案具有较好的耐受性。
重磅研究二
Ziftomenib治疗复发/难治性(R/R)NPM1突变急性髓系白血病(AML):来自关键性KOMET-001研究的Ⅰb/Ⅱ期临床活性与安全性结果(摘要号:6506)
背景:NPM1突变(NPM1-m)约占急性髓系白血病(AML)患者的30%。尽管目前已有风险分层方法,但近一半的患者会在一年内发展为复发/难治性(R/R)疾病,且此时化疗后的完全缓解(CR)率不足10%。Ziftomenib是一种强效、高选择性、口服、在研的Menin抑制剂,在单药治疗和联合治疗中对成人R/R NPM1突变和KMT2A重排AML患者表现出临床活性,600 mg/d作为NPM1突变单药治疗的Ⅱ期推荐剂量。本文展示了在关键性KOMET-001研究中,接受Ziftomenib单药治疗的NPM1突变患者的初步分析结果。
方法:KOMET-001(NCT04067336)是一项多中心、开放标签的Ⅰ期/Ⅱ期研究,评估Ziftomenib在成人R/R AML患者中的疗效。在Ⅱ期中,NPM1突变的R/R AML患者接受Ziftomenib 600 mg 每日一次治疗。Ⅱ期的主要终点为完全缓解伴完全/部分血液学恢复(CR/CRh);关键次要终点为复合完全缓解(CRc)、CR/CRh和CRc的持续时间以及安全性。以下分析包括来自Ⅰb/Ⅱ期的NPM1突变患者数据。
结果:Ⅱ期的主要终点已达成(P=0.0058)。截至2024年12月20日,Ⅰb/Ⅱ期研究共入组112名患者(51%来自美国/加拿大,49%来自欧洲/英国),并接受Ziftomenib 600 mg每日一次治疗,中位随访时间为4.2个月。患者中位年龄为69岁(范围:22–86岁),56%为女性,83%为ECOG表现状态评分0–1,既往治疗中位数为2次(范围:1–7),其中60%的患者既往接受过维奈克拉(VEN)治疗,23%的患者既往接受过移植治疗。在所有Ⅰb/Ⅱ期患者中,CR/CRh率为25%(28/112;95% CI:17-34),总缓解率为35%(39/112;95%CI:26-44)。在Ⅱ期研究中,23%(21/92;95% CI:15-33)患者达到了CR/CRh。在接受检测的CR/CRh应答患者中,67% (10/15) 的微小残留病 (MRD) 阴性。无论是否接受过VEN治疗,CR/CRh率均较为相似(VEN初治组21% vs. VEN暴露组24%)。Ziftomenib耐受性良好,3%(3/112)患者因治疗相关不良事件(TRAEs)中断治疗。40%(45/112)患者出现≥3级TRAEs,常见的不良事件包括13%的分化综合征(均为3级),贫血、发热性中性粒细胞减少症和血小板减少症各≤5%,以及2%的QTc延长(3级)。将呈现更新的临床活性和安全性数据。
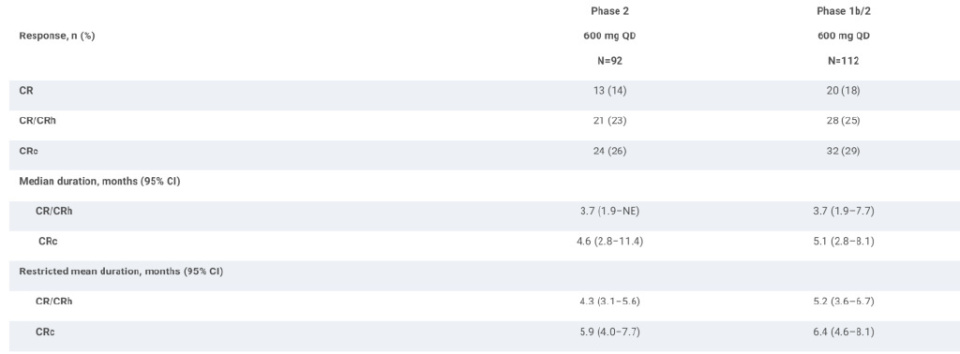
结论:在关键性KOMET-001研究中,Ⅱ期的主要终点已达成:Ziftomenib在R/R NPM1突变AML患者中取得了深度且持久的疗效,无论是否曾接受过VEN治疗。Ziftomenib耐受性良好,造血抑制有限,且仅有3%的患者因Ziftomenib相关不良事件中断治疗。综合这些数据,支持Ziftomenib单药治疗作为R/R NPM1突变AML患者的新治疗选择的潜力。
专家解读
姜尔烈教授:该研究讨论了Menin抑制剂的单药治疗,其CR率也表现出较好的效果,超过了20%,接近30%。目前,该药物正计划开展Ⅲ期临床研究,探索其与维奈克拉、阿扎胞苷的联合应用,或与经典的3+7方案联合使用。这项Ⅲ研究尤其是Menin抑制剂与维奈克拉或阿扎胞苷的联合应用有很大潜力。通过三药联合,预计可以进一步提高缓解率。
今天的讨论主要集中在难治复发患者的治疗,但后续临床研究主要针对初治患者。预计在这一群体中,Menin抑制剂联合其他药物的治疗方案将取得更高的缓解率。目前其他分子靶向药物,如FLT3 抑制剂、IDH抑制剂、RAS抑制剂和Menin抑制剂等,联合低强度化疗在未来可能成为一种替代传统化疗的策略。这些药物的联合使用不仅可能提高一线治疗的缓解率,还能降低诱导治疗相关的死亡率,改善患者的安全性。
因此,小分子靶向药物与非细胞毒药物的联合应用,已然成为当前研究的热点领域。未来,这类联合方案有望发展为可替代传统细胞毒治疗的安全有效方案,为AML的治疗带来新的变革。
专家简介

姜尔烈 教授
中国医学科学院血液病医院(中国医学科学院血液学研究所)干细胞移植中心主任
医学博士、主任医师、博士生(后)导师
中国初级卫生保健基金会造血干细胞移植专委会主任委员
CSCO白血病专委会主任委员
中国血液病专科联盟白血病自体移植协作组组长
中华医学会血液学分会造血干细胞应用学组副组长
中国抗癌协会血液肿瘤专业委员会常务委员,造血干细胞移植与细胞治疗学组副组长
CSCO自体造血干细胞移植工作组副组长
天津市抗癌协会常务理事
天津市血液与再生医学学会副理事长
《中华血液学杂志》、《白血病·淋巴瘤》等杂志编委