六月上海花似锦,浦江潮涌映朝晖。2025年6月27日至29日,2025血液学转化和创新大会暨第十届上海淋巴细胞疾病学术研讨会在上海正式召开。本次大会特邀国内外知名专家学者分享学术成果,旨在推动血液领域基础科学与临床成果转化的发展,围绕新疗法、专业培训以及科学普及等方面展开广泛交流与合作。会议期间,浙江大学医学院附属第二医院钱文斌教授以《CAR-NK细胞疗法治疗淋巴瘤新进展及新一代CAR-NK疗法》为题,分享了CAR-NK细胞疗法的最新突破性进展,为这一新兴免疫治疗手段的临床应用提供了重要理论依据与实践指导。《肿瘤瞭望-血液时讯》特整理成文,以飨读者。

近年来,嵌合抗原受体自然杀伤(CAR-NK)细胞疗法作为一种新兴的免疫治疗手段,在淋巴瘤治疗领域展现出显著的应用潜力。钱文斌教授全面综述了CAR-NK细胞疗法在淋巴瘤治疗中的最新研究进展,包括其临床研究现状、创新疗法、转化研究以及耐药机制的研究,以期为该领域的进一步发展提供参考。
一、CAR-NK细胞疗法研究现状
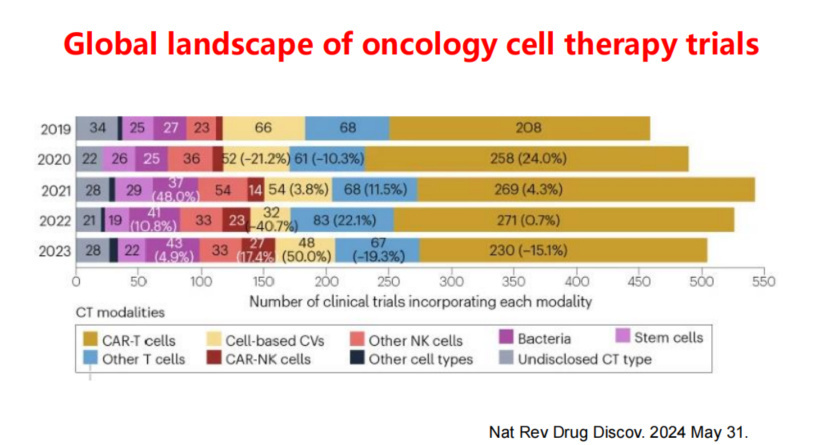
CAR-NK细胞疗法作为一种新兴的免疫治疗方法,其临床试验数量呈现逐年增长的趋势。据统计,全球范围内CAR-NK细胞疗法的临床试验数量从2017年的1项增长至2024年的108项,涵盖了多种血液系统恶性肿瘤和实体肿瘤。在血液系统恶性肿瘤中,CD19、BCMA、NKG2D等靶点的研究较为集中,而在实体肿瘤中,TROP2、GPC3、5T4等靶点也逐渐成为研究热点。
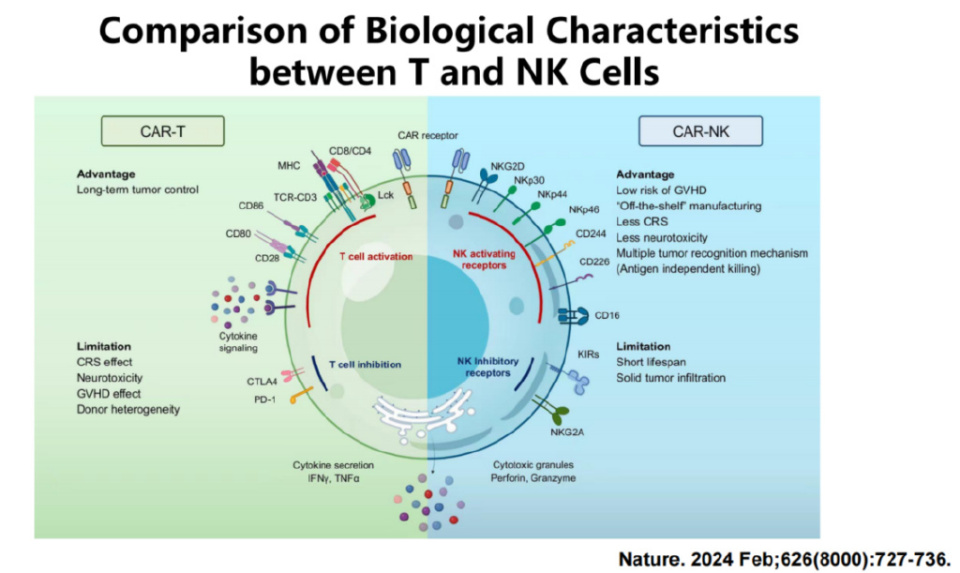
与CAR-T细胞疗法相比,CAR-NK细胞疗法具有独特的优势。首先,其引发移植物抗宿主病(GVHD)的风险较低,这提高了治疗的安全性。其次,CAR-NK细胞疗法支持“现货(off-the-shelf)”生产,即可以预先制备并储存。此外,其引发的细胞因子释放综合征(CRS)和神经毒性反应较少,进一步降低了治疗的风险。最后,CAR-NK细胞具有多重肿瘤识别机制,包括抗原非依赖性杀伤,有助于更广泛地识别和杀伤肿瘤细胞。钱文斌教授团队研究发现,CAR-NK还具备克服抗原逃逸的潜力。然而,CAR-NK细胞疗法也存在一些局限性,如CAR-NK细胞在体内的寿命相对较短,且对实体瘤的浸润性较差。
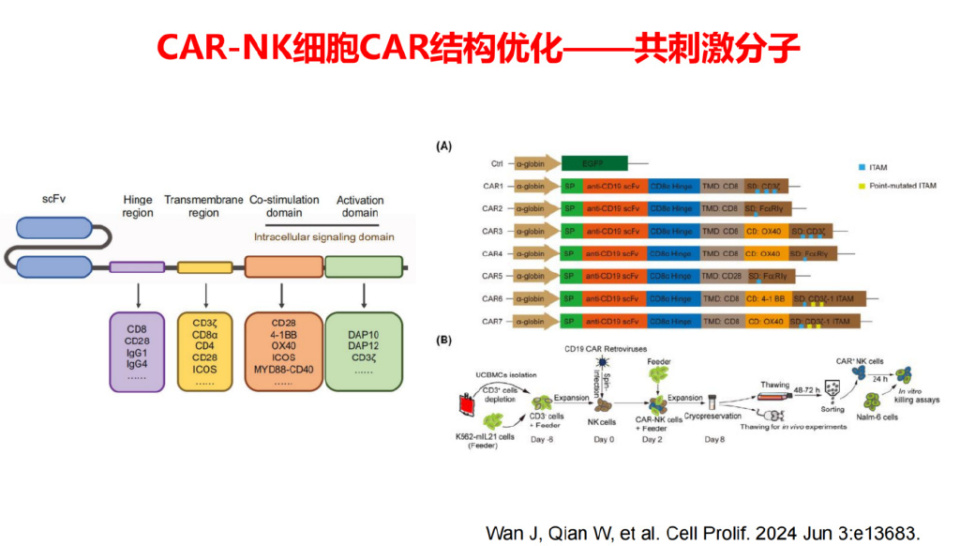
CAR-NK的CAR通常由胞外结构域、跨膜结构域以及胞内激活结构域组成,其中,胞外结构域包括信号肽、识别抗原的单链抗体片段(scFv)和铰链区,连同调控元件将决定CAR的功效。第一代CAR分子包含一个合成的细胞外受体、一个跨膜域和一个细胞内信号域;第二、三代的CAR分子分别具有一个或多个细胞内共刺激结构域。通过对各个结构域的优化,CAR-NK的CAR分子目前已经发展至第四代,通过引入不同的共刺激分子和细胞因子修饰,显著提高了其抗肿瘤活性和体内持久性。
我国一项研究中设计了七种CD19 CAR构建体,并使用逆转录病毒系统在NK细胞中表达,评估了它们的抗肿瘤效果和持久性。结果显示,所有构建体均增强了NK细胞的抗肿瘤能力,并延长了荷瘤小鼠的生存期。特别是,CAR1(CD8 TMD-CD3ζ SD)-NK细胞在治疗荷瘤动物方面表现出卓越的疗效,并且在与OX40共刺激结构域结合时展现出增强的持久性。
二、CAR-NK细胞疗法治疗淋巴瘤临床研究进展
近年来,CAR-NK细胞疗法在治疗淋巴瘤的临床研究中取得了令人鼓舞的成果。首个基于脐血来源的CD19 CAR-NK细胞疗法的临床试验结果显示,在接受治疗的11名患者中,4名淋巴瘤患者和3名CLL患者获得了完全缓解,其中弥漫大B细胞淋巴瘤(DLBCL)患者中持续CR达13个月。所有剂量水平下,反应均迅速出现,且在输注后30天内即可观察到。输注的CAR-NK细胞在体内进行了扩增,并在至少12个月内以低水平持续存在。
美国德克萨斯大学MD安德森癌症中心报告了一项I/II期临床试验,37名复发性或难治性B细胞恶性肿瘤患者接受了靶向CD19的脐血来源的CD19 CAR-NK细胞治疗取得了良好结果。在第30天和100天时,接受治疗的患者的总缓解率(ORR)均为48.6%,一年无进展生存率为32%、总生存率为68%。对不同类型的B细胞恶性肿瘤均展现获益:低级别非霍奇金淋巴瘤30天后的ORR为100%,未转化的CLL的ORR为67%,DLBCL患者的ORR为41%。
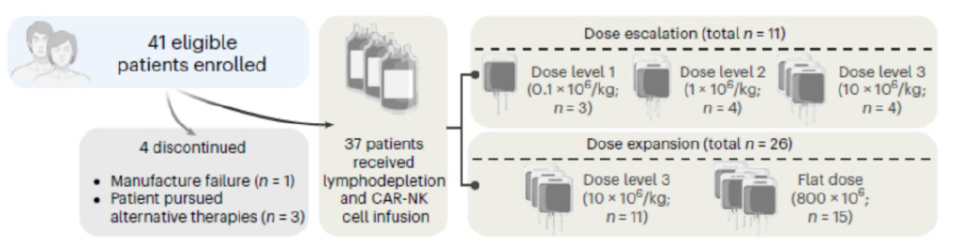
2024年ASH上,现货型、同种异体、脐带血来源的、CD19 CAR-NK细胞产品TAK-007研究显示,26例LBCL/iNHL患者接受了TAK-007治疗,其中半数为门诊治疗。既往全身治疗中位线数为5(范围:2-11),其中8例LBCL和1例iNHL患者接受过抗CD19 CAR-T治疗。从入组到接受淋巴细胞清除化疗的中位时间为8天。总体ORR为53.8%。接受800M TAK-007治疗的23例患者中有14例(61%)发生缓解。在9例iNHL患者中,ORR为77.8%,CR率为55.6%,iNHL患者的中位缓解持续时间为4.9个月。LBCL的CR21.4%,中位缓解持续时间为2.6个月。在术前活检的一系列CD19抗原密度中均观察到临床缓解,即克服抗原逃逸。在TAK-007给药后的10天内,有3例患者出现了CRS(2例为1级;1例为2级)。在TAK-007给药后的60天内未出现ICANS。未观察到显著的促炎细胞因子水平升高。
FT596是一种诱导多能干细胞(iPSC)来源的CAR-NK细胞疗法,具有三种抗肿瘤方式:CD19 CAR;高亲和力、不可切割的CD16 Fc受体;IL-15-IL-15受体融合。华盛顿大学Armin Ghobadi教授于柳叶刀发表了一项首次人体I期研究,评估了FT596作为单药治疗和联合利妥昔单抗治疗复发或难治性B细胞淋巴瘤的安全性和耐受性。研究报告了FT596令人鼓舞的初步疗效,特别是在滤泡性淋巴瘤患者中,ORR达到了100%,其中85%的患者达到CR。在大B细胞淋巴瘤患者中,ORR为38%,CRR为25%。此外,FT596在先前接受过CAR-T细胞治疗的患者中取得了30% CRR的疗效。研究还发现输注后NK细胞水平迅速达到峰值,并可持续长达15天。
三、创新CAR-NK疗法治疗DLBCL
在创新CAR-NK疗法方面,多项临床前研究和早期临床试验展示了基于改造的慢病毒载体CAR-NK细胞疗法的有效性和安全性,以及其在治疗DLBCL中的潜力。例如,通过使用狒狒包膜假型慢病毒载体(BaEV-LV)转导脐带血来源的NK细胞,构建具有4-1BB和CD3ζ信号内结构域,以及共表达白细胞介素-15(IL-15)以促进细胞扩增与存活的CD19特异性CAR-NK细胞(CD19-BBz CAR-NK),为淋巴瘤治疗领域提供了"通用型"策略。
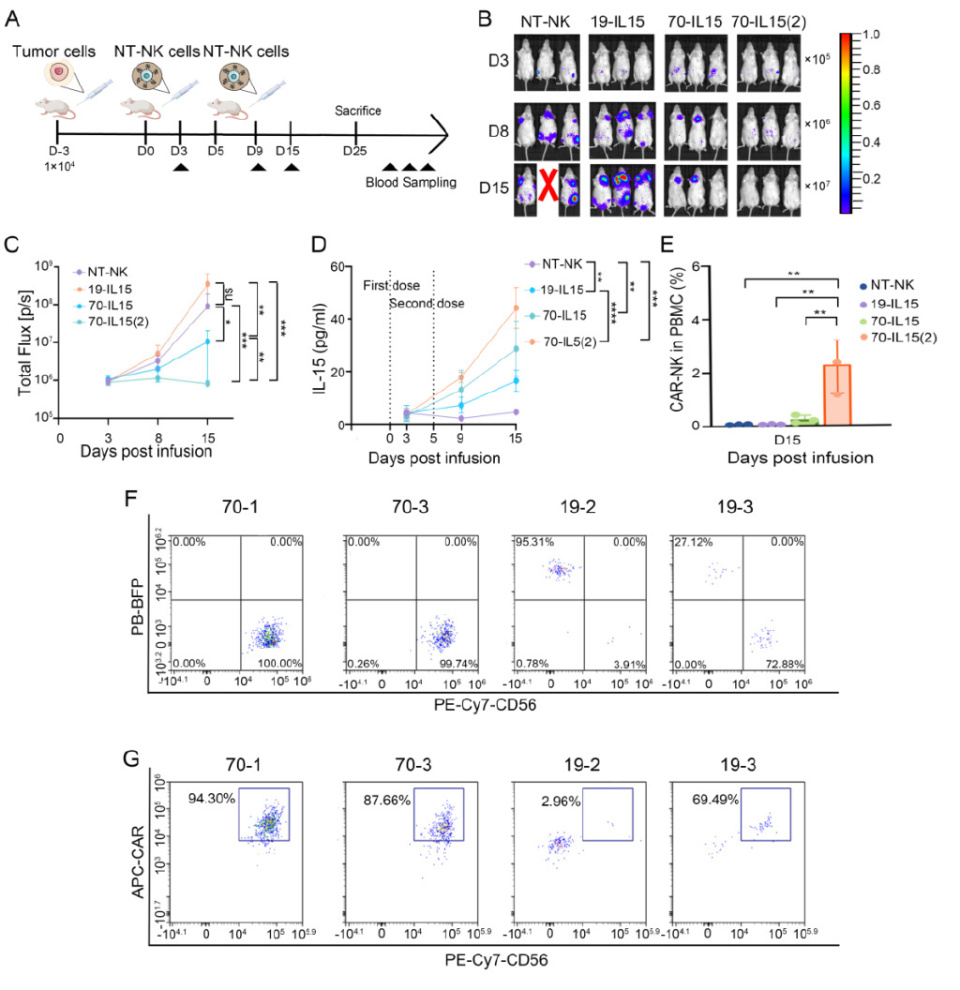
此外,靶向CD70、CD19及CD70/CD19双靶点CAR-NK是具有潜在临床应用价值的、新型CAR-T疗法。钱文斌教授团队尝试将回输方案改成2次回输(D3、D8各10:1),结果显示携带IL15的CD70 CAR-NK取得了令人惊喜的疗效,为CAR-NK输注方式的重塑提供了依据。
四、脐血来源CD19 CAR-NK疗法治DLBCL的转化研究
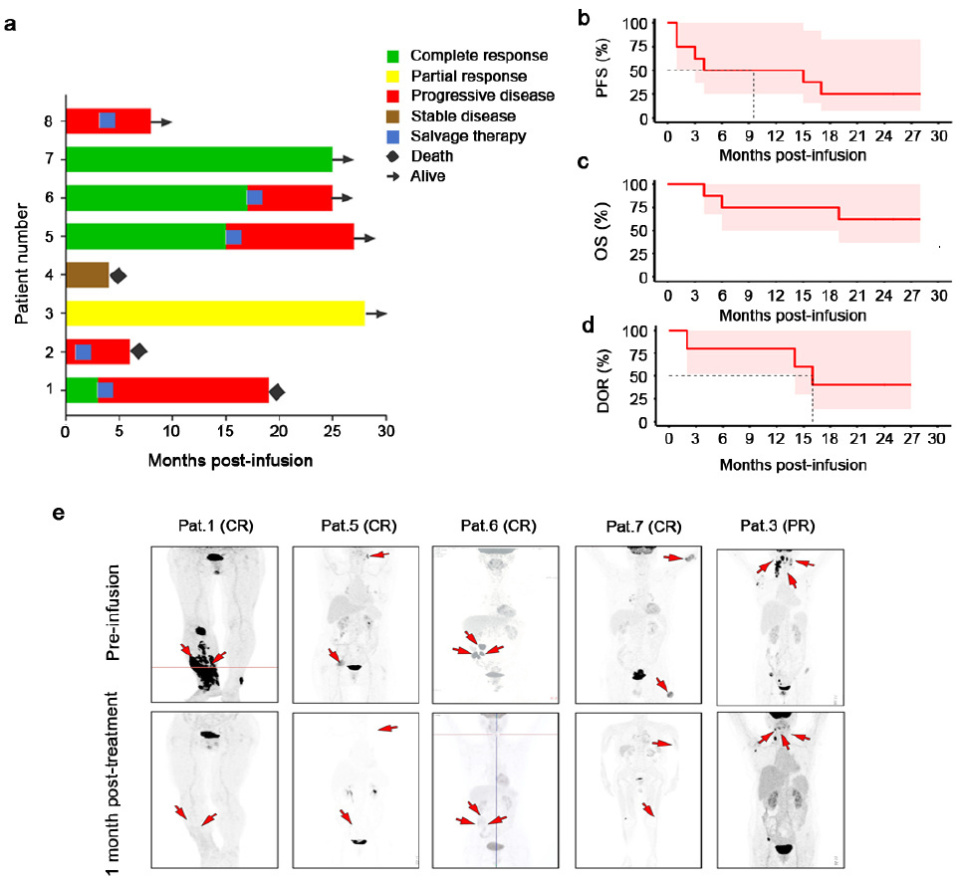
一项I期剂量递增试验(NCT05472558),对8例复发/难治性大B细胞淋巴瘤患者进行CAR-NK细胞的重复输注治疗,达到了预设终点,主要终点包括安全性、最大耐受剂量和总缓解率,次要终点涵盖缓解持续时间、总生存期和无进展生存期。试验期间未发生剂量限制性毒性,亦未达到最大耐受剂量。未观察到细胞因子释放综合征、神经毒性或移植物抗宿主病病例。
结果显示,第30天的ORR为62.5%,其中4例(50%)患者达到完全缓解。中位无进展生存期为9.5个月,中位总生存期尚未达到。事后探索性单细胞RNA测序分析揭示了与CAR-NK细胞疗效相关的分子特征,以及疗效关联性免疫细胞相互作用网络。
五、CAR-NK细胞疗法治疗淋巴瘤耐药机制研究
尽管CAR-NK细胞疗法在治疗淋巴瘤中展现出良好的疗效,但部分患者仍会出现耐药现象。研究发现,CAR-NK细胞产品的异质性可能是影响疗效的重要因素。通过对CAR-NK细胞产品的亚群分析,发现不同亚群的细胞在功能和基因表达谱上存在差异。例如,NK0亚群是PD的特征性亚群,而NK4亚群为高NFkB/低MHC-II。这些亚群的特征分析有助于预测治疗疗效,并为个体化治疗提供依据。此外,患者的外周血免疫细胞变化也与治疗疗效密切相关。在CR患者中,外周血中的抗原呈递相关细胞和细胞毒性细胞显著增加,而疾病进展(PD)患者CD4+ T细胞呈现免疫抑制表型。CR患者NK细胞与单核细胞间的抗原呈递信号传导强度显著高于PD患者。
最新研究还首次揭示了转录因子环磷酸腺苷反应元件调节因子(CREM)是NK细胞效应功能的核心调控枢纽,发现在过继转移CAR-NK细胞发挥最佳抗肿瘤效应的肿瘤模型中,CREM表达呈现显著诱导特征,且CREM缺失可显著增强CAR-NK细胞在体内外的细胞毒活性及细胞因子分泌能力,并在肿瘤再攻击模型中表现出更强的抗耗竭能力,为通过靶向CREM信号通路优化NK细胞疗法疗效提供了重要理论依据。
这些发现表明,为提升NK细胞疗法疗效并突破耐药瓶颈,未来策略可聚焦于构建高效体外扩增体系以实现规模化制备,通过工程化改造诱导记忆样NK表型以增强其持久抗肿瘤活性,采用多靶点CAR设计或联合疗法克服肿瘤抗原异质性,并开发靶向肿瘤微环境调控策略以综合提升治疗效果。
结 语
CAR-NK细胞疗法作为一种新兴的免疫治疗方法,在多种治疗领域展现出巨大的临床应用潜力。近年来,通过不断优化CAR结构、引入共刺激分子和细胞因子修饰,以及探索新的治疗策略,CAR-NK细胞疗法的疗效和安全性得到了显著提高。未来,随着基础研究的深入和临床试验的开展,CAR-NK细胞疗法有望为越来越多的患者提供更加有效和安全的治疗选择。
专家简介

钱文斌 教授
浙江大学医学院附属第二医院
浙江大学医学院附属第二医院血液内科 主任
浙江大学医学院附属第二医院生物治疗中心 主任
科技创新2030国家重大项目 首席科学家
中国医师协会血液科医师分会 委员
中国抗癌协会肿瘤血液病学/血液肿瘤专业委员会 常委
中国抗癌协会淋巴瘤专业委员会 委员
中国老年保健协会淋巴瘤专业委员会 副主任委员
中华血液学会 淋巴细胞疾病学组、感染学组 委员
浙江省医学会血液学分会 主任委员
以第一/通讯作者在Cell Discovery, eClinical Medicine, Clin Cancer Res, Leukemia (2), Haematologica, Blood Cancer Journal, Cancer Communication, J Hematol & Oncol (2), Signal Transduction and Target Therapy, Cell Mol Immunol和Lancet Hematology等国际知名刊物发表论文90余篇
【CAR T细胞治疗NHL毒副作用临床管理指导原则】、【CAR-T细胞治疗淋巴瘤MDT全程管理专家共识】共同主编,清华大学出版社,2021年【CAR-T细胞免疫治疗学】人民卫生出版社,2021年;【肿瘤生物细胞治疗病例精解】上海科学技术文献出版社,2024年,副主编主持国家自然基金重点项目、原创探索项目和面上项目7项和浙江省重点研发计划等作为负责人或主要成员获得国家科技进步二等奖2项、省科技进步一、二等奖近10项