当2025年国际恶性淋巴瘤会议(ICML)的学术帷幕缓缓落下,Martin Dreyling教授为全球学者勾勒出弥漫大B细胞淋巴瘤(DLBCL)领域的最新演进图谱。在闭幕式中,他特别强调:卢加诺会议已超越传统学术平台的范畴,成为凝聚全球共识的"通用语言",推动着从基础分子机制到临床诊疗策略的全链条革新。本文将深度聚焦DLBCL这一会议核心议题,以三重维度呈现:从百年病理分类的历史沿革到分子分型的精准迭代,从肿瘤微环境的免疫调控机制到靶向治疗的临床转化突破。Martin Dreyling教授的系统性总结不仅揭示了"化疗时代落幕" 的科学依据,更通过卢加诺精神的框架,为DLBCL诊疗指明了"分子分型 + 微环境调控 + 免疫联合"的三维发展路径。

01
三重L框架下的学术共识构建
ICML始终以“三重L”为核心定位——即卢加诺(Lugano)作为淋巴瘤(Lymphoma)领域通用语言(Lingua Franca)的学术交流平台。本届会议延续了轻松而富有成效的讨论氛围,与会者围绕弥漫大B细胞淋巴瘤(DLBCL)的分子分型、免疫微环境调控及靶向治疗进展展开深度研讨。会议特别强调,跨学科协作与标准化分类体系是推动领域发展的基石,成功汇聚了全球学者对淋巴瘤精准诊疗的探索成果。
从学术传承角度看,卢加诺会议的独特价值在于融合了基础研究与临床实践。正如Dreyling教授所提及的,会议不仅是科研成果的展示场,更是“桥梁建造者”的孵化器——从美国学者John Altman的历史贡献,到Emanuele Zucca创立国际淋巴瘤研究组(IELSG)的实践,均体现了学术共同体对标准化研究体系的长期投入。这种传承性在DLBCL的分类演进中尤为显著。
02
淋巴瘤分类体系的演进与未来统一路径
01
病理分类的迭代:从显微镜观察到分子分型
Dreyling教授开篇回顾了淋巴瘤分类体系发展的艰辛历程,强调了建立“共同语言”对于领域进步的基础性作用。
淋巴瘤分类体系的发展历经百年探索。20世纪60年代,Lennert与Feller通过显微镜形态学观察,首次实现淋巴瘤亚型的病理识别,为后续分类奠定了形态学基础。然而,早期分类面临“各学派标准不一”的困境,直至“工作分型(Working Formulation)”的提出,才通过简化细胞形态与大小特征,初步建立了全球通用的沟通语言。
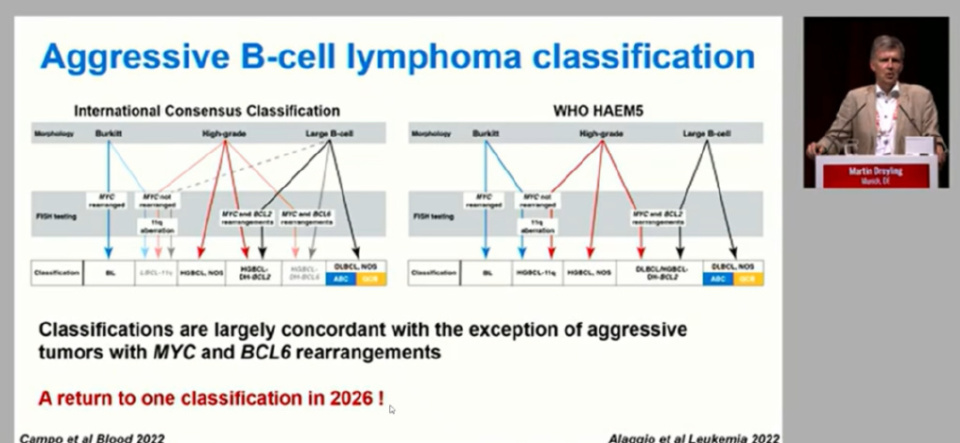
随后,通过将临床诊疗需求纳入分类体系,病理学家与临床医生的协作推动了分类从“形态描述”向“治疗指导”的功能转型。随后进一步聚焦分类标准化问题,Dreyling教授坦言,近期出现的WHO与ICC两种分类体系并存虽在核心内容上相近,但命名差异造成了实践困扰。他欣慰地指出,依托卢加诺会议特有的协作精神,各方已达成共识计划,将于明年重聚并致力于在第六版WHO分类中实现再次统一,这将是领域的一项重大成就。
02
分子时代的分类挑战:从细胞起源到遗传集群
DLBCL的分子分型研究始于“细胞起源(Cell of Origin)”理论,该理论通过基因表达谱将DLBCL分为生发中心B细胞样(GCB)与活化B细胞样(ABC)亚型,为预后判断提供了分子依据。然而,单纯基于细胞起源的分类在临床应用中遭遇瓶颈——如靶向治疗尝试仅聚焦单一通路(如Polatuzumab针对CD79b)时,未能显著改善患者预后。Dreyling教授明确指出,深入理解DLBCL的分子异质性,是实现更可靠诊断、精准预后判断及个体化靶向治疗的关键。
未来,对分子分型体系的核心要求在于:
提升诊断可靠性: 准确区分不同淋巴瘤实体,确保研究对象的一致性。
高覆盖率: 应能覆盖绝大多数病例(而非仅10%),方具临床实用价值。
临床可操作性: 解决在常规临床实践中应用的可行性挑战(即“实用性挑战”)。
目前,多个研究联盟(如 LymphGen, DLBCLclass)基于基因表达谱和遗传变异开发了不同的分子分型方案(通常识别5~7个亚型),它们均具有坚实的科学基础。这些方案超越了传统的“细胞起源”概念,提供了更精细的疾病认知。例如,ABC型可进一步细分为多个具有独特分子特征的亚群(如MCD, N1)。教授强调,不同方案间的差异源于其设计目标(如追求全覆盖 vs. 追求高分类置信度)和所采用的技术/算法视角不同,这类似于从不同角度观察山脉会得到不同景观。
因此,当前尚无“终极”分类方案,分子分型体系仍需持续演进和完善。表观遗传调控在决定恶性细胞分化状态和干细胞特性中的作用,是理解DLBCL生物学和潜在治疗靶点的重要前沿。

03
肿瘤微环境:免疫治疗疗效的关键决定因素
肿瘤微环境(TME)在DLBCL,尤其是在免疫治疗时代具有关键作用。早期滤泡淋巴瘤基因表达谱分析受TME影响的经验教训,反向凸显了综合评估恶性细胞与其微环境的重要性。研究显示,DLBCL中存在不同的TME模式,至少可分为三类:

正常淋巴结模式: 富含功能正常的免疫细胞。
T细胞耗竭模式: 虽有大量免疫细胞浸润,但功能受损。
“冷肿瘤”模式: 以间质细胞为主,缺乏有效T细胞浸润。
这些模式对治疗反应,特别是免疫治疗(如CAR-T细胞疗法、双特异性抗体)的疗效具有显著预测价值。数据显示,具有“正常”TME模式的患者对CAR-T细胞治疗的反应率和生存获益显著更优,提示其微环境更有利于免疫效应细胞的激活和功能发挥。双特异性抗体的疗效同样观察到与TME状态的相关性。理解TME分型是优化免疫治疗策略、筛选潜在获益人群的必经之路。
04
靶向治疗崛起:从实验室到临床实践的变革
分子分型与TME研究的深化正迅速转化为治疗模式的实质性变革。Dreyling教授重点阐述了以下关键进展。
01
分子分型指导靶向治疗的探索
POLARIX试验显示,特定分子亚型患者更能从Pola-R-CHP方案中获益。同样,明确识别MCD/N1等亚型的患者,在R-CHOP基础上联合BTK抑制剂显示出显著改善的预后。
中国研究者基于现有可及靶向药物(BTKi、来那度胺、去甲基化药物等),结合简化分子模型设计了GUIDANCE-1研究方案,其初步结果令人鼓舞,尽管样本量较小,但为假设驱动研究提供了范例。更大规模的GUIDANCE-2研究正在进行,其结果有望为分子分型指导下的个体化治疗提供更强有力的证据。这标志着DLBCL分子分型指导治疗已进入“黄金时期”。
02
一线治疗的探索与展望
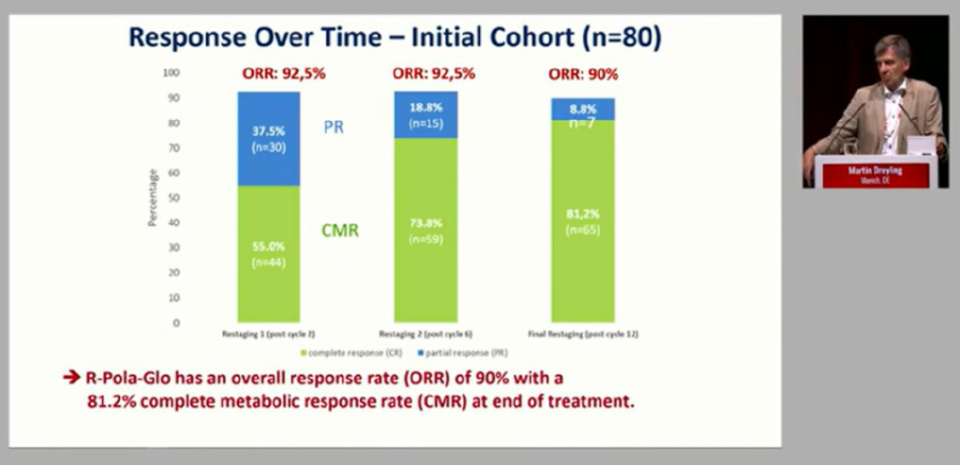
作为一线治疗近50年的金标准,R-CHOP的局限性日益显现。研究显示,R-Pola-Glo的ORR达到90%,在治疗结束时的CMR为81.2%,结果令人振奋,提示此类组合有潜力挑战一线标准治疗。
Dreyling教授预言,未来5年DLBCL一线治疗将逐步淘汰单纯化疗。未来,领域重点很可能在于R-CHOP的改良或替代方案,包括联合双特异性抗体、采用升级版抗体药物、整合靶向化疗等策略。以双特异性抗体和靶向化疗为代表的新型药物,结合传统免疫化疗,正塑造DLBCL治疗的新范式。
03
复发/难治性DLBCL:化疗核心地位的终结
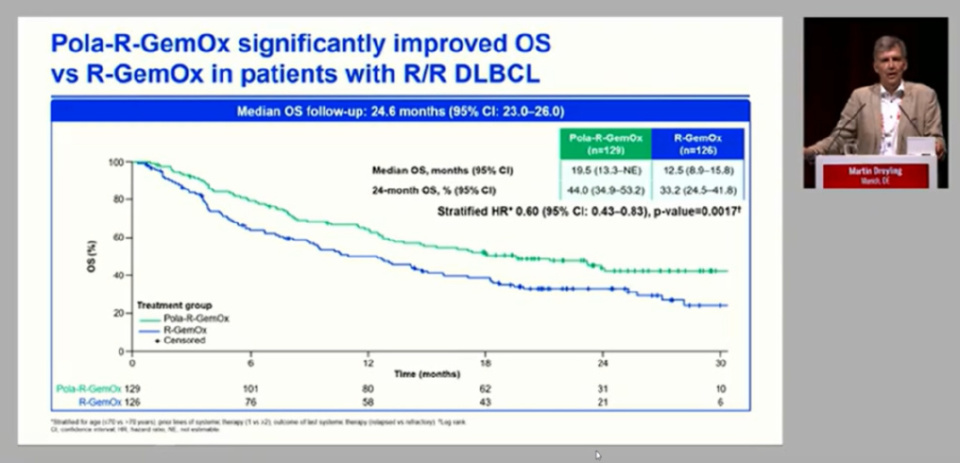
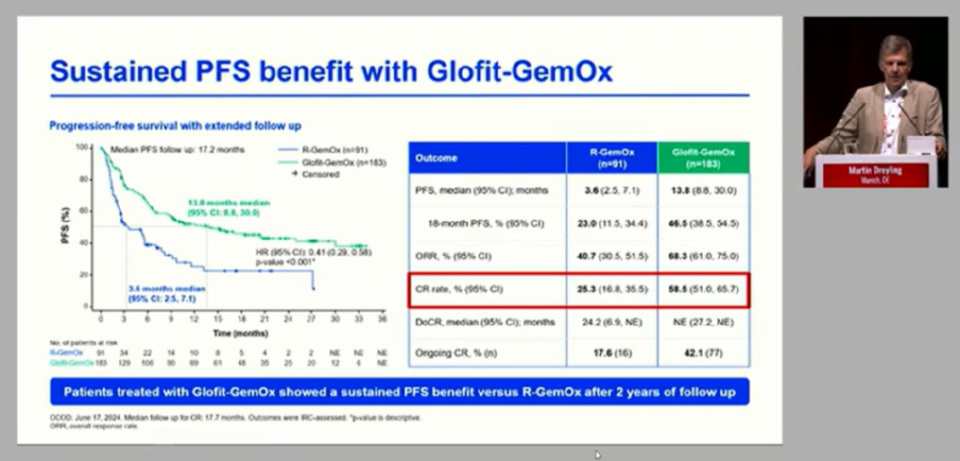
既往R-GEMOX或含铂化疗是复发/难治性(R/R) DLBCL的标准方案。然而,新标准正在确立。维泊妥珠单抗(Pola)可被视为“靶向化疗”,Pola-R-GemOx 方案显示出优势——无进展生存期(PFS)和总生存期(OS)显著延长。CD20/CD3双特异性抗体格菲妥单抗(Glofit)联合GemOx方案与R-GemOx方案相比也显示出CRR提升约30%,早期PFS数据提示显著获益,且OS趋势积极。此外,Mosun-Pola使CRR翻倍,并与R-GemOx相比提高了30%的ORR。
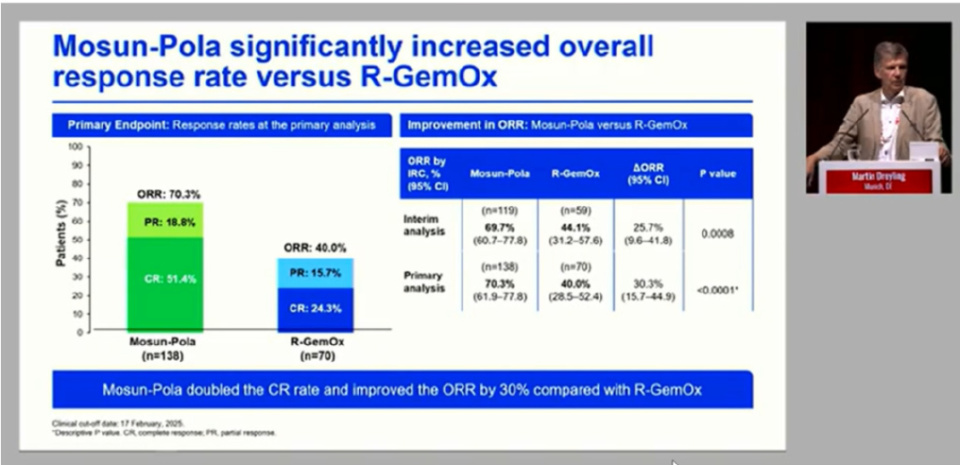
Dreyling教授强调,本次会议标志着R/R DLBCL“单纯化疗时代”的终结。抗体偶联药物、双特异性抗体等高效靶向药物与化疗或彼此联合已成为新的治疗选择。虽然化疗在部分联合方案中仍有作用,但其核心地位已被取代。
05
免疫治疗:持续优化与挑战
CAR-T细胞疗法已在二线R/R DLBCL中确立标准治疗地位,为近半数患者带来长期缓解。本次会议聚焦于如何克服另一半患者的治疗失败的问题。例如:多靶点策略——攻击多个抗原表位以克服抗原丢失等耐药机制;细胞产品优化——探索使用体内扩增能力更强的细胞类型(如干细胞记忆T细胞衍生的CAR-T),可能改善耐受性、缩短制备时间并增强持久性;可及性提升——西班牙、以色列等地的学术机构推动“自研”(academic) CAR-T细胞研究,旨在降低成本、提高可及性。
06
会议共识与未来展望
最后,Dreyling教授总结道,18-ICML会议的核心价值在于推动“学术共识”与“临床转化”的双向融合。会议在DLBCL研究领域取得多项突破性进展,包括分子分型成熟化(精细化分子分型已进入临床实践“黄金期”,是推动DLBCL靶向治疗的基础)、微环境作用明晰(TME分型是预测免疫治疗疗效的关键因素)、治疗范式变革(DLBCL的治疗已告别单纯化疗时代)及免疫治疗持续进化(CAR-T等免疫疗法在不断优化)。
基于会议成果,学界对未来发展形成三大共识:①分类统一:2026年第六版WHO淋巴瘤分类将实现全球统一,为临床实践提供标准化语言;②精准诊疗:DLBCL的分子亚型分类将成为靶向治疗的基础,需加速建立可普及的检测体系;③联合策略:免疫治疗与靶向药物的联合应用将重塑治疗格局,尤其在一线治疗中需验证新方案的长期获益。
正如Dreyling教授所言:“卢加诺精神的本质,是用科学对话取代学术分歧,用临床需求驱动研究方向。我们正站在淋巴瘤精准治疗的新纪元,但必须清醒认识到,从实验室到临床的‘最后一公里’仍需全球协作。”呼吁研究者在最终统一分类达成前,考虑建立“工作转换方案”以实现不同体系间的互译,便于临床医生遵循和应用。他坚信现在是DLBCL靶向治疗的最佳时机,并展望未来两年内将有大量新数据涌现,持续推动领域进步。随着分子生物学与免疫治疗的深入发展,淋巴瘤诊疗即将迈入“精准医学2.0时代”,而2年后的第19届会议,必将见证更多突破性成果的临床转化。卢加诺会议所凝聚的协作精神与产生的丰硕成果,将持续引领淋巴瘤研究迈向精准化、个体化的新时代。

2027,不见不散!
摘要提交开启日期:2026年12月1日
摘要提交截止日期:2027年3月15日
注册开启日期:待公布
酒店预订截止日期:待公布