近日,EHA 2025大会报告(EHA Perspectives Congress Reports)正式发布,分为恶性血液学和非恶性血液学两大部分。报告全面梳理了大会期间公布的重大科研成果与临床进展,为全球血液学专业人士提供了深入了解领域前沿动态的权威参考。本期特别整理了恶性血液学报告中关于“淋巴系统恶性肿瘤微环境及下一代建模”的专题内容,旨在为大家提供富有价值的临床与科研洞见。
精选演讲概览

患者来源的3D淋巴瘤模型
由于淋巴瘤细胞与肿瘤微环境(TME)之间复杂的相互作用,建立B细胞淋巴瘤的临床前模型极具挑战性。目前,主要有三种方法用于构建稳健的临床前3D淋巴瘤模型:细胞系、小鼠模型和患者来源的细胞。PDLS,即患者来源的淋巴瘤球体,是一种稳健的体外模型,结合了淋巴瘤细胞、单核细胞、自体T细胞和特定的细胞因子混合物[1]。
PDLS是表征疾病病理学、预测患者用药反应、发现新靶点以及理解耐药机制的宝贵模型。仿生成分,如天然或合成水凝胶,可模拟细胞外基质,为3D培养系统提供支架结构,支持球体生长。例如,PDLT(患者来源的淋巴瘤肿瘤类器官)由肿瘤活检样本、大鼠胶原蛋白和基质细胞培养而成,并在IL-4刺激下形成直径约1 mm的肿瘤类器官,包含CD19+和CD3+细胞。
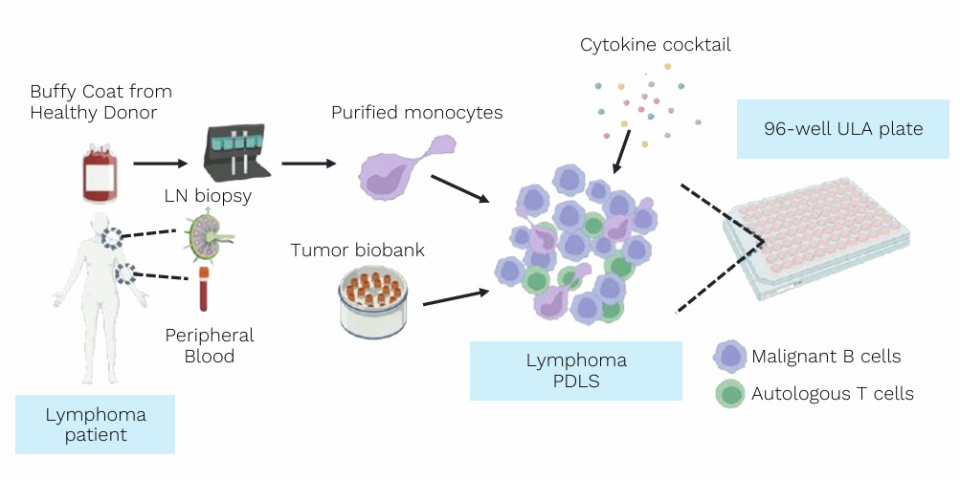
Dobano-López等既往发表的论文中,使用来自滤泡性淋巴瘤(FL)患者的细胞构建了PDLS模型[2]。该模型成功再现了B细胞和T细胞在盘状3D结构中的增殖,以及呈现中间型M1/M2表型的巨噬细胞。PDLS模型中的B细胞转录通路与FL淋巴结中的转录特征高度相似,T细胞群体也保留了CD4与CD8群体中的多种表型。
研究人员还利用该FL-PDLS模型评估了双靶向CD19/BCMA的CAR-T细胞治疗非霍奇金淋巴瘤的潜力[3]。此外,类似的PDLS模型也已被证明可在其他疾病中复制淋巴结TME,如套细胞淋巴瘤[4]。尽管FL-PDLS模型尚未能够模拟淋巴结内和淋巴结间的变异性以及肿瘤克隆随时间的演化,但未来有望通过整合更多微环境成分,在体外重建更完整的TME。
Pola-R-GemOx在复发/难治性DLBCL中显示出OS获益
维泊妥珠单抗(Polatuzumab vedotin)是一种靶向CD79b的抗体偶联药物(ADC),目前已在欧盟获批用于初治及复发/难治性弥漫大B细胞淋巴瘤(DLBCL)治疗,后者的适应证是与苯达莫司汀和利妥昔单抗联合用药[5]。尽管已有多种疗法,但复发/难治性DLBCL患者仍迫切需要更多替代治疗方案。
在EHA 2025的全体会议上,Matthew Matasar博士公布了POLARGO研究(NCT04182204)的最新结果。这是一项全球多中心、随机的Ⅲ期临床研究,评估维泊妥珠单抗联合利妥昔单抗、吉西他滨和奥沙利铂(Pola-R-GemOx)与R-GemOx方案在既往接受过至少一线治疗且不适合进行自体干细胞移植的R/R DLBCL患者中的疗效与安全性[6]。
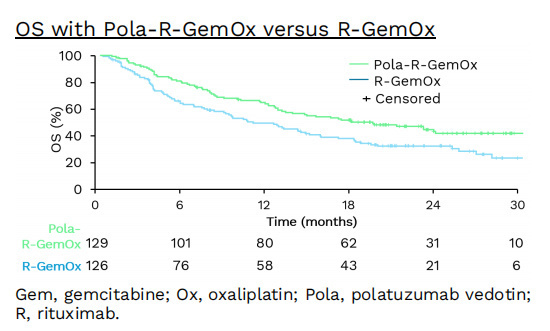
在纳入15位患者的安全性预试验阶段后,共有255名患者按1:1比例被随机分配接受Pola-R-GemOx或R-GemOx治疗。研究结果显示,Pola-R-GemOx在总生存期(OS)这一主要终点上具有显著优势,中位OS较单用R-GemOx延长了7个月(HR=0.60,95%CI:0.43-0.83,P=0.0017)。
尽管Pola-R-GemOx组报告的外周神经病变和感染发生率较高,但该治疗方案的耐受性仍在可控范围内,显示出良好的疗效,为不适合使用T细胞耗竭药物苯达莫司汀的患者提供了有力替代选择。研究结果支持在特定患者中将维泊妥珠单抗加入GemOx方案,为超越传统挽救治疗提供了更广泛的治疗选择。
Mosunetuzumab SC在MZL患者中诱导了高缓解率
在EHA 2025上展示的另一项重要的淋巴瘤临床试验是MorningSun研究。这项由John Burke博士展示的Ⅱ期篮子研究 (NCT05207670) 评估了莫妥珠单抗(Monsunetuzumab,Mosun) 皮下(SC)制剂在初治症状性边缘区淋巴瘤 (MZL) 患者中的疗效和安全性[7]。Mosun是一种靶向CD20/CD3的双特异性抗体,目前已被批准用于复发/难治性滤泡性淋巴瘤(R/R FL)的固定疗程静脉注射(IV)治疗。
在本研究中,Mosun SC采用阶梯式剂量递增给药方式:第1周期第1天5 mg,第8天和第15天各45 mg,随后每周期(每21天为一个周期)第1天给予45 mg,最长可持续17个周期,直至疾病进展或出现不可接受的不良反应。为了降低细胞因子释放综合征(CRS)风险,研究在第1周期内进行Mosun SC的递增剂量给药,同时第1和第2周期强制使用糖皮质激素预处理,后续周期可选择性使用。
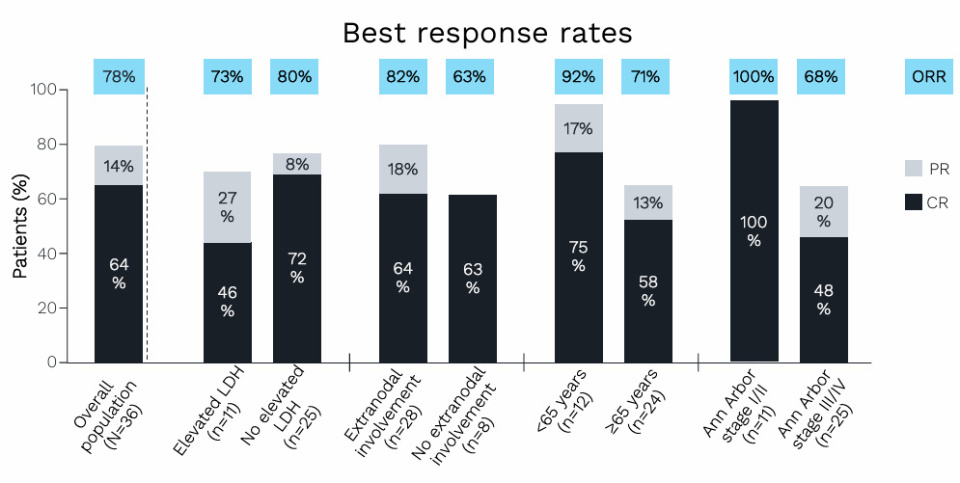
在中位随访18个月后,研究达到主要终点——总缓解率(ORR)为78%,完全代谢缓解率(CMR)为64%。截至分析时,6个月无进展生存率(PFS)为90.5%,12个月为83.6%,中位PFS尚未达到。最常见的不良事件包括注射部位反应、疲劳、腹泻、中性粒细胞减少和可控的CRS。
研究者指出,与静脉注射Mosun相比,Mosun SC具有相似的疗效和良好的CRS可控性。此外,Mosun SC无需强制住院治疗,可在社区门诊进行给药,为MZL患者提供了更便捷的治疗选择,支持其作为一线治疗方案开展进一步研究。
CLL靶向治疗的耐药机制
慢性淋巴细胞白血病 (CLL) 患者的病情进展各异,有些患者无需治疗,而有些患者则需要在确诊后立即接受治疗。其中部分患者虽经治疗获得缓解,但缓解期短暂,病情随后迅速恶化。尽管针对CLL异常信号通路和分子缺陷的小分子抑制剂显著改善了患者生存率,但由于肿瘤的固有异质性、白血病克隆持续存在,以及支持肿瘤克隆存活的肿瘤微环境(TME)等因素,患者仍可能在治疗过程中逐渐产生耐药[8]。
CLL的发生与进展并非仅依赖白血病细胞本身的特性,还涉及与TME的复杂相互作用。Herishanu等曾指出,淋巴结(LN)是CLL发病的关键部位,在此处CLL细胞被激活并促进肿瘤生长[9]。与外周血中的CLL细胞相比,LN中的CLL细胞表现出更高的基因表达活性,尤其是在B细胞受体(BCR)信号通路和NF-κB通路的激活方面。
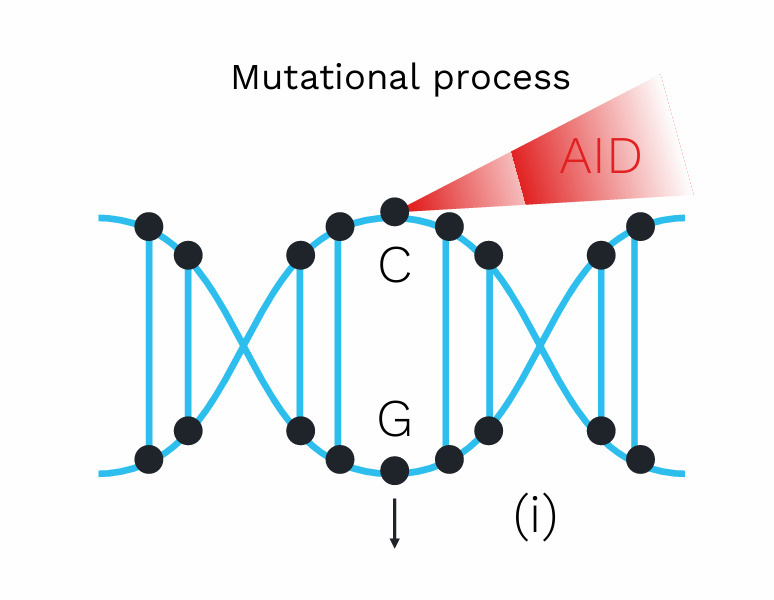
此外,Kasar等对一组CLL患者进行全基因组测序分析发现,最常突变的基因具有符合活化诱导胞苷脱氨酶(AID)活性的突变模式[10]。AID在B细胞发育过程中可促使胞苷脱氨为尿嘧啶,修复过程中通过错误修复机制引发典型(canonical)或非典型(non-canonical)AID突变。研究表明,非典型AID活性在CLL发展的早期阶段发挥更重要作用,而典型AID相关突变则在疾病后期逐渐显现。然而,总体而言,AID表达水平在存在或不存在亚克隆扩增的患者间并无显著差异[11]。
另一方面,T细胞介导的免疫监视机制可能是限制LN中克隆进化的重要因素之一。综上,研究强调了破坏肿瘤微环境的病理性相互作用以及抑制BCR信号通路,可能是未来CLL治疗中应优先考虑的策略方向。
新型BTK降解剂BGB-16673在R/R CLL/SLL中展现抗肿瘤活性
布鲁顿酪氨酸激酶抑制剂(BTKi)已彻底改变B细胞白血病的治疗格局,包括慢性淋巴细胞白血病(CLL)和小淋巴细胞淋巴瘤(SLL),目前已成为治疗初治(TN)及复发/难治性(R/R)CLL/SLL患者的主要药物。然而,BTKi的持续使用可能导致不耐受或因突变而出现耐药性,从而引发临床复发[12-13]。
BGB-16673是一种BTK降解剂,通过不同于传统BTKi的机制中断B细胞受体(BCR)信号通路。该药为口服给药、靶向BTK的嵌合降解激活化合物(CDAC),可降解野生型BTK及多种突变型BTK。在EHA 2025大会上,Lydia Scarfò博士报告了CaDAnCe-101 I期临床试验的最新疗效与安全性数据。本研究评估了BGB-16673在至少接受过一种治疗(包括BTKi)后的R/R CLL/SLL患者中的应用效果[14]。
在开放标签、剂量递增的Ia阶段试验中,共纳入72例复发/难治性B细胞恶性肿瘤患者,给予BGB-16673每日一次口服(剂量范围为50-600 mg),28天为一个周期。随后在1b阶段进行安全性扩展,纳入120例CLL/SLL或其他B细胞肿瘤患者。本次分析纳入66例患者,中位随访时间为15.6个月。基线特征显示,入组患者中不乏具有不良生物学标志者,包括:Binet C期(46.8%)、IGHV未突变型(77.6%)、17p缺失(del[17p])和/或TP53突变(65.2%)、复杂核型(≥3种异常;50.0%)。突变情况包括BTK突变(38.1%)、PLCG2突变(15.9%)及二者兼有(7.9%)。
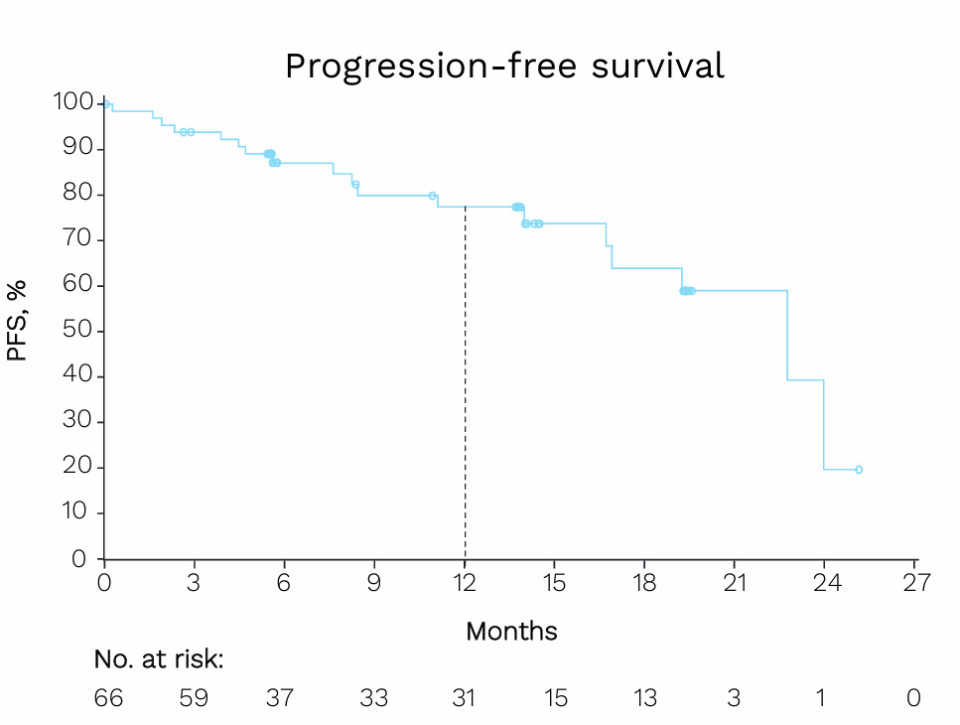
在安全性方面,BGB-16673表现出良好的耐受性。最常见的≥3级不良事件包括中性粒细胞减少(24%)、肺炎(11%)和血小板减少(5%)。严重不良事件发生率为45.5%,其中12.1%被认为与治疗相关。4例患者出现与治疗相关不良事件(TEAEs)导致死亡,但均与治疗无关;9例患者停药,其中2例因TEAE所致。疗效方面,总体缓解率(ORR)达到84.8%,其中完全缓解(CR)/骨髓不完全恢复的CR(CRi)为4.5%,部分缓解(PR)为66.7%,合并淋巴细胞增多的部分缓解(PR-L)为13.6%,1年无进展生存率(PFS)达77.4%。
这些数据表明,BGB-16673具有良好安全性与耐受性,并在R/R CLL/SLL患者中显示出令人鼓舞的抗肿瘤活性。尤其重要的是,无论基线是否存在突变或其他高风险特征,该药均展现出治疗反应,提示其具有广泛的临床适用性,适合复杂患者群体。
总体而言,本次EHA 2025大会上展示的最新数据,有助于我们更科学地制定淋巴系统恶性肿瘤的治疗策略——包括运用新的临床前模型和测试新型药物,以更深入理解肿瘤耐药机制及其与微环境的相互作用。
参考文献:
[1]Pérez-Galán P. 3D lymphoma models. Oral presentation p151-1 presented at EHA2025. [2]Dobano-López C, et al. Patient-derived follicular lymphoma recapitulate lymph node signaling and immune profile uncovering galectin-9 as a novel immunotherapeutic target. Blood Cancer J. 2024;14(1):75.
[3]Guedan S. Next-Generation CAR-T: Dual specificity to counter tumor escape in lymphoma. Oral presentation p196-2 at EHA2025.
[4]Araujo-Ayala F, et al. A novel patient derived 3D model recapitulates mantle cell lymphoma lymph node signaling, immune profile and in vivo ibrutinib responses. Leukemia. Jun;37(6):1311-1323.
[5]https://www.ema.europa.eu/en/medicin es/human/EPAR/polivy [accessed 16 June 2025].
[6]Matasar M. Polatuzumab vedotin, rituximab, gemcitabine and oxaliplatin (Pola-R-GemOx) for relapsed/refractory (R/R) diffuse large B-cell lymphoma (DLBCL): results from the randomized Phase III Polargo trial. Oral presentation s101 at EHA2025.
[7]Burke M. MorningSun: open-label Phase II trial of the efficacy and safety of subcutaneous mosunetuzumab (mosun sc) as frontline (1L) treatment in symptomatic patients with marginal zone lymphoma (MZL). presentation s232 at EHA2025.
[8]Sun C. The impact of the CLL microenvironment. Oral presentation p257-1 at EHA2025.
[9]Herishanu Y, et al. The lymph node microenvironment promotes B-cell receptor signaling, NF-kappaB activation, and tumor proliferation in chronic lymphocytic leukemia. Blood 2011;117(2):563-74.
[10]Kasar S, et al. Whole-genome sequencing reveals activation-induced cytidine deaminase signatures during indolent chronic lymphocytic leukaemia evolution. Nat Commun. 2015;6:8866.
[11]Sun C, et al. The immune microenvironment shapes transcriptional and genetic heterogeneity in chronic lymphocyticleukemia.Blood Adv.2023;7(1):145-158.
[12]Woyach JA, et al. Resistance mechanisms for the Bruton's tyrosine kinase inhibitor ibrutinib. N Engl J Med.2014;370:2286-2294.
[13] Wang E, et al. Mechanisms of Resistance to Noncovalent Bruton's Tyrosine Kinase Inhibitors. N Engl J Med. 2022;386:735-743.
[14]Scarfo L. Updated efficacy and safety of the bruton tyrosine kinase (BTK) degrader BGB-16673 in patients (pts) with relapsed or refractory (r/r) CLL/SLL: results from the ongoing phase (ph) 1 CaDAnCe-101 study. Oral presentation s158 at EHA2025.