编者按:2025年美国临床肿瘤学会(ASCO)年会于当地时间 5月30日至6月3日在美国芝加哥盛大召开。作为全球临床肿瘤学领域规模最大、学术水平最高且最具权威性的盛会之一,ASCO年会汇聚全球肿瘤学界医生及专业人士,聚焦肿瘤领域的热点与难点问题,带来国际前沿研究发现和临床试验成果展示。在急性髓系白血病(AML)治疗领域,众多创新药物与治疗方案纷纷涌现,为AML患者带来了新的希望和更多选择。《肿瘤瞭望-血液时讯》遴选其中的重磅研究成果,为您呈现前沿资讯。
全口服DEC-C联合VEN方案:重塑不适合强化疗新诊断AML患者治疗体验
摘要号:6504
标题:An all-oral regimen of decitabine-cedazuridine (DEC-C) plus venetoclax (VEN) in patients (pts) with newly diagnosed acute myeloid leukemia (AML) ineligible for intensive induction chemotherapy: Results from a phase 2 cohort of 101 pts
中文标题:全口服方案地西他滨-cedazuridine(DEC-C)联合维奈克拉(VEN)用于不适合强化诱导化疗的新诊断急性髓系白血病(AML)患者:来自101例患者的Ⅱ期队列研究结果
第一作者:Amer Zeidan(美国耶鲁大学医学院)
背景:基于III期VIALE-A试验(完全缓解[CR]率为36.7%;中位CR持续时间为17.5个月;中位总生存期[OS]为14.7个月),BCL-2抑制剂VEN联合阿扎胞苷(AZA)获批用于治疗年龄≥75岁且不适合强化诱导化疗的AML患者。然而,每月连续7天在诊所接受AZA静脉注射直至疾病进展,给患者带来了沉重负担。此外,多项调整后的比较表明AZA与地西他滨具有相似的临床疗效。口服DEC-C(地西他滨35 mg和cedazuridine 100 mg)与静脉注射地西他滨的药代动力学(PK)曲线下面积(AUC)相当。本项I/II期试验旨在评估DEC-C联合VEN全口服方案在年龄≥75岁或因合并症无法接受一线强化诱导化疗的AML患者中的疗效(NCT04657081)。本次报告该试验关键的II期部分的结果。
方法:符合条件的患者接受口服 DEC-C(第1至5天)联合VEN(400 mg/d,28天为一周期;在第1周期中VEN采用递增方案(第1天100 mg,第2天200 mg,第3天及以后400 mg)。第1周期骨髓检查为可选,VEN和/DEC-C的剂量调整基于患者反应和血细胞计数恢复情况。主要终点是基于欧洲白血病网(ELN)2017缓解标准的CR率。
结果:截至2024年9月30日,共纳入101例患者,中位治疗周期数为4(范围1-15)。患者中位年龄78岁。根据ELN 2017分类标准,31.7%的患者预后良好,33.7%预后中等,29.7% 预后不良。中位随访时间为11.2个月。CR率和 CR/CR伴血液学不完全恢复(CRi)率为46.5%(95% CI:36.5%-56.7%)和 63.4%(95% CI:53.2%-72.7%),中位CR达成时间为2.4个月。中位CR持续时间尚未达到;在达成CR的患者中,80.0%在6个月时仍保持CR,75.3%在12个月时仍保持CR。中位OS为15.5个月(95% CI:7.6-未达到)。98.0%的患者报告了≥3 级治疗相关不良事件,最常见的是发热性中性粒细胞减少症(49.5%)、贫血(38.6%)和中性粒细胞减少症(35.6%)。30天和60天死亡率分别为3.0%和9.9%。PK数据证实口服DEC-C和VEN之间无药物相互作用。
结论:DEC-C 联合VEN的全口服方案在不适合强化诱导化疗的新诊断AML患者中,与静脉注射AZA 联合VEN方案相当,在安全性、疗效及生存率方面表现良好。这些数据支持DEC - C 联合VEN有望成为这类患者的治疗选择。
ICT01联合AV:点亮老年/不适合强化疗新诊断AML患者治疗新希望
摘要号:6507
标题:γ9δ2 T-cell activation (γδTCA) with ICT01 combined with azacitidine-venetoclax (AV) for older/unfit adults with newly diagnosed (ND) AML: Preliminary efficacy and dose selection in phase 1/2 study EVICTION
中文标题:ICT01介导的γ9δ2 T细胞激活(γδTCA)联合阿扎胞苷-维奈克拉(AV)治疗老年/unfit新诊断(ND)AML成人患者:EVICTIONⅠ/Ⅱ期研究的初步疗效及剂量选择
第一作者:Pierre Yves Dumas(法国波尔多大学医疗中心)
背景:AML会损害免疫监视,绕过靶点识别及随后的细胞毒性T细胞反应。AV的免疫调节和细胞毒性效应与ICT01诱导的γδTCA在带有γδTC过继转移的体内AML模型中展现出协同增效作用。ICT01是一种首创的人源化抗butyrophilin 3A单克隆抗体(mAb),其 Fc 功能被阻断,能选择性地诱导 γδTCA,从而实现直接的抗白血病细胞毒性以及IFNγ和TNFα的释放。γδTC 在移植后抗白血病效应中发挥关键作用,且肿瘤内γδTC的存在具有预后意义。ICT01诱导的γδTCA呈剂量依赖性,且安全、耐受性良好。本项剂量优化的Ⅰ/Ⅱ期研究旨在探讨ICT01介导的γδTCA联合AV的疗效。
方法:纳入年龄≥75岁或不适合接受强化化疗的新诊断AML患者,按 1:1 随机分配至AV联合ICT01 10 mg(ICT01低剂量组)或ICT01 75 mg组(ICT01高剂量组),每4周给药一次(Q4W)。研究评估了细胞遗传学、二代测序(NGS)、外周血(PB)和骨髓(BM)的药效学(PD)、安全性及抗肿瘤疗效。
结果:截至2025年1月20日,共45例患者随机分组,其中33例有明确疾病评估结果,中位年龄75岁(范围 51-87 岁),少数患者(30%)根据ELN 2024标准为低危,55%患者存在不确定风险的异常情况,其中一些提示对AV反应不佳。患者诊断时骨髓原始细胞中位数为 38%(范围5%-98%)。研究未报告剂量限制性毒性(DLT),所有患者均至少发生1例不良事件,30天死亡率为3%。42%患者出现3/4级发热性中性粒细胞减少症,71%患者出现中性粒细胞减少症。ICT01可在PB和BM中快速、可重复地诱导γδTCA,随后血清IFNγ和TNFα 水平升高,反映了下游免疫细胞效应。首次给予ICT01后,PB和BM中的γδTC 计数迅速下降,在ICT01低剂量给药期间恢复至接近基线值,但在持续给予ICT01高剂量时几乎检测不到。ICT01低剂量组具有良好的风险-效益特征,CR/CRi达90%(CR 71%,CRi 19%),中性粒细胞减少症/发热性中性粒细胞减少症发生率低于ICT01高剂量组及已发表数据。而 ICT01高剂量组因重复给药导致γδTC 激活死亡,PD效应与较低的疗效相关(CR/CRi 75% [CR 42%,CRi 33%])。值得注意的是,根据ELN 2024,无论患者是不利(TP53/CK的CR 40%、CR/CRi 60%;N=10)、中等/不确定(MECOMr、NRAS、ASXL1、JAK2、DNMT3A、SF3B1、U2AF1、SRSF2、RUNX1、STAG2的CR 47%、CR/CRi 95%),还是有利风险突变(NPM1、IDH1/2的CR 80%、CR/CRi 90%),治疗反应率尤其是ICT01低剂量组的反应率均很高。
结论:对于AV联合治疗,推荐ICT01 Ⅱ期剂量为每 4 周 10 mg 。两种ICT01方案均安全、耐受性良好,在老年/不适合高强度化疗的新诊断AML患者中产生了非常高的 CR 和 CR/CRi 率。在高危患者中观察到的高反应率值得进一步临床研究。
menin抑制剂:破局复发/难治性NPM1突变AML患者治疗难题
摘要号:6506
标题:Ziftomenib in relapsed/refractory (R/R) NPM1-mutant acute myeloid leukemia (AML): Phase 1b/2 clinical activity and safety results from the pivotal KOMET-001 study
中文标题:Ziftomenib治疗复发/难治性(R/R)NPM1突变急性髓系白血病(AML):关键KOMET-001研究的1b/2期临床活性和安全性结果
第一作者:Eunice Wang(美国罗斯威尔·帕克综合癌症中心)
背景:NPM1突变(NPM1-m)驱动约30%的AML患者发生白血病。尽管进行了当前的风险分层,但几乎一半患者在一年内会出现复发/难治性(R/R)疾病,此后化疗后的完全缓解(CR)率不足10%。Ziftomenib是一种强效、高选择性、口服的研究性menin抑制剂,在成人R/R NPM1-m和KMT2A重排(KMT2A-r)AML中单药治疗及联合治疗均显示出临床活性,推荐的2期单药治疗剂量为每日一次(QD)600 mg。本次介绍关键KOMET-001研究中接受600 mg QD Ziftomenib治疗NPM1-m患者的主要分析结果。
方法:KOMET-001(NCT04067336)是一项在成人R/R AML中进行的多中心、开放标签的1/2期研究。在2期中,NPM1-m R/R AML患者接受600 mg QD Ziftomenib治疗。2期主要终点:完全缓解(CR)/CR伴部分血液学恢复(CRh);关键次要终点:复合CR(CRc)、CR/CRh和CRc持续时间以及安全性。以下分析包括来自1b/2期的NPM1-m患者数据。
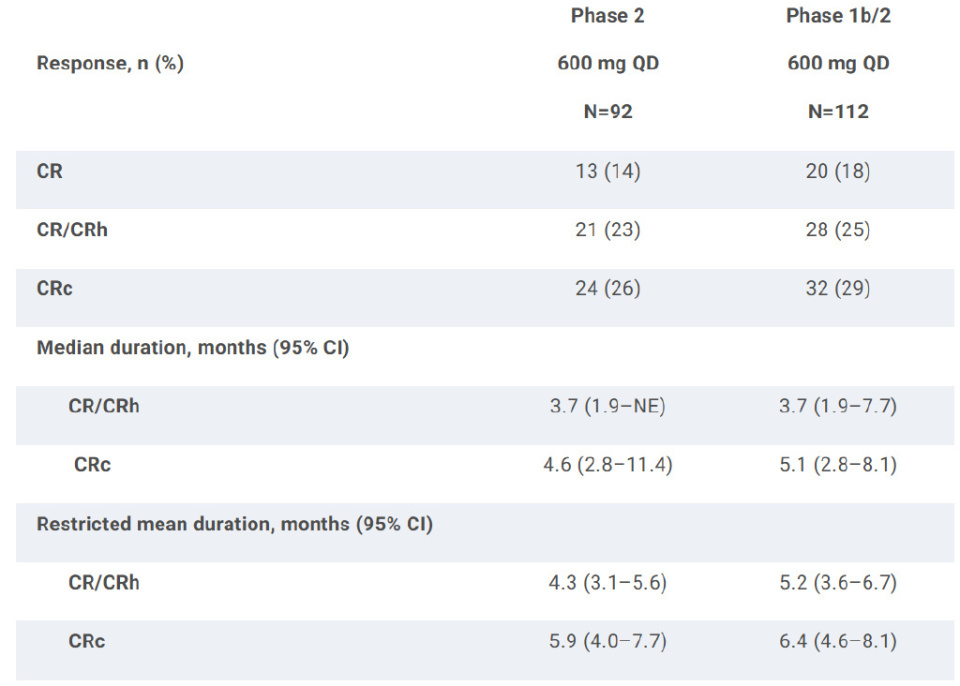
结果:2期主要终点达成(P=0.0058)。截至2024年12月20日,1b/2期共纳入112例患者(51%来自美国/加拿大,49%来自欧洲/英国),接受600 mg QD Ziftomenib治疗,中位随访时间为4.2个月。患者中位年龄69岁(范围22-86岁),56%为女性,83% ECOG PS 0-1,既往治疗中位数为2次(范围1-7),包括60%既往接受过维奈克拉(VEN)治疗和23%接受过移植治疗。所有1b/2期患者中,CR/CRh率为25%(28/112;95%CI:17-34),总体缓解率为35%(39/112;95% CI:26-44)。在2期患者中,23%(21/92;95 CI:15-33)实现CR/CRh(见下表),在可评估的CR/CRh应答者中,67%(10/15)达到微小残留病(MRD)阴性(本地检测)。在VEN未治疗和暴露过的患者中观察到相当的CR/CRh率(分别为21% vs. 24%)。Ziftomenib耐受性良好,3%(3/112)的患者因治疗相关不良事件(TRAEs)停药。40%(45/112)的患者出现3级及以上TRAEs,包括13%分化综合征(均为3级),贫血、发热性中性粒细胞减少症和血小板减少症各≤5%,以及2% QTc延长(3级)。
结论:在关键的KOMET-001研究中,2期主要终点达成:无论患者是否接受过VEN治疗,Ziftomenib在R/R NPM1-m AML中均实现了深度且持久的应答。Ziftomenib耐受性良好,骨髓抑制有限,仅3%因Ziftomenib相关不良事件停药。综合这些数据,支持将Ziftomenib单药治疗作为R/R NPM1-m AML的新治疗选择。