近日,EHA 2025大会报告(EHA Perspectives Congress Reports)正式发布,分为恶性血液学和非恶性血液学两大部分。报告全面梳理了大会期间公布的重大科研成果与临床进展,为全球血液学专业人士提供了深入了解领域前沿动态的权威参考。本期特整理非恶性血液学报告中关于“造血干细胞及其微环境:从生理到病理”的专题内容,分为上下两部分(点击此处查看上部分内容),旨在为大家提供富有价值的临床与科研洞见。
精选演讲概览
应激条件下的骨髓微环境
骨髓微环境通过密集的基质细胞网络为造血干细胞(HSCs)提供结构框架。各种免疫和基质细胞共同塑造骨髓微环境,与HSCs相互作用并调控其状态,而生长因子、细胞因子和细胞外基质(ECM)等非细胞性物质则为HSC的生长和维持提供必要的营养和信号。
骨髓的非造血基质框架由窦状内皮细胞(SECs)、动脉内皮细胞以及间充质基质细胞(MSC)群体组成,尤其是富含CXCL12的LepR+网状细胞(CARc),它们在调节造血过程中发挥着积极作用。SEC与CARc网络的组织与相互作用在整个骨髓中高度稳定。
在小鼠中,这些基质网络具有极强的损伤耐受性:即使经历重度骨髓消耗性破坏,也能通过自组织再生过程完全重建正常的网络拓扑结构。稳态CARc群体的再生激活应激修复途径,特别是mTORC1信号通路,并在骨髓基质中引起长期的转录组后遗症,这与ECM的产生和细胞衰老的改变相关。
骨髓内皮细胞(EC)在造血调控中发挥关键作用,范可尼贫血等疾病模型已证实这一点;然而,ECs功能障碍的分子驱动因素仍不清楚。TGF-β1可在多种细胞类型中调控造血,因此研究者尝试抑制TGF-β1,以观察其能否改善功能异常EC模型中的造血功能[5]。
体外实验显示,TGF-β1过表达损害了骨髓内皮细胞的功能,包括迁移和管腔形成,同时增加细胞凋亡及活性氧(ROS)水平;通过沉默TGF-β通路基因可逆转这些损伤。在小鼠模型中,AAV介导的TGF-β受体(TGF-βRI)构成性活性过表达,导致骨髓内皮细胞功能损害并加重造血损伤。多组学研究进一步阐明,TGF-β1的持续激活驱使骨髓内皮细胞进入适应性修复过程,这可能与VEGF和Notch通路之间相互作用的失调有关,最终导致p38α的激活。
为了验证这些发现的临床相关性,研究者在体外对移植后造血功能不良(PGF)患者的骨髓样本进行 TGF-β1 抑制处理,并与移植后造血功能良好患者及健康供者的样本进行对比。结果显示,TGF-β1 抑制可恢复PGF患者骨髓内皮细胞的功能。
一项前瞻性临床试验初步评估了luspatercept(一种TGF-β配体陷阱)对7例造血干细胞移植(HSCT)后贫血患者的疗效,结果令人鼓舞:多谱系造血恢复增强。
RANK配体(RANKL)是由成骨细胞和骨细胞分泌的细胞因子,可与破骨祖细胞膜上的 RANK 结合,促使成熟破骨细胞介导骨吸收。RANKL基因突变导致破骨细胞缺乏性骨质疏松,确立了其在维持骨稳态和高效造血中的角色。RANKL还可调控基质干细胞(SSC)向成骨-软骨分化。鉴于SSC对HSC微环境的重要性,研究者敲除RANKL基因,观察其对骨髓SSC支持HSC能力的影响[6]。
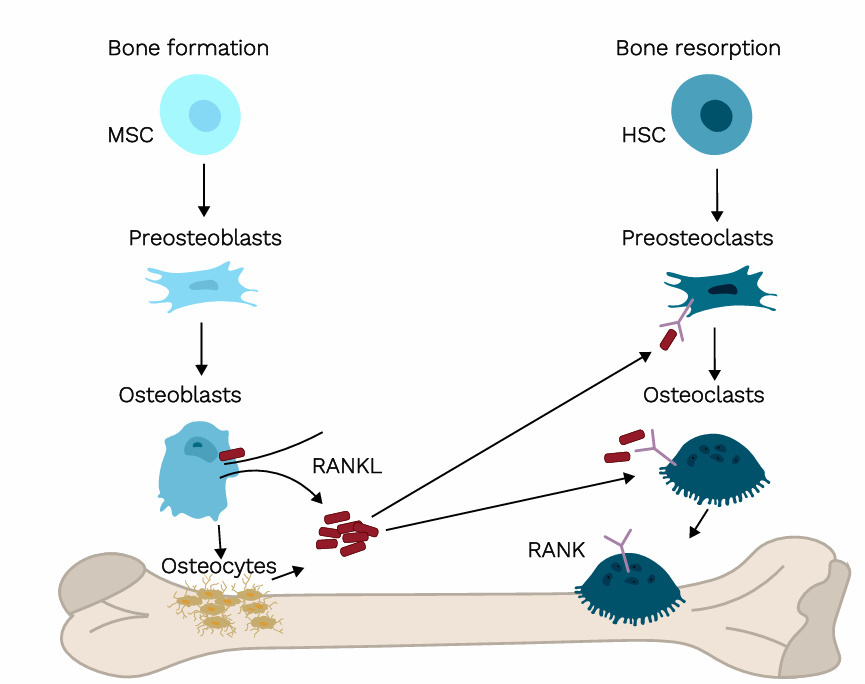
RANKL/RANK 轴在骨稳态中的作用
从RANKL敲除(RANKL-KO)小鼠骨髓提取的干细胞和祖细胞表现出静息性丧失及早发髓系分化;共同淋巴祖细胞比例下降,且向B细胞分化能力减弱。这些缺陷仅限于骨髓,在RANKL-KO小鼠的胎肝或脾脏中未观察到。将RANKL-KO骨髓细胞移植至野生型受体的骨髓重建实验表明,造血缺陷源于RANKL-KO小鼠的微环境缺陷,而非细胞自主性缺陷。基因表达研究证实,与HSC支持相关的SSC基因表达改变,且从HSC阶段即出现谱系启动缺陷。研究结果提示,在骨髓微环境中持续抑制 RANKL 信号通路可能会影响骨髓稳态的整体平衡。
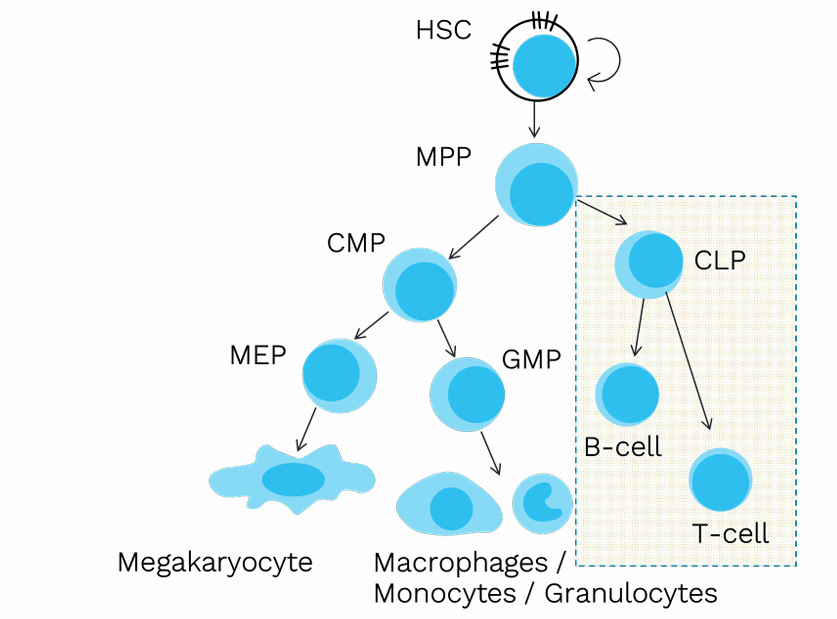
RANKL敲除小鼠的造血各阶段概述及受影响的祖细胞和成熟细胞(虚线区域)
克隆性造血(CH)与阿尔茨海默病(AD)
Dnmt3a和Tet2基因突变在造血干细胞(HSCs)中被正向选择,导致克隆性造血(CH)。有趣的是,先前研究发现潜能未定的克隆性造血(CHIP)与阿尔茨海默病(AD)风险降低相关,并已在英国生物样本库的大型队列中得到验证[7]。
为探讨CH与AD之间的相关性,研究者将Dnmt3a或Tet2功能缺失(LoF)的骨髓移植至 6–8周龄的AD易感小鼠(5xFAD)。移植后8周,这些小鼠接受每周 1 次、共 8 周期的脂多糖(LPS)注射。
在这一AD易感小鼠移植模型中,Tet2 LoF小鼠的晚发性AD风险降低,而Dnmt3a LoF小鼠未见此效应。Tet2 LoF通过增强趋化因子信号,促进CCR2介导的非经典单核细胞及 M1 型巨噬细胞向中枢神经系统浸润。Tet2 LoF的髓系细胞及小胶质样细胞表现出更强的β-淀粉样蛋白清除能力,从而可能减轻AD的症状表现。
太空贫血
对宇航员血液进行检测发现,太空旅行会引起与胰岛素和雌激素信号等关键通路相关的基因表达变化。宇航员是健康成年人,但在太空中常出现一种以胎儿血红蛋白(HbF)升高为特征的贫血。研究人员利用一套独特的多组学技术,分析了不同太空时间点、不同红细胞生成阶段的血红蛋白表达情况[8]。
结果显示,珠蛋白基因表达存在显著差异,并与样本的时空特征相对应。由于宇航员人数有限且血液样本量少,研究团队开发了一种新的红细胞谱系富集方案。未来成果有望阐明地中海贫血、镰状细胞病等血红蛋白病中观察到的珠蛋白基因转换现象。
总体而言,EHA 2025展示的新研究加深了我们对正常和应激条件下微环境对造血干细胞(HSC)调控机制的理解,这为针对衰老和恶性微环境的治疗提供了新思路。
参考文献:
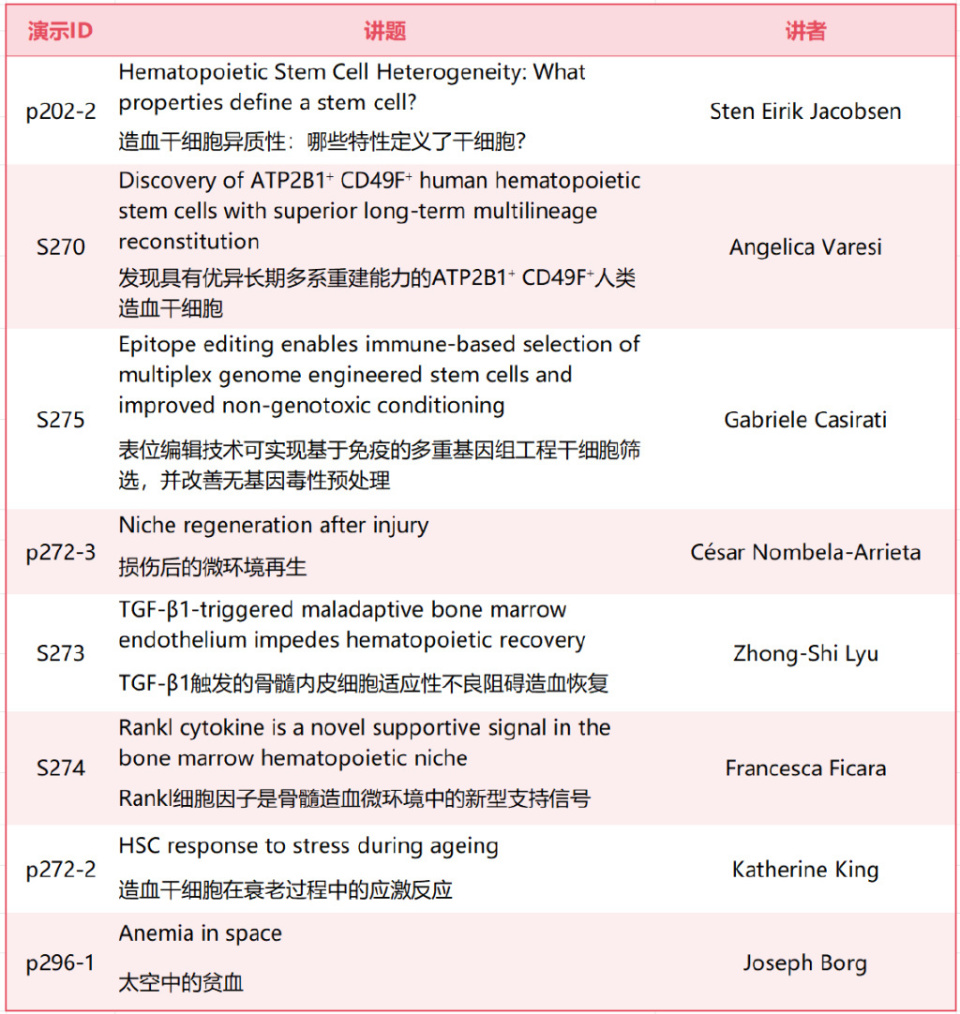
1. Jacobsen SE. Hematopoietic Stem Cell Heterogeneity: What properties define a stem cell? Oral presentation P202-2 at EHA2025.
2. Varesi A. Discovery of ATP2B1+ CD49F+ human hematopoietic stem cells with superior long-term multilineage reconstitution. Oral presentation S270 at EHA2025.
3. Casirati G. Epitope editing enables immune-based selection of multiplex genome engineered stem cells and improved non-genotoxic conditioning. Oral Abstract S275 at EHA2025.
4. Nombela-Arrieta C. Niche regeneration after injury. Oral presentation p272-3 at EHA2025.
5. Lyu ZS. TGF-?1-triggered maladaptive bone marrow endothelium impedes hematopoietic recovery. Oral presentation S273 at EHA2025.
6. Ficara F. RANKL cytokine is a novel supportive signal in the bone marrow hematopoietic niche. Oral abstract S274 at EHA2025.
7. King K. HSC response to stress during ageing. Oral presentation p272-2 at EHA2025.
8. Borg J. Anemia in space. Oral presentation p296-1 at EHA2025.