近日,EHA 2025大会报告(EHA Perspectives Congress Reports)正式发布,分为恶性血液学和非恶性血液学两大部分。报告全面梳理了大会期间公布的重大科研成果与临床进展,为全球血液学专业人士提供了深入了解领域前沿动态的权威参考。本期特别整理了恶性血液学报告中关于“AML的基因组学与新疗法”的专题内容,旨在为大家提供富有价值的临床与科研洞见。
精选演讲概览

超越传统诱导化疗(IC)和去甲基化药物(HMA)
在过去50年中,急性髓系白血病(AML)的诱导化疗方案几乎未发生显著变化,仍以“7+3”方案(阿糖胞苷+蒽环类药物)为主。尽管该方案可取得较高的完全缓解(CR)率,但长期生存率仍较差,尤其是在无法进行异基因造血干细胞移植(HSCT)的患者中[1]。因此,近年来研究重点逐步转向在“7+3”基础上引入新策略[2]。
Gemtuzumab ozogamicin(GO)是一种抗CD33抗体偶联药物(ADC),其细胞毒性部分源于calicheamicin。GO已被批准联合标准诱导化疗用于CD33阳性的初治AML患者[3]。在III期ALFA-0701试验中,GO联合柔红霉素和阿糖胞苷可显著改善无事件生存期(EFS),尤其在核心结合因子(CBF)AML中疗效显著[4]。
其他靶向治疗包括:FLT3抑制剂(如米哚妥林、奎扎替尼),用于FLT3突变AML[5];IDH1/2抑制剂(艾伏尼布、恩西地平),针对约20%携带IDH1/2突变的AML患者,目前正在与IC联合开展III期试验[6];BCL-2抑制剂维奈克拉,可阻断AML细胞的抗凋亡机制,与IC联合用于初治和复发/难治AML,复合完全缓解(cCR)率高达95%[7]。总体而言,将靶向治疗纳入适合强化化疗的初诊AML成年患者的一线治疗中展现出良好前景,该治疗格局仍将持续演进。
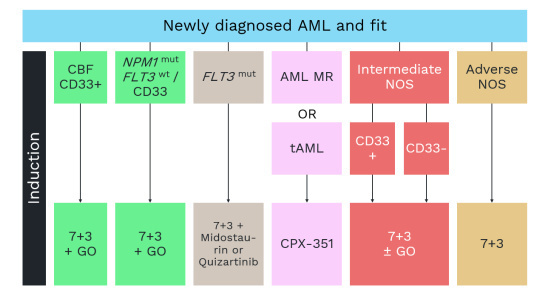
对于不适合IC的初治AML患者,目前标准治疗为去甲基化药物(HMA,阿扎胞苷或地西他滨)联合维奈克拉,尽管该组合在总生存(OS)方面不如IC[8]。IDH1抑制剂艾伏尼布联合阿扎胞苷在IDH1突变AML中也展现出鼓舞人心的早期疗效[9],但目前仍需在携带高风险基因突变(如TP53、FLT3、RAS)患者中进一步优化疗效[10]。VIALE-A研究确立了维奈克拉联合阿扎胞苷作为老年或unfit AML患者中的新标准方案。真实世界数据也进一步支持该方案对改善生活质量的临床价值[11]。
全口服地西他滨-西达尿苷联合维奈克拉用于老年AML患者
由于住院治疗对老年患者负担较大,ASCERTAIN-V(NCT04975919)1/2期试验在中位年龄超过75岁、且不适合接受强化化疗(IC)的AML患者中,评估了全口服地西他滨-西达尿苷(DEC-C)联合维奈克拉(Ven)的治疗方案。所有患者在第1个周期完成Ven剂量递增后,并于每个周期(28天为一个治疗周期)的第1-5天接受口服DEC-C以及每日服用400 mg的Ven。
Gail Roboz博士在EHA 2025大会上公布了该研究结果:在1期(n=30)、2A期(n=58)和2B期(n=101)中,完全缓解(CR)率分别为40.0%、37.9%和46.5%[12]。在2B期中位随访11.2个月后,观察到的中位总生存期(OS)为15.5个月。共44名获得CR的患者接受了微小残留病(MRD)检测,其中55.1%(n=27)曾在某一时间点实现MRD阴性。MRD阴性者的中位OS尚未达到(NE),而MRD阳性者的中位OS为15.5个月。
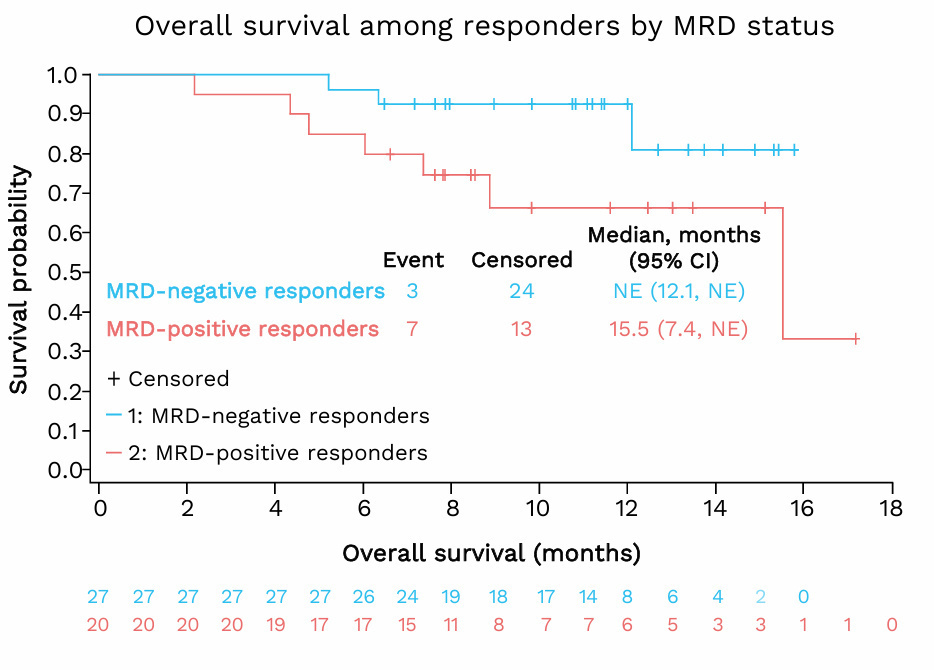
安全性方面,1期、2A期和2B期中分别有86.7%、91.4%和98.0%的患者出现3级或以上不良事件,最常见的严重不良事件与骨髓抑制相关,包括贫血(25.9%)、中性粒细胞减少(20.6%)、发热性中性粒细胞减少(20.6%)和血小板减少(14.3%)。由于Ven联合阿扎胞苷常导致中性粒细胞减少和治疗相关性骨髓抑制,该研究也对剂量调整进行了分析。在1期、2A期和2B期中,患者完成的治疗周期中位数分别为4、5和4个。观察到接受骨髓检查的比例从1期的3.3%增加至2A期的15.5%,再至2B期的31.7%。
研究者认为,全口服DEC-C+Ven方案在不适合IC治疗的新诊断老年AML患者中,其安全性、缓解率和生存数据与注射用阿扎胞苷+Ven治疗方案相当。与标准剂量治疗相比,在缓解后治疗周期中早期进行骨髓检查并相应调整DEC-C和/或Ven剂量,有助于提高长期疗效和耐受性。目前,该治疗方案已进入大规模3期临床试验阶段。
肿瘤异质性与克隆选择
治疗后的复发与肿瘤异质性和克隆选择密切相关。在复发性和难治性(R/R)患者中,携带有不同抗药机制的AML克隆可能在下一次治疗开始前就已经存在。单细胞多组学技术在识别休眠干细胞样细胞和白血病干细胞方面发挥了重要作用,这些细胞是治疗耐药性和治疗后复发的根本原因[13]。
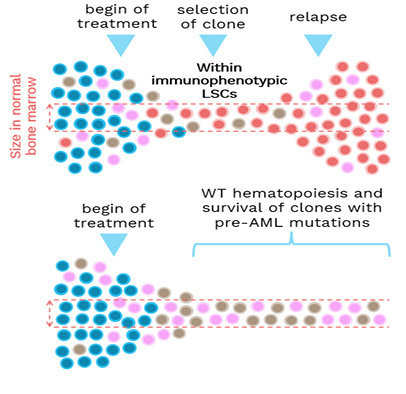
通过单细胞RNA测序对AML患者骨髓样本进行克隆演化监测,观察克隆间基因表达的变化,并将其与克隆随时间变化的显性位点相关联。研究发现,耐药克隆可能会发生基因突变演化,但并非一定如此。最终导致复发的克隆通常从一开始就存在。
在长期缓解的患者中,治疗后观察到正常造血功能和仅携带AML前突变的克隆。如果能通过可扩展、具有成本效益的技术,如单细胞技术,早期检测到克隆选择,许多复发可能是可预防的。
联合治疗对抗肿瘤耐药机制
在接受维奈克拉联合治疗的AML患者中,复发可能通过多种机制发生,包括BCL2家族蛋白、FLT3、RAS和MAPK的上调或突变、新的TP53突变,以及单核细胞克隆的扩展等因素。因此,已有几种新药获批或正在开发,旨在针对这些问题。为了实现更持久和有效的缓解,可能需要个性化、针对特定异常的患者特异性联合治疗,这也有助于减少维奈克拉单药治疗的原发性和继发性耐药。
Menin抑制剂作为AML的联合治疗
Menin抑制剂是目前临床研发中的新型且具有前景的药物,其靶向HOX/MEIS1转录程序,这一程序对于KMT2A重排(KMT2A-r)和NPM1突变(NPM1-m)AML的白血病发生至关重要。当前正在为AML开发的Menin抑制剂包括revumenib、ziftomenib、bleximenib、BMF-219和DSP-5336,其中revumenib的临床开发进展最为迅速[14]。
在2025 EHA大会上,几种Menin抑制剂的新数据得到了展示。Harry Erba博士介绍了KOMET-007剂量递增试验的结果,该试验在82例NPM1-m和KMT2A-r AML患者中,评估了每日600 mg ziftomenib与7+3诱导化疗或维奈克拉/阿扎胞苷(ven/aza)的联合应用(NCT05735184)[15]。该联合方案的安全性与单独使用7+3方案相似,且获得了更高的缓解率,包括持久缓解。
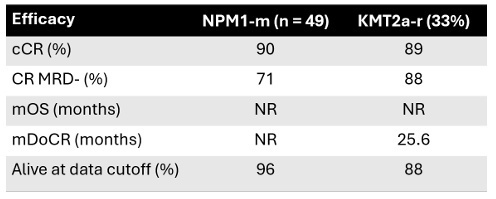
另一篇摘要介绍了bleximenib(JNJ-75276617)的数据,该药物也在一项Ib 期临床试验 (NCT04811560) 中进行了测试,其与ven/aza联合治疗新诊断和复发或难治性AML,且伴有 KMT2A/NPM1基因变异[16]。在推荐剂量(RP2D)为100 mg每日两次时,bleximenib联合治疗在复发/难治性AML患者中达到了82%的总缓解率(ORR)和59%的完全临床缓解(cCR)率。在新诊断患者群体中,ORR为 90%,cCR率为75%。3级或以上的事件主要集中在骨髓抑制,如中性粒细胞减少。
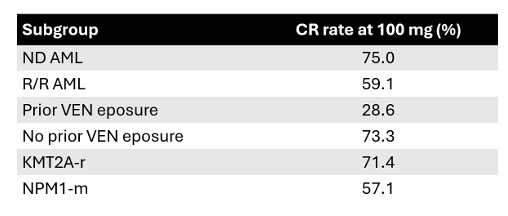
最后,Joshua Zeidner博士介绍了BEAT AML主试验(BAMT)的子研究。一项剂量递增和扩展试验 (NCT06652438) 也对revumenib与ven/aza 联合治疗进行了测试,该试验仅针对新诊断的AML患者[17]。43名NPM1-m或KMT2A-r的患者接受了两种剂量的revumenib(113 mg和163 mg)联合治疗,口服每日两次。未确定最大耐受剂量(MTD),且没有患者因不良事件中止revumenib治疗。疗效与其他Menin联合治疗一致。
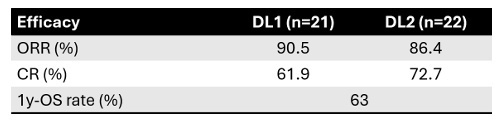
总体而言,Menin抑制剂是KMT2A-r和NPM1突变AML的有前景的新型治疗方法。正在进行的临床试验的早期结果在缓解率和安全性方面令人鼓舞,尤其是对于那些已接受过大量治疗的患者。然而,仍需更多的研究来确认这些发现,识别可能从这些治疗中获益的患者亚群,并确定这些新药物的最佳使用时机和剂量。此外,Menin抑制剂与其他药物如venetoclax和azacitidine的联合使用,增强了两类药物的疗效,可能改善KMT2A-r和NPM1突变AML患者的治疗效果,特别是在老年患者和R/R AML患者中。
地西他滨、维奈克拉和奎扎替尼三联疗法治疗FLT3-ITD突变AML
FMS样酪氨酸激酶3(FLT3)是一种酪氨酸激酶受体,在造血细胞存活、增殖和分化中起着至关重要的作用。20%-30%的AML患者会出现FLT3突变,这通常提示治疗效果不佳。奎扎替尼是一种二代FLT3抑制剂,目前正在进行III期临床试验。临床前数据表明,奎扎替尼和维奈克拉可能具有协同作用。因此,启动了一项I/II期临床试验,以确定奎扎替尼联合地西他滨和维奈克拉治疗FLT3突变AML患者的推荐剂量(RP2D),包括新诊断(ND)和复发/难治性(R/R)患者,且这些患者不适合接受强化化疗(IC)。
Musa Yilmaz博士展示了30 mg剂量的奎扎替尼未出现剂量限制性毒性,在ND(94%)和R/R(61%)患者中均观察到较高的缓解率[18]。ND患者在中位随访17个月后,尚未达到中位总生存期(OS),且1年OS率为72%。在R/R患者中,中位OS为6.3个月,1年OS率为20%。在安全性方面,中性粒细胞的延迟恢复可通过将维奈克拉和奎扎替尼的给药时间缩短至14天来缓解,3级QTcF延长较为罕见(4%)。
地西他滨、维奈克拉和奎扎替尼的联合治疗在高风险患者中显示出良好的疗效,但仍需更多数据来进一步了解该三联疗法在AML患者一线治疗和复发/难治性治疗中的应用。
Sonrotoclax在初治及R/R AML中的治疗
维奈克拉是治疗包括AML在内多种血液肿瘤的突破性药物。然而,随着治疗的持续,肿瘤细胞可能会发展出对维奈克拉的耐药机制。Sonrotoclax是新一代BCL-2抑制剂,具有更高的选择性和效力,能够抑制野生型和G101V突变型BCL-2[19]。
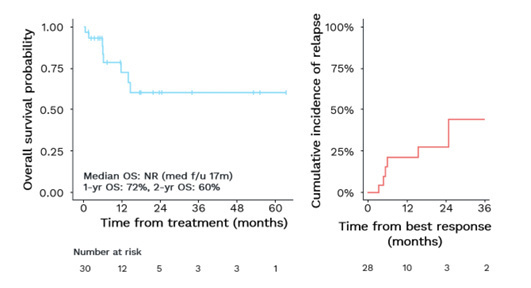
在2025 EHA大会上,研究人员展示了关于Sonrotoclax联合阿扎胞苷治疗初治及R/R MDS和AML患者的海报摘要[20]。在这项Ib/II期剂量递增和扩展试验(BGB 11417-103)中,测试了多个Sonrotoclax给药方案,剂量从40 mg至320 mg不等,疗程为10至28天,28天为一个周期。所有剂量方案的总体缓解率为75%,其中初治患者的完全缓解(CR)率为60%,R/R患者的CR率为43%。与骨髓抑制相关的不良事件频繁发生,90%的初治患者和84%的R/R患者出现了≥3级的中性粒细胞减少。总体而言,15.2%和11.8%的患者中止了治疗。
考虑到研究中纳入的高风险患者,研究人员得出结论,Sonrotoclax与阿扎胞苷联合治疗在初治和R/R患者中均显示出有效性,并且具有可接受的安全性。
总之,EHA 2025为AML治疗的前沿治疗方法提供了宝贵的见解。这些方法包括探索当前诱导化疗和去甲基化药物的替代治疗方案,以及基于肿瘤独特特征测试更有效的治疗组合。对肿瘤异质性和克隆选择的更深入理解,是开发AML复发后治疗的基础,也为探索联合治疗和预防耐药新策略提供了思路。大会还展示了针对老年及不适合强化治疗患者的全口服治疗方案的新数据,以及Menin抑制剂与标准治疗联合使用的早期临床试验结果。此外,三联疗法和Sonrotoclax疗法的数据为AML治疗的未来带来了希望,强调需要以安全有效的方式优化其使用,以进一步改善患者预后。
参考文献:
[1]Büchner T, et al. Acute Myeloid Leukemia (AML): different treatment strategies versus a common standard arm--combined prospective analysis by the German AML Intergroup. J Clin Oncol. 2012;30(29):3604-3610.
[2]Röllig C. Beyond 3 plus 7. Oral presentation p126-1 at EHA2025.
[3]Döhner H, et al. Diagnosis and management of AML in adults: 2022 recommendations from an international expert panel on behalf of the ELN. Blood. 2022;140(12):1345 1377.
[4]Lambert J, et al. Gemtuzumab ozogamicin for de novo acute myeloid leukemia: final efficacy and safety updates from the open-label, Phase III ALFA-0701 trial. Haematologica. 2019;104(1):113-119.
[5]Erba HP, et al. Quizartinib plus chemotherapy in newly diagnosed patients with FLT3-internal-tandem duplication-positive acute myeloid leukaemia (QuANTUM-First): a randomised, double-blind, placebo controlled, Phase 3 trial. Lancet. 2023;401(10388):1571-1583.
[6]A Study of Ivosidenib or Enasidenib in Combination With Induction Therapy and Consolidation Therapy, Followed by Maintenance Therapy in Patients With Newly Diagnosed Acute Myeloid Leukemia or Myedysplastic Syndrome EB2, With an IDH1 or IDH2 Mutation, Respectively, Eligible for Intensive Chemotherapy (HOVON150AML). ClinicalTrials.gov ID NCT03839771. Last Accessed 1st July 2025. www. clinicaltrials.gov/study/ NCT03839771.
[7]DiNardo CD, et al. Long term results of venetoclax combined with FLAG IDA induction and consolidation for newly diagnosed and relapsed or refractory acute myeloid leukemia. Leukemia. 2025;39(4):854-863.
[8]Cherry EM, et al. Venetoclax and azacitidine compared with induction chemotherapy for newly diagnosed patients with acute myeloid leukemia. Blood Adv. 2021;5(24):5565 5573.
[9]Montesinos P, et al. Ivosidenib and Azacitidine in IDH1-Mutated Acute Myeloid Leukemia. 2022;386(16):1519-1531 NEJM. 2022;386(16):1519-1531
[10]DiNardo C. Beyond HMA+venetoclax. Oral presentation p126-2 at EHA2025.
[11]Gangat N et Tefferi A. Venetoclax in the treatment of acute myeloid leukemia: Beyond VIALE-A. Am J Hematol. 2024;99:515–518.
[12]Roboz G. All-oral decitabine cedazuridine (DEC-C) + venetoclax (VEN) in ND AML patients: Phase 1/2 clinical trial results. Oral presentation s135 at EHA2025.
[13]Vyas P. New combination therapies. Oral presentation p250-3 at EHA2025.
[14]Candoni A, Coppola G. A 2024 Update on Menin Inhibitors. A New Class of Target Agents against KMT2A Rearranged and NPM1-Mutated Acute Myeloid Leukemia. Hematol Rep. 2024;16(2):244-254.
[15]Erba H. Ziftomenib combined with intensive induction chemotherapy (7+3) in newly diagnosed NPM1-M or KMT2A-r acute myeloid leukemia (AML): Updated Phase 1a/b results from KOMET-007. Oral presentation S136 at EHA2025.
[16]Wei AH. RP2D determination of bleximenib in combination with VEN+AZA: phase 1b study in nd & r/r aml with KMT2A/NPM1 alterations. Abstract s137 at EHA2025.
[17]Zeidner J. Azacitidine, venetoclax, and revumenib for newly diagnosed older adults with acute myeloid leukemia (AML) and NPM1 mutation or KMT2A Rearrangement: updated results from the Beat AML consortium. Oral presentation s138 at EHA2025.
[18]Yilmaz N. Phase I/II study of decitabine, venetoclax, and quizartinib triplet combination in FLT3-ITD mutated AML. Abstract S142 presented at EHA2025.
[19]Yunhang G, et al. Discovery of the Clinical Candidate Sonrotoclax (BGB 11417), a Highly Potent and Selective Inhibitor for Both WT and G101V Mutant Bcl-2. J Med Chem. 2024;67(10):7836-7858.
[20]Montesinos P. Updated safety and antileukemic activity data for sonrotoclax (BGB-11417), a potent and selective BCL2 inhibitor, in patients with relapsed/refractory acute myeloid leukemia. PF491 at EHA2025.