第30届欧洲血液学会年会(EHA 2025)于6月12日至15日在意大利米兰盛大召开,汇聚全球血液学领域的最新研究成果与前沿进展。在本次大会上,中国医学科学院血液病医院(中国医学科学院血液学研究所)竺晓凡教授团队的口头报告(S170)引发关注。该研究首次构建了儿童NRAS突变型髓系肿瘤的单细胞图谱,揭示其髓系谱系偏倚机制,并锁定CDK6等关键靶点,为“不可成药”NRAS突变提供新解。《肿瘤瞭望-血液时讯》现场特邀竺晓凡教授接受采访,深度解析研究亮点与转化前景,并分享本届大会儿童血液病治疗领域的多项重磅进展。
《肿瘤瞭望-血液时讯》NRAS突变存在于多种髓系肿瘤中,但却引发不同疾病表型。您团队本次研究结合人源与小鼠模型,揭示了哪些关键的分化偏向机制?这一机制在JMML与MDS之间有何异同?
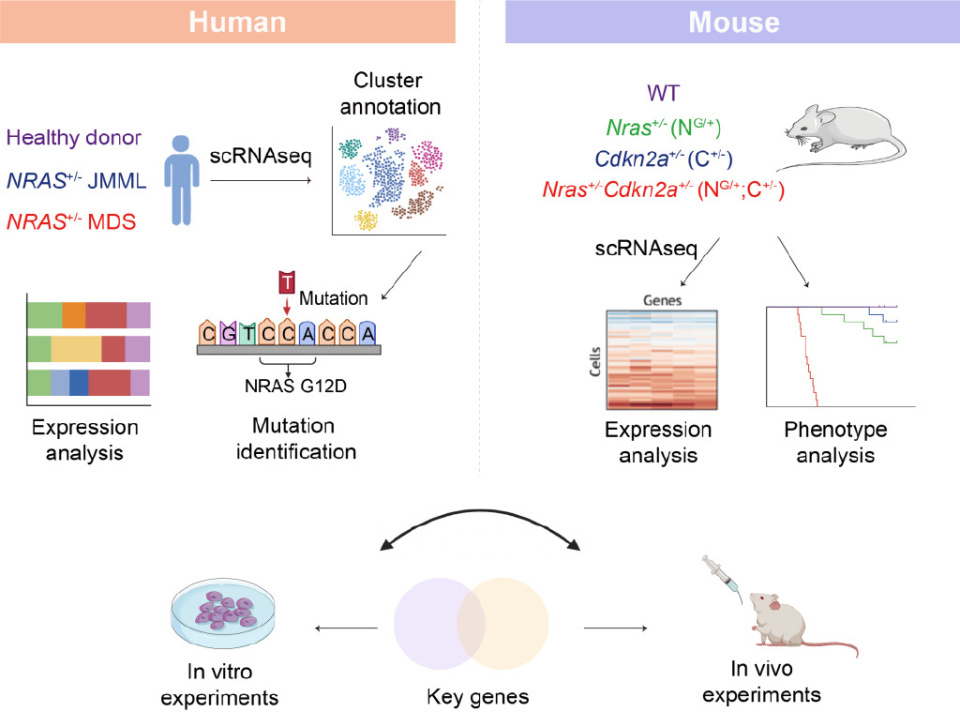
竺晓凡教授:NRAS突变广泛存在于多种儿童髓系肿瘤中,包括幼年型粒单核细胞白血病(JMML)和骨髓增生异常综合征(MDS),但其生物学行为和临床表现却显著不同。为阐明“同一突变导致不同疾病”的机制,我们团队结合了患者来源的单细胞组学分析和小鼠功能模型,进行了系统比较。
研究发现,虽然JMML和MDS均携带NRAS突变,但其起源细胞亚群存在差异,导致了不同的分化轨迹。JMML中的突变细胞从造血干细胞(HSC)到多种祖细胞(GMP、CLP等)均有广泛分布,呈现出较强的扩散性增殖特征;而MDS中的突变细胞主要集中在LMprog(髓淋祖细胞)阶段,在此阶段出现了明显的分化阻滞和功能重塑。
进一步的单细胞ATAC-seq和RNA-seq联合分析揭示,MDS中LMprog细胞的染色质开放度显著增加,并激活了包括RUNX1、CEBPA和HIF1A在内的关键髓系转录因子,驱动异常髓系偏向,并上调CDK6等促增殖因子。相较之下,JMML则缺乏这种显著的表观重塑。
这项研究首次从单细胞层面揭示了NRAS突变在不同髓系肿瘤中的“谱系特异性分化偏向机制”,为理解其致病多样性提供了重要线索。
《肿瘤瞭望-血液时讯》此次研究构建了儿童NRAS突变型髓系肿瘤的单细胞图谱,并锁定了如FLT3、CDK6等多个潜在靶点。请问在众多候选靶点中,哪些最具转化潜力?是否已进入后续临床前或药物筛选阶段?
竺晓凡教授:在构建了完整的NRAS突变型髓系肿瘤单细胞图谱后,我们识别出多个潜在治疗靶点,其中CDK6最具转化潜力。
CDK6不仅在MDS患者中显著上调,还显示出对突变细胞的功能依赖性:NRAS突变驱动的MDS细胞在LMprog阶段高度依赖CDK6维持其分化阻滞和增殖状态。我们通过CDK6抑制剂Palbociclib的体内外实验验证,无论是在患者来源的造血干细胞、NRAS突变小鼠模型,还是MDS的PDX模型中,均观察到显著的分化恢复、细胞凋亡增加和白血病起始细胞的耗竭,进一步确认了CDK6作为治疗靶点的功能价值。
目前,Palbociclib在小鼠模型中的系统评估已完成,显示出良好的安全性和抗肿瘤活性。下一阶段,我们将围绕CDK6进行联合用药筛选,探索其与化疗或免疫疗法的协同效果。
《肿瘤瞭望-血液时讯》NRAS长期被视为“不可成药”靶点,您的研究从髓系谱系偏向和信号通路失衡角度寻找突破口。未来,您如何规划将这一图谱研究成果进一步推进至儿童高危髓系肿瘤的临床精准治疗中?
竺晓凡教授:NRAS“不可成药性”确实是该研究领域的重大障碍。我们团队绕开直接靶向NRAS的难点,转而聚焦于其下游的功能依赖环节,特别是CDK6介导的髓系偏向和分化阻滞。未来,我们的研究成果将从以下三个层面进行加速转化:
第一,基于单细胞图谱构建儿童髓系肿瘤的分子分型体系,助力NRAS突变疾病的精准风险分层和个体化治疗策略的制定。
第二,开发基于CDK6的联合靶向治疗方案。通过临床前药物筛选,评估CDK6抑制剂与现有疗法(如低剂量化疗、去甲基化药物、免疫治疗)的协同潜力,以优化治疗方案。
第三,推动CDK6靶向治疗策略进入早期临床验证。我们已在筹备相关的临床试验,以评估CDK6抑制剂在难治性NRAS突变型儿童MDS中的安全性和初步疗效。
我们相信,从“不可成药”到“精准打击”,以功能依赖为核心的新靶点策略,有望为NRAS突变相关的儿童高危髓系肿瘤带来突破性治疗新机遇。
《肿瘤瞭望-血液时讯》最后,请您分享下本次来到EHA大会现场的感受,在儿童血液疾病治疗领域还有哪些令您印象深刻的突破性进展或研究成果?
竺晓凡教授:本次来到EHA大会现场,我深刻感受到国际学术界对儿童血液病研究的高度重视,现场氛围热烈,学术交流充分,给我留下了深刻印象。在儿童血液疾病治疗领域,今年的大会展示了多项令人振奋的突破性进展。
首先,在复发/难治性FLT3-ITD突变的AML儿童患者中,gilteritinib联合化疗的I/II期临床试验显示了良好的生物活性和安全性,使部分患者顺利进入造血干细胞移植阶段。这为这一高风险人群带来了新的治疗希望。
其次,对于携带KMT2A基因重排的AML儿童患者,异基因造血干细胞移植(allo-HSCT)联合Menin抑制剂取得了令人瞩目的长期生存率(3年总生存率超80%),尤其是在达到完全缓解后移植的患儿中显著降低了复发风险。这进一步巩固了HSCT在KMT2A-r AML中的核心地位。
最后,CALGB 10403方案对青少年和年轻成人(AYA)ALL患者的10年随访结果首次公布,整体生存率超过50%,MRD阴性患者的预后尤为理想(DFS和OS均超过80%)。这一结果凸显了早期清除MRD及完成维持治疗对于长期生存的重要性。
总之,这些研究不仅为临床实践提供了新的证据,也为未来儿童血液病治疗的发展提供了新的思路。
特别鸣谢
宗苏玉:在中国医学科学院血液病医院(中国医学科学院血液学研究所)儿童血液与肿瘤诊疗中心全体人员的努力下,本研究才得以顺利完成。在此特别感谢张英驰教授、竺晓凡教授、杨文钰教授的指导,以及Zhu /Zhang实验室Tianyuan Hu、Xiaoli Chen、Peng Wu、Yunlong Chen、Yongjuan Duan、Jingliao Zhang、Jiarui Zheng、Linlin Jing、Yuxin Huang的大力支持。

专家简介

竺晓凡 教授
中国医学科学院血液病医院(中国医学科学院血液学研究所)临床首席专家
主任医师,博士研究生导师
国务院特殊津贴专家
天津市有突出贡献专家
国家卫生健康委儿童白血病专家委员会副主任委员
中国抗癌协会小儿肿瘤专业委员会候任主任委员
中国抗癌协会儿童癌症协作组CCCG-2025-ALL PI
中国临床肿瘤学会(CSCO)淋巴瘤专委会委员
《中华儿科杂志》、《中华血液学杂志》等杂志编委
获国家自然科学二等奖、宋庆龄儿科医学奖、五洲女子科技奖、天津市自然科学一等奖等奖项