第30届欧洲血液学会年会(EHA 2025)于6月12日至15日在意大利米兰盛大召开。作为全球顶尖的血液学盛会之一,本次大会聚焦血液学各亚专科领域的最新进展,展示前沿的循证诊断和治疗方法,发布临床与转化研究的最新数据,并呈现创新技术、诊断工具及风险评估策略的成果。在本届大会上,上海交通大学医学院附属仁济医院侯健教授团队的一项研究入选大会口头报告(S188),揭示了非编码增强子型eccDNA在多发性骨髓瘤耐药中的关键作用,为探索新的治疗靶点提供了重要依据。《肿瘤瞭望-血液时讯》现场特邀侯健教授深入解读该研究。
《肿瘤瞭望-血液时讯》在本次大会上,您团队的一项研究入选口头报告,揭示了eccANKRD28这一非编码增强子型eccDNA在多发性骨髓瘤中的耐药机制。请问,这一发现意味着什么?它会如何改变我们对骨髓瘤治疗的理解?
侯健教授:多发性骨髓瘤目前仍是一种无法治愈的疾病,其难治性主要体现在患者经多次治疗后,体内骨髓瘤细胞逐渐对现有疗法产生耐药性,而耐药的形成机制极为复杂。
我们的研究从染色体外DNA这一创新角度出发,揭示了其在耐药过程中所起的作用。染色体外DNA是在细胞DNA受损时从染色体上脱落的片段。过去这些脱落的DNA被认为是没有功能的,但我们的研究发现,它们实际上具有增强子活性,能够调控肿瘤细胞的转录激活,进而影响其代谢,最终导致耐药。这一发现为理解骨髓瘤细胞对化疗药物及靶向药物(如来那度胺、硼替佐米)的耐药机制提供了全新的视角,展现了显著的创新性。
《肿瘤瞭望-血液时讯》eccANKRD28在诊断时的拷贝数与患者的预后及生物标志物密切相关。您认为eccANKRD28未来是否有望作为临床“液体活检”的新型指标,用于风险分层或治疗监测?目前还面临哪些技术瓶颈?
侯健教授:染色体外环状DNA(eccDNA)是细胞DNA损伤时从染色体上脱落下来的片段。正常细胞中也有一定eccDNA的存在,但与正常细胞相比,骨髓瘤细胞能产生大量且特异性的eccDNA。在我们的研究中,我们发现eccDNA ANKRD28在肿瘤细胞与正常浆细胞中的含量存在显著差异。因此其有望作为肿瘤耐药的生物标志物。当然,这一设想还需通过大量临床样本的进一步验证。
《肿瘤瞭望-血液时讯》在本项研究中,您整合了多组学技术(如Circle-seq、scATAC-seq、CUT&Tag等)。在具体研究过程中,这种多维度联合分析为识别功能性非编码eccDNA提供了哪些独特优势?
侯健教授:多组学技术,包括基因组学、蛋白组学等,以其高通量和多维度的特点,为我们研究 eccDNA ANKRD28 的作用提供了强大支持。我们综合利用这些先进技术,从多个角度对 eccDNA ANKRD28在骨髓瘤细胞对硼替佐米和来那度胺耐药中的作用进行了深入分析。这种多维度的研究方法,不仅丰富了我们对eccDNA ANKRD28功能的理解,还为证实其在肿瘤细胞耐药机制中的关键角色提供了确凿证据。
《肿瘤瞭望-血液时讯》鉴于eccANKRD28可通过CRISPR调控影响治疗敏感性,您是否考虑将这一通路作为潜在靶点进行干预?针对该机制的药物开发或基因编辑策略目前处于怎样的探索阶段?
侯健教授:通过细胞培养、多组学筛选和动物实验等前期研究,我们证实了eccDNA ANKRD28在骨髓瘤细胞耐药中作为增强子发挥着重要作用。这一发现为未来通过靶向干预逆转多发性骨髓瘤耐药提供了初步证据。目前,我们团队正在进一步研究,旨在将这些初步的实验成果逐步转化为临床应用,为广大患者带来福音。
研究简介
摘要号:S188
标题:ENHANCER EXTRACHROMOSOMAL CIRCULAR DNA ANKRD28 DRIVES DRUG RESISTANCE VIA POU2F2-MEDIATED TRANSCRIPTIONAL REWIRING IN MULTIPLE MYELOMA
中文标题:增强子染色体外环状DNA ANKRD28通过POU2F2介导的转录重编程驱动多发性骨髓瘤的药物耐药
第一作者:Binzhen Chen
通讯作者:侯健
研究背景
多发性骨髓瘤(MM)仍是一种无法治愈的疾病,这主要是由于药物耐药性的出现,而其潜在机制尚不明确。异常的增强子活性在调节基因表达程序中发挥关键作用,这些程序有助于肿瘤的起始、维持、进展和治疗耐药性。染色体外环状DNA(eccDNA)在编码和非编码区域的癌症基因组中普遍存在,其对下游癌基因和/或治疗耐药性基因的扩增推动了肿瘤内表观遗传异质性。然而,作为增强子的非编码 eccDNA 区域的作用大多被忽视。
研究目的
本研究旨在探讨增强子染色体外环状DNA ANKRD28(eccANKRD28)在多发性骨髓瘤(MM)的药物耐药性和疾病进展中的作用。
研究方法
我们对来自供体和对硼替佐米/来那度胺/地塞米松(VRd)治疗反应良好(高敏感性,HS)或较差(低敏感性,LS)的新诊断多发性骨髓瘤(NDMM)患者的血清样本进行了 Circle-seq 和 RNA-seq 分析。鉴于血清eccDNA核心区域完全为非编码区域,我们通过整合增强子图谱(H3K27ac ChIP-seq)、单细胞转录组(scRNA-seq)、染色质可及性(scATAC-seq)数据集以及转录因子靶标筛选(CUT&Tag),映射了活性调控元件。通过对这些数据集的综合分析,我们识别了增强子eccDNA、eccDNA活性所需的关键转录因子(TFs)以及与已知癌基因相关的下游调控网络。我们还应用了多发性骨髓瘤异种移植NSG小鼠模型,以验证内源性eccDNA 操控的MM细胞在体内的功能。
研究结果
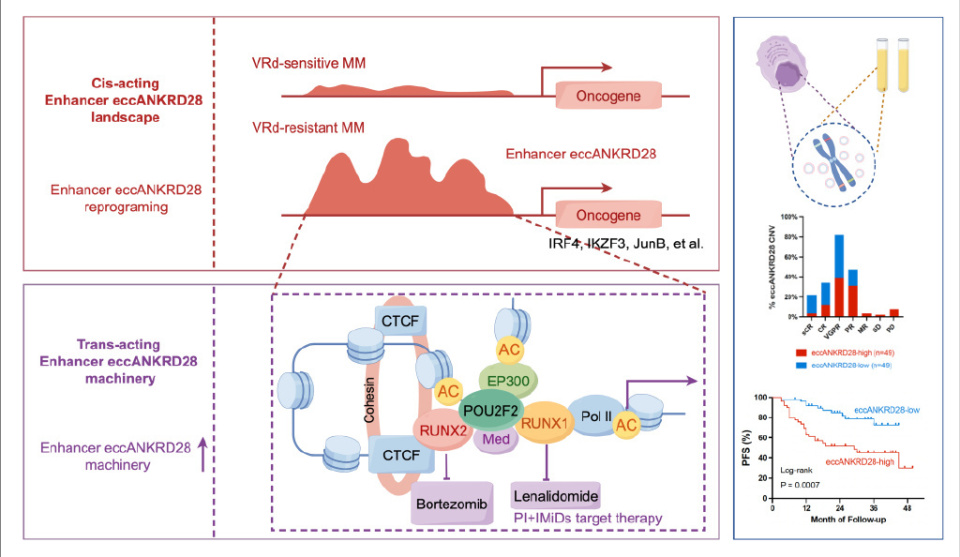
我们描绘了eccDNA的全基因组图谱,并鉴定出具有预后和治疗效果预测价值的 eccANKRD28。我们进一步评估了98例NDMM患者和10例供体的eccANKRD28拷贝数,发现诊断时eccANKRD28拷贝数高的患者无进展生存期(PFS)显著较差(中位PFS 29个月 vs. 尚未达到,HR 3.14,95%CI:1.64-5.99,P=0.0007)。eccANKRD28拷贝数与参与/未参与的游离轻链比率[FLCR(i/ u)](P=1.0e-9,r=0.62,n=80)、β2-MG(P=0.04,r=0.24,n=78)以及骨髓浆细胞百分比(BMPC%)(P= 2.6e-14,r= 0.79,n=61)呈正相关。已建立的VRd耐药RPMI-8226、U266 和OPM-2细胞系显示出更高丰度的eccANKRD28以及增强的转录活性,CRISPR/Cas9介导的eccANKRD28升高在体内外均降低了硼替佐米和来那度胺治疗的敏感性。综合多组学分析(H3K27ac ChIP-seq、scRNA-seq、scATAC-seq、CUT&Tag等)识别出 eccANKRD28作为一种由关键转录因子POU class 2 homeobox 2(POU2F2)驱动药物耐药性的活性增强子。POU2F2与序列特异性的eccANKRD28以及RUNX1和RUNX2模序相互作用形成蛋白质复合物,激活包括IRF4、JUNB、IKZF3、RUNX3和BCL2在内的癌基因的启动子。
研究结论
我们的研究结果表明,增强子eccANKRD28通过POU2F2介导的转录级联反应诱导药物耐药性,并进一步加速多发性骨髓瘤的进展。
专家简介

侯健 教授
上海交通大学医学院附属仁济医院主任医师
国际骨髓瘤工作组(IMWG)委员
中华医学会血液学分会常委
中国抗癌协会血液肿瘤专委会常委
中国医师协会血液科分会常委、肿瘤科分会委员
中国淋巴瘤联盟常委
中国病理生理学会实验血液学分会委员
中国免疫学会血液免疫分会常委
上海市免疫学会血液免疫专委会主委
上海医学会血液学分会主委
中国医药创新促进会药物临床研究专委会副主委