靶向及免疫治疗的新进展已显著改善了套细胞淋巴瘤(MCL)尤其是难治/复发患者的治疗前景。就一线方案而言,纳入新型药物的策略正被积极研究。在适合移植的年轻患者中,含伊布替尼的免疫化疗诱导后序贯自体造血干细胞移植(ASCT)已显示出优于单纯化疗±ASCT的疗效,故将伊布替尼纳入年轻MCL患者的一线治疗已成为新的标准。对于高龄、不适合大剂量化疗及ASCT的群体,多项研究探索了靶向药物联合免疫化疗或单药±其他靶向方案,结果令人鼓舞。德国慕尼黑大学附属医院的E. Silkenstedt教授与M. Dreyling教授综述了当前MCL一线治疗标准,重点阐述了靶向策略,特别是BTK抑制剂(BTKi)在初始治疗中的整合。
01、引言
套细胞淋巴瘤(MCL)临床特征具有高度异质性,病程可从惰性(数年内无需治疗)至高度侵袭性(预后极差)不等。患者通常表现为多部位淋巴结肿大,多数确诊时已处于晚期(Ann Arbor III-IV期)。90%的患者存在结外浸润,包括骨髓(53%~82%)、血液(50%)、肝脏(25%)及胃肠道(20%~60%),40%伴脾肿大。部分病例以白血病形式表现,并伴显著脾大,此类非结节性白血病亚型常呈惰性病程。
根据世界卫生组织(WHO)淋巴瘤分类更新,MCL分为两类:结节性MCL(80%~90%)以未突变免疫球蛋白重链可变区基因(IGHV)、SOX11过表达及侵袭性临床行为为特征;非结节性白血病MCL(10%~20%)则多见IGHV突变、SOX11阴性及惰性病程。组织学上,除经典型外,还可见多形性及母细胞样变型,后者因高增殖活性(Ki-67指数升高)常提示更差预后。
传统上,MCL预后较差,中位总生存期(OS)仅3~5年。但近年来,治疗领域取得重大进展,显著改善了患者生存状况。
02、一线治疗策略
MCL临床病程特点为初始缓解率高,但早期复发常见,多数患者呈现侵袭性进程。然而,10%~15%患者为惰性亚型,此类病例多表现为非结节性白血病形式或Ki-67指数极低(<10%),观察等待策略结合密切监测被视为合理选择。但多数患者仍需早期干预,尽管晚期(III-IV期)疾病仍被视为不可治愈。
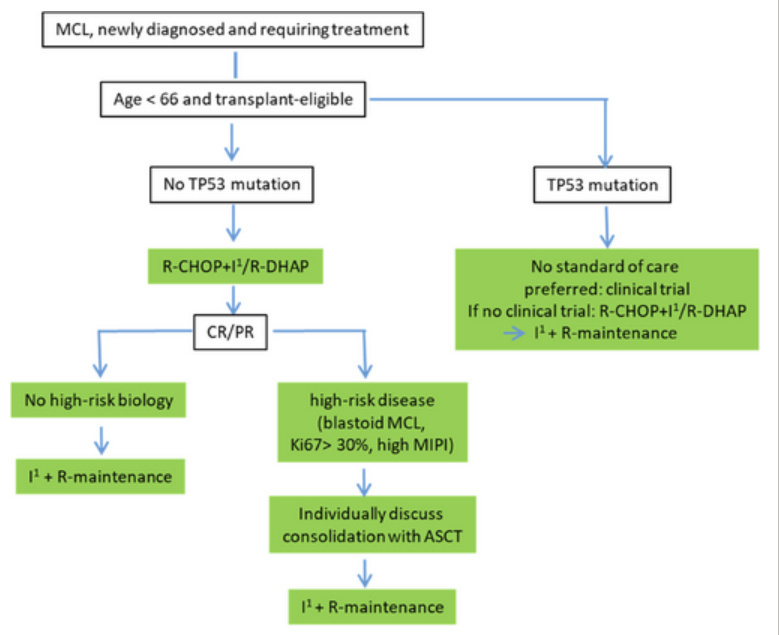 治疗策略
治疗策略
1、年轻患者(≤65岁)的一线治疗
多项研究证实,年轻且体能状态良好的患者(≤65岁)采用含大剂量化疗的免疫化疗诱导方案联合ASCT巩固可获得长期缓解,该策略曾被视为标准治疗。例如,欧洲MCL网络开展的III期试验(MCL Younger)显示,R-CHOP/DHAP方案序贯ASCT较单纯R-CHOP后ASCT使治疗失败时间(TTF)延长超一倍(109个月 vs. 47个月)。另一项大型随机试验证实,ASCT巩固可显著延长无进展生存期(PFS)(3.3年 vs. 1.5年)及总生存期(OS)。北欧MCL2研究的15年更新数据进一步支持此结论:接受交替R-maxi-CHOP(剂量强化利妥昔单抗联合环磷酰胺、多柔比星、长春新碱和泼尼松)及大剂量阿糖胞苷(HIDAC)诱导后ASCT巩固的患者(<66岁),中位OS和PFS分别达12.7年及8.5年。
此外,利妥昔单抗维持治疗的应用(尤其不适宜大剂量治疗患者)显著改善了该群体生存。一项III期试验显示,ASCT后予3年利妥昔单抗维持治疗较观察组显著提高4年PFS(83% vs. 64%)及OS(89% vs. 80%),确立其标准地位。
需强调的是,ASCT在MCL中的长期疗效数据多源于前利妥昔单抗时代。含阿糖胞苷和利妥昔单抗的现代诱导方案背景下,ASCT相对于无巩固的PFS和OS获益尚未通过随机试验验证。因此,当前需探讨在更优的挽救治疗、靶向药物及强化维持方案可及的当下,ASCT能否仍带来生存获益?一项基于Flatiron健康数据库的真实世界分析(纳入2011-2021年4216例MCL患者)显示,ASCT与实际治疗间期(TTNT)或OS无显著关联(TTNT HR=0.84;OS HR=0.86),而利妥昔单抗维持治疗联合免疫化疗(利妥昔单抗-苯达莫司汀)可显著延长TTNT(HR=1.96)及OS(HR=1.51),提示长期生存获益可能更依赖于强化维持而非ASCT。
ASCT的局限性还包括高急性及远期毒性,尤其考虑MCL中位发病年龄为67岁,多数患者存在毒性风险。近期III期TRIANGLE试验评估了ASCT在一线治疗中的剩余价值:870例<65岁患者随机分为三组:标准ASCT组(A组)、含伊布替尼的ASCT组(A+I组)及无ASCT的伊布替尼联合组(I组)。中位随访53个月后,A+I组3年无失败生存期(FFS)达86%,显著优于A组(75%;单侧P=0.0034,HR=0.64);I组FFS亦优于A组(85% vs. 75%;单侧P=0.0102)。但A+I组与I组间无显著差异(3年FFS 86% vs. 85%)。OS方面,A+I组(3年OS 90%)及I组(91%)均优于A组(85%)。
TRIANGLE试验允许所有组别接受利妥昔单抗维持治疗(依国家指南)。探索性分析显示,联合伊布替尼维持可改善缓解持续时间(DOR,HR=0.35),但感染毒性发生率更高(30% vs. 25% vs. 13%)。血液学毒性(≥3级)仅在A组显著升高(28% vs. 11%),其他组别无差异。伊布替尼维持固定疗程为2年,多数患者完成治疗后仍持续缓解,提示复发后重启BTKi可能有效,但MCL中BTKi再挑战数据有限,需警惕既往BTKi暴露可能降低后续挽救疗效。综上,TRIANGLE试验证实含伊布替尼方案较传统ASCT方案疗效更优,且无ASCT的伊布替尼联合方案不劣于标准治疗,由此确立其为年轻MCL患者一线治疗新标准。是否ASCT仍能为部分患者带来额外获益,需进一步明确。
基于微小残留病(MRD)状态对预后的强预测价值(MRD阴性患者后续PFS更优),ECOG-ACRIN 4151试验(NCT03267433)比较了ASCT后利妥昔单抗维持与单纯利妥昔单抗维持(无ASCT)在MRD阴性首次完全缓解(CR)患者中的疗效。首次中期分析显示,MRD阴性(灵敏度10-6)患者未从ASCT巩固中获益,而MRD阳性患者可能受益于自体干细胞移植。需更长期随访验证。
MCL异质性显著,高风险特征包括TP53缺失/突变、Ki-67>30%及母细胞样形态,此类患者FFS和OS显著更差。即使接受优化免疫化疗、大剂量阿糖胞苷及ASCT,年轻TP53异常MCL患者预后仍不佳(如欧洲MCL Younger试验及北欧MCL2/MCL3试验数据)。因此,新版淋巴瘤分类推荐首次诊断时必须检测Ki-67增殖指数及TP53状态。此类高风险患者尤其受益于一线治疗加入伊布替尼。
针对TP53突变患者的II期BOVen试验(泽布替尼、奥妥珠单抗联合维奈克拉)报告了鼓舞人心的结果:25例初治患者总体缓解率(ORR)达96%,完全缓解率(CR)88%,中位随访28.2个月后,2年PFS、疾病特异生存及OS分别为72%、91%及76%,提示该方案可能成为TP53突变患者的有效选择,需进一步验证。
CAR-T细胞治疗或T细胞衔接器能否部分克服TP53异常的负面预后影响,目前正通过CARMAN试验探索。该试验为国际多中心、随机对照II期试验,评估CAR-T(brexucabtagene autoleucel)对比标准含伊布替尼诱导化疗(≤65岁患者接受伊布替尼-利妥昔单抗3周期序贯伊布替尼-R-CHOP 2周期,非PR者进入ASCT)的疗效与安全性,并包含6个月伊布替尼维持治疗(CAR-T后3个月启动)。
2、老年患者(>65岁)的治疗
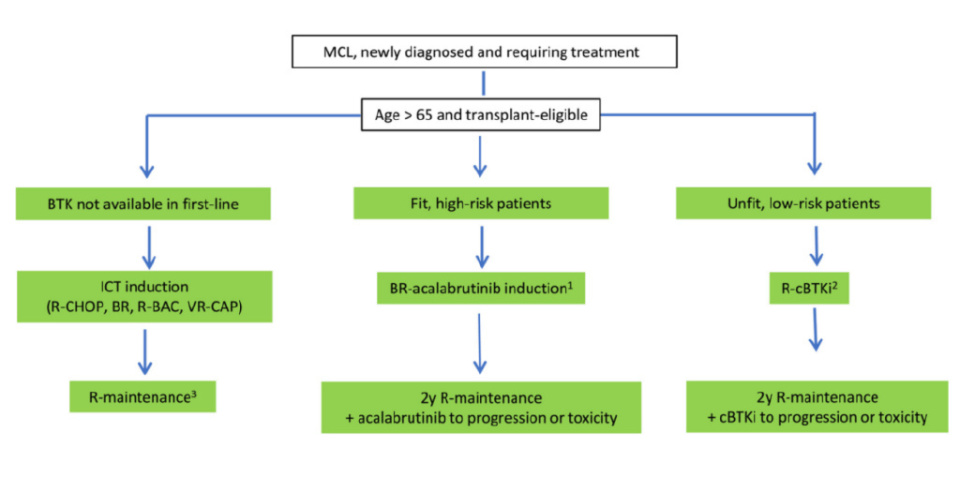 针对65岁以上患者的建议治疗方案
针对65岁以上患者的建议治疗方案
不适合移植的>65岁患者群体在体能和认知能力方面表现出高度异质性。体能状态良好的>65岁患者应接受常规免疫化疗后接利妥昔单抗维持治疗。一项大型国际III期试验证实,硼替佐米、利妥昔单抗、环磷酰胺、阿霉素和泼尼松(VR-CAP)联合方案相比R-CHOP方案显著延长了总生存期(OS),82个月时的OS翻倍(90.7个月 vs. 45.7个月)。然而,试验组血液学毒性(尤其是≥3级血小板减少症)显著增加(57% vs. 6%),因此建议修改硼替佐米用药方案(仅第1天和第4天给药)。利妥昔单抗、苯达莫司汀联合阿糖胞苷(R-BAC)方案提供了另一种有效的选择。但该方案伴随着严重的血液学毒性,因此应仅用于体能状态极佳且具有高风险特征(如母细胞样变异型、高LDH水平)的老年患者。
对于不符合此类强化治疗方案条件的患者,R-苯达莫司汀(BR)提供了一种适当替代方案。与R-CHOP相比,该联合方案达到相似的缓解率(93% vs. 91%),在无进展生存期(PFS)上数值上更优(35个月 vs. 21个月),且观察到更良好的安全性特征。然而,根据我们在临床实践中的经验,BR常伴有严重的迟发性感染并发症。英国一项现实世界数据分析报告,在接受BR治疗的患者中,21.7%发生了与苯达莫司汀相关的3-5级严重不良事件(SAE),其中约50%为感染(最常见呼吸道和泌尿道感染),且与中性粒细胞减少无关。13%的患者因苯达莫司汀相关毒性(最常见感染)而停止治疗。
一项大型欧洲III期随机试验比较了利妥昔单抗维持治疗与干扰素维持治疗,证实了利妥昔单抗作为维持治疗的优效性。该研究中,R-CHOP诱导治疗后接受利妥昔单抗维持的患者,4年后58%仍处于缓解状态,而干扰素组为29%(P=0.01)。利妥昔单抗组的无进展生存期和总生存期也显著改善(5年PFS:利妥昔单抗组51% vs. 干扰素组22%;5年OS:利妥昔单抗组79% vs. 干扰素组59%)。类似地,一项美国大型回顾性调查也表明利妥昔单抗维持带来更优的无进展生存率和总生存率。基于这些结果,利妥昔单抗维持治疗现被普遍推荐。
综上所述,VR-CAP、BR或R-CHOP代表了当前不适合大剂量治疗(占套细胞淋巴瘤患者多数)老年患者的标准方案。我们认为,对于较高风险特征(如高Ki67表达、母细胞样形态)的患者,应优先选择VR-CAP。BR则可能特别适用于表现更像慢性淋巴细胞白血病(CLL)的惰性型患者。
SHINE试验在≥65岁患者中比较了利妥昔单抗-苯达莫司汀(BR)联合伊布替尼与单独BR方案,显示伊布替尼组相比单用BR组显著延长了中位PFS(80.6个月 vs. 52.9个月),但总生存期(7年时57% vs. 55%)相似。ECHO III期试验评估了阿卡替尼(Acalabrutinib)联合BR方案,结果同样显示显著的PFS获益(包括具有高风险特征的患者),以及在剔除COVID事件后观察到的总生存期改善趋势。
近期发表的随机II/III期ENRICH试验在≥60岁患者中比较了一线利妥昔单抗-伊布替尼(IR)方案与利妥昔单抗-化疗方案(R-化疗)。结果显示IR相较于R-化疗显著延长PFS(65.3个月 vs. 42.4个月),尤其在与R-CHOP方案相比时效果更明显。IR方案降低了血液学毒性并改善了患者生活质量。
总之,BR-阿卡替尼可能代表一种有用的选择,特别适合体能状态良好且能耐受此三联方案的高危患者。不含化疗的利妥昔单抗-共价BTK抑制剂(R-cBTKi)方案对于患有合并症的老年患者是可行的治疗选择。
结 论
总体而言,共价BTK抑制剂正日益整合到一线治疗方案和临床实践中。根据近期公布的TRIANGLE试验结果(显示含伊布替尼的方案优于化疗后接ASCT),目前认为在年轻套细胞淋巴瘤患者的一线治疗中,将伊布替尼加入CHOP类方案并进行利妥昔单抗维持已成为新的标准治疗。
未来,BR-阿卡替尼可能成为老年但体能状态良好/强壮且能耐受此三联方案患者的有用选择。利妥昔单抗-cBTKi对于患有合并症的老年患者是一个有吸引力的选项。
然而,由于法规和医保问题,共价BTK抑制剂在各地的可及性存在差异。若无法获得伊布替尼,尽管缺乏III期数据,第二代BTK抑制剂如泽布替尼可视为合理的替代选择,尤其是伴有TP53畸变的患者可受益于基于BTK抑制剂的方案,但应尽可能将这些患者纳入临床试验中接受治疗。