套细胞淋巴瘤(MCL)被认为是一种侵袭性强、目前尚无法治愈的成熟B细胞肿瘤,其特点表现为复发模式,每次疾病进展后的缓解期和生存期缩短。当复发发生在化学免疫疗法(CIT)后早期,或存在高危特征时,患者预后尤其不良。近年来,布鲁顿酪氨酸激酶抑制剂(BTKi)的引入彻底改变了复发/难治性(R/R)MCL患者的治疗格局,现正逐步被整合进入一线治疗方案。因此,治疗方案的选择排序颇具挑战性,因为针对接受过不同一线BTKi为基础治疗后进展的患者的最佳管理策略仍未明确。巴塞罗那临床医院(Hospital Clínic of Barcelona)Eva Giné教授表示,当前治疗模式正从CIT转向包含新型细胞免疫疗法和T细胞衔接器免疫疗法在内的靶向联合方案,这一转变前景广阔,且科学证据的生成也在稳步推进中。
R/R MCL获批的新型靶向治疗
对MCL分子病理生理学认识的深入,促进了多种靶向药物在R/R MCL领域的研发和获批。尽管目前仅对伊布替尼和替西罗莫司进行过直接比较,但在一线CIT治疗后,共价BTK抑制剂(cBTKi)单药治疗已被确立为标准治疗。此外,针对cBTKi治疗失败的患者,近期已有两种靶向CD19的嵌合抗原受体T细胞(CAR-T)疗法产品——Brexucabtagene autoleucel(Brexu-Cel)和lisocabtagene maraleucel(liso-cel),以及首款非共价BTK抑制剂(非共价BTKi)匹妥布替尼(Pintobrutinib)获批上市。
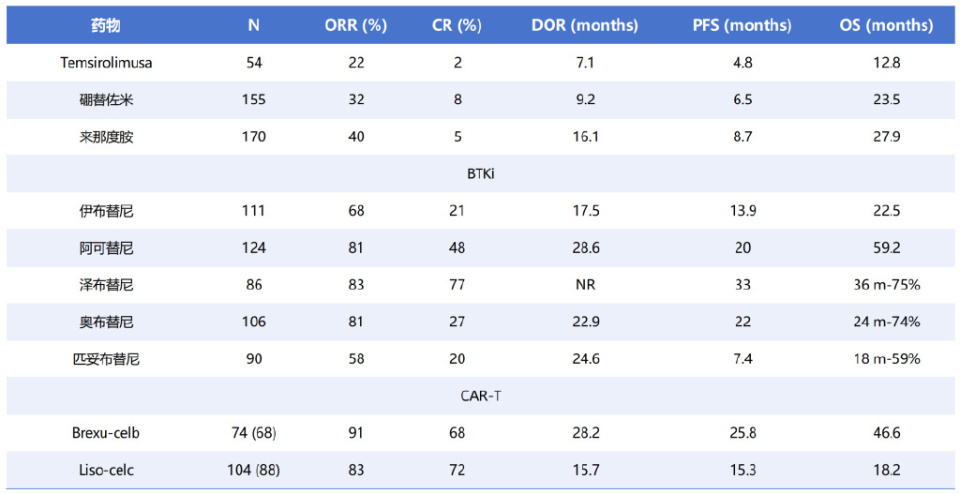 R/R MCL的单药靶向治疗
R/R MCL的单药靶向治疗
重要的是,制定最佳的治疗排序策略需要在每次疾病进展时,仔细评估疾病风险特征、患者个体因素(包括合并症、既往治疗经历和毒副反应)以及患者偏好,以便为每位患者设定恰当的治疗目标。此外,各国对新型疗法的可及性存在差异,这对治疗方案的选择和排序具有重大影响。
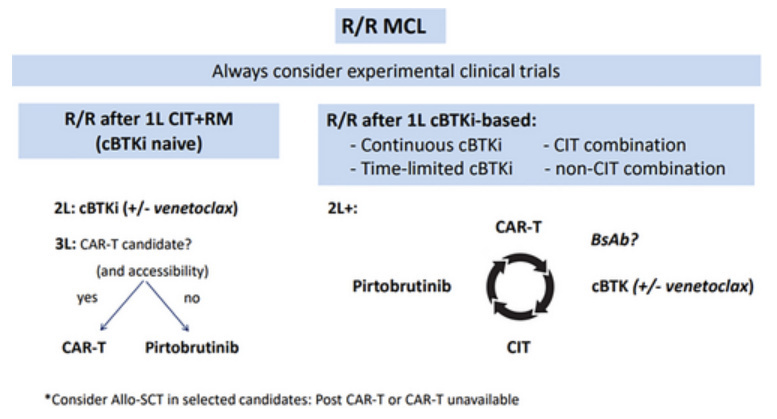 关于套细胞淋巴瘤治疗考虑因素
关于套细胞淋巴瘤治疗考虑因素
1、共价BTK抑制剂
目前,第一代cBTKi伊布替尼是自2014年以来在欧洲获批用于R/R MCL的唯一共价抑制剂。通常持续给药直至疾病进展或出现不可耐受的毒性。伊布替尼在早期复发和晚期复发患者中均显示优势,尤其是在首次MCL复发时使用通常疗效更高。此外,在出现中枢神经系统(CNS)受累的情况下,伊布替尼也是优于其他选择的方案。在毒性方面,针对MCL的回顾性研究显示,因不良事件(AEs)导致的停药率范围较广(10%-26%)。
第二代cBTKi(阿可替尼和泽布替尼)具有更高的特异性,与伊布替尼相比脱靶抑制减少、毒性降低。其中阿可替尼和泽布替尼目前分别自2017年和2019年起在美国获批。奥布替尼仅在中国获批。cBTKi在具有不良预后生物学特征的MCL病例中(包括母细胞样/多形性变异、高Ki67或TP53突变病例)也表现出显著疗效,因此其应用迅速扩展,并取代了挽救性强化化疗(ICT)的地位。值得注意的是,在随机研究中,阿可替尼和泽布替尼诱发的房颤、高血压和出血事件发生率均低于伊布替尼。此外,对于各类B细胞肿瘤患者,在维持疾病高效控制的同时,切换使用不同抑制剂可在多数情况下显著改善毒副反应。
最后,匹妥布替尼(pirtobrutinib)作为首款在欧洲和美国获批用于cBTKi失败后的非共价BTKi将在后文详述。值得注意的是,其安全性特征似乎具有特别优势。一项正在进行的随机研究正在直接比较匹妥布替尼与cBTKi,其结果有望澄清未来MCL领域抑制剂的选择。
2、基于cBTKi的无化疗联合方案与其他方案
为提高伊布替尼的疗效,在多项针对R/R患者的II期试验中对其进行了联合用药探索。近期公布了一项最具前景且协同性强的联合方案(伊布替尼联合维奈克拉)的随机研究的初步数据。其中伊布替尼持续给药直至进展,维奈克拉则仅在前24个月联合使用。与单药伊布替尼相比,该联合方案显著改善了无进展生存期(PFS),尽管≥3级AE的发生率更高。截至目前,两组间总生存期(OS)未检出差异。此外,对TP53突变病例的亚组分析提示该联合方案可能具有良好活性。另一方面,II期AIM研究的长期随访显示,在达到无法检测微小残留病(uMRD)的R/R患者中,中断治疗仍可维持持续缓解,并且在进展时进行再次治疗是可行的。此外,在R/R病例中发现主要累及9p的基因损伤。
除上述方案外,一些不含cBTKi的靶向联合方案也在进行测试。维奈克拉-R2(来那度胺联合利妥昔单抗)组合方案即使在对BTKi既往暴露的患者中也显示出尚可的活性(总缓解率[ORR]分别为63%和40%),但TP53突变病例的结局明显差于野生型病例。该研究还为R/R MCL患者实施以MRD驱动的限时治疗提供了可行性证据,48%的患者在维持缓解状态下停止了治疗。
随着BTKi逐步纳入一线治疗,这将促使目前用于治疗BTKi失败的方案更早应用,并强化了对开发具有不同作用机制新策略的需求。尽管如此,某些情况下患者对BTKi可能仍保持敏感性,例如既往限时暴露者。此类情形下,考虑再次暴露于BTKi(可能以联合方式为佳)是合理的,尽管目前相关经验尚有限。最终,确定最佳的基于BTKi的联合方案类型、其治疗时长以及在不同MCL患者亚组中的排序,将是未来几年研究的挑战。
3、共价BTK抑制剂在MCL中的治疗失败
在MCL中,疾病进展是cBTKi治疗失败的主要原因,而非药物不耐受。约三分之一患者对伊布替尼存在原发性内在耐药,其余患者则会随时间发展获得性耐药。与伊布替尼耐药相关的生物学机制复杂且尚未完全阐明,目前已知涉及PI3K-AKT通路的持续活化、BCR信号的替代性激活,以及代谢向氧化磷酸化和谷氨酰胺分解等的重编程。与慢性淋巴细胞白血病(CLL)相反,BTKC481S突变和PLCG2突变在伊布替尼难治性MCL中罕见或未见报道。高危特征患者对cBTKi表现出更大的耐药性且缓解期短,在一线CIT后早期进展的患者或在首次复发后阶段使用伊布替尼时也观察到类似情况。一个简单的临床模型——BTKi MIPI已被提出用于估计二线cBTKi的治疗时长。
全球范围内的回顾性研究显示,cBTKi治疗失败的患者预期寿命小于1年。值得注意的是,高达30%-50%的患者未接受后续治疗并迅速死亡。过去曾使用过多种挽救治疗方案,但无一方案显示出明显优于其他方案的优势。传统的挽救治疗如CIT、硼替佐米、来那度胺甚至超适应证使用维奈克拉,通常仅能获得较低且短暂的缓解。最成功的策略之一是采用R-BAC方案,可为适宜患者在清髓性预处理后桥接异基因造血干细胞移植(allo-SCT)。
就此而言,allo-SCT仍是迄今为止MCL唯一可能治愈的治疗手段,甚至可能消除TP53改变的有害影响。然而,其适用性高度受限,仅适用于年轻、体能状态好、疾病有反应且能找到供者的患者。事实上,allo-SCT的使用多年来持续减少,尤其是在新型细胞免疫疗法引入后。
4、CAR-T细胞疗法
CAR-T细胞疗法是目前cBTKi失败后疗效最高的挽救选择,但其可及性存在众所周知的局限。总体而言,不同产品均能诱导较高的完全缓解(CR)率,且在高危患者中也具有一致性。然而,该疗法相关的毒性不容忽视,在MCL中的治愈潜力亦不明确,尽管观察到一些持久的缓解。
基于关键性单臂ZUMA-2研究的结果,Brexu-Cel是自2020年以来欧洲唯一获批用于MCL的CAR-T产品。在先前的cBTKi治疗失败的病例中,Brexu-Cel获得了前所未有的持久缓解。五年随访显示25%的回输患者仍处于持续CR状态,但并未观察到生存曲线出现平台期,这与弥漫大B细胞淋巴瘤(DLBCL)不同。此外,在相当数量的患者中观察到与Brexu-Cel相关的免疫毒性事件。上市后研究也证实了Brexu-Cel结果在临床试验不符合入组标准的患者以及高风险特征病例中的可重现性,尽管后者获益程度相对较低。此外,需要重症监护病房(ICU)支持的患者比例达20%,且主要因感染导致的非复发死亡率(NRM)高于预期。MCL患者接受CAR-T细胞疗法后发生严重血液毒性的风险增加,导致严重感染率升高且生存结局更差。在MCL患者中,不同病种间的NRM最高,达10.6%。
liso-cel代表了应对BTKi失败的一种潜在新型治疗选择,并于2024年6月获得美国食品药品监督管理局(FDA)批准。该疗法在高危MCL病例(甚至伴有CNS受累或allo-SCT后病例)中具有活性,并表现出良好的安全性特征,免疫相关毒性较低。初始研究人群(主要为经过大量预处理的老年患者)报告的中位PFS为15个月。CAR-T产品varnimcabtagene autoleucel (ARI-0001)也取得了相似结果。
为解决CD19 CAR-T疗法的毒性及复发风险顾虑,一项针对20例MCL患者的限时伊布替尼联合CTL019 CAR-T的初步结果已公布。该联合方案可行且有效,数据表明伊布替尼对CAR-T细胞适应性和回输后动力学有积极作用。此经验为首创,诸多将BTKi与细胞免疫疗法或其他T细胞衔接器免疫疗法联合用于MCL的方案正在探索中。
意向性治疗分析表明,14%-30%获批接受CAR-T治疗的MCL患者未能完成产品回输,主要原因为疾病进展,其次是生产失败。使用桥接治疗的患者比例在68%至90%之间,且有治疗反应的患者似乎结局更好。肿块大小、≥3处结外受累、乳酸脱氢酶升高和ECOG体能状态评分>1等特征也与接受Brexu-Cel后生存结局更差及更多毒性相关,这表明需要制定更有效的桥接策略。值得注意的是,应避免在单采前至少6个月内使用苯达莫司汀,因其可能影响T细胞数量和功能,导致生产失败率增高、CAR-T细胞扩增不足、甚至PFS和OS缩短。
CAR-T在MCL早期治疗线和高危患者中的作用正在被积极研究,有望改善患者结局。近期报告了86例BTKi初治R/R MCL患者接受Brexu-Cel治疗的初步数据,报告的总缓解率(ORR)和完全缓解率(CRR)分别高达91%和73%,且观察到的安全性特征无明显改变。
关于cBTKi失败后CAR-T细胞疗法和allo-SCT在MCL治疗决策中的定位,主要移植协会2021年的推荐已将其置于allo-SCT之前,主要基于其更好的安全性特征。近期一项欧洲血液和骨髓移植学会(EBMT)的研究也对比了这两种选择,显示Brexu-Cel具有更优的安全性特征,治疗相关死亡率更低且无慢性移植物抗宿主病发病率。在两项近期发布的报告中,CAR-T失败患者预后极差,OS短于6个月;allo-SCT在此背景下的数据仅有个案报道。
5、非共价BTK抑制剂
为满足伊布替尼失败后对可及、耐受良好且有效疗法的未满足需求,研发了首创新药高选择性非共价BTKi匹妥布替尼,并近期在欧盟获批。匹妥布替尼采用远离C481位点的可逆性BTK结合模式,无论肿瘤细胞自身BTK更新率如何均可实现持续的BTK抑制,这很可能解释了其在cBTKi失败后仍具活性的原因,而序贯使用其他cBTKi则观察到阴性结果。因此,匹妥布替尼显示出高活性:缓解率57%、CR率20%、中位起效时间1.8个月、中位缓解持续时间21.6个月。在高危患者中也观察到一致的结果,尽管其PFS较短。值得注意的是,匹妥布替尼具有特别良好的安全性特征,停药率低至3%。疲劳和腹泻是最常报告的毒性事件,3级事件中以中性粒细胞减少和感染为主。3级房颤和出血事件罕见,未报告高血压病例。其他非共价BTKi(如nemtabrutinib)也正处于临床研发阶段。
总而言之,目前在欧盟内有两种截然不同的方案被推荐用于cBTKi失败后的挽救治疗。无疑,匹妥布替尼提供了更便捷、即时的治疗可及性和更优的安全性。然而,ZUMA-2与BRUIN研究之间的间接比较提示,在缓解率和PFS方面疗效更优的是Brexu-Cel。值得注意的是,BRUIN试验中高达19%的患者后续接受了CAR-T细胞疗法,这也说明匹妥布替尼作为一种桥接选择具有重要价值。
双特异性抗体与其他新兴疗法
关于潜在引入的新疗法,T细胞衔接双特异性抗体(BsAb)是目前在R/R MCL中初步结果最具前景的分子。近期报告了一项I/II期研究在60例患者中使用格菲妥单抗(一种CD20xCD3 BsAb,固定12个周期疗程,使用奥妥珠单抗预处理)的经验。其活性高,BTKi初治和经治患者的CR率均超过70%,中位CR持续时间分别为15个月和12个月。用于处理细胞因子释放综合征(CRS)的托珠单抗使用率和ICU入住率分别为37%和15%。格菲妥单抗停药率为7%,5级不良事件为15%(主要因CR患者罹患COVID19感染)。一项III期研究正在进行中,旨在进一步评估格菲妥单抗单药疗法用于BTKi经治R/R MCL患者。Epcoritamab和odronextamab也在进行MCL适应症评估(数据有限)。此外,也有报道在BTKi和CAR-T细胞疗法失败后患者中,采用莫妥珠单抗与维泊妥珠单抗联合方案取得了鼓舞性结果。
然而,在MCL领域,仍需更多关于缓解持续时间和安全性(特别是在CRS管理和感染性并发症方面)的数据,以更好地定义BsAb的最佳联合方案、定位和目标人群。多项临床试验正在更早期的治疗线中评估基于BsAb的联合方案。未来的证据也将有助于澄清BsAb和CAR-T细胞疗法在MCL中的最佳应用选择,鉴于骨髓和外周血高浸润的特性,其应用难度可能较其他疾病更高。目前,初步数据显示BsAb用于治疗CAR-T失败患者结果令人鼓舞。
重要的是,当前正积极研发多种新作用机制的疗法,包括非共价BTKi、BTK降解剂、Bcl-2抑制剂、靶向ROR1的抗体药物偶联物、BsAb、双抗原靶向CAR-T(如lv20.19)、具有新靶点的CAR-T、人源化和通用型(同种异体)CAR-T,这些有望为改善MCL患者结局做出贡献。