近日,EHA 2025大会报告(EHA Perspectives Congress Reports)正式发布,分为恶性血液学和非恶性血液学两大部分。报告全面梳理了大会期间公布的重大科研成果与临床进展,为全球血液学专业人士提供了深入了解领域前沿动态的权威参考。本期特整理非恶性血液学报告中关于“血小板疾病的新治疗方式”的专题内容,分为上下两部分(点击此处查看上部分内容),旨在为大家提供富有价值的临床与科研洞见。
精选演讲概览
靶向细胞毒性T细胞治疗难治性ITP的潜力
在免疫性血小板减少症(ITP)中,对利妥昔单抗治疗无应答的患者表现出一种独特的免疫特征,包括重新表达CD45RA的终末分化效应记忆CD8+T细胞(TEMRA)增多,这些细胞具有高度的细胞毒性和衰老特征,并参与血小板的破坏。T细胞受体(TCR)深度测序显示,难治性患者的T细胞多样性降低,同时伴有克隆扩增。值得注意的是,在慢性ITP中,T细胞的多样性似乎与血小板计数相关,其中扩增的单个T细胞克隆与多样性降低和血小板水平下降相关。配对TCR和基因表达谱分析进一步证实,这些扩增的CD8+T细胞主要富集在TEMRA亚群。这表明在难治性ITP患者中,靶向细胞毒性T细胞可能具有潜力[3]。
T细胞靶向疗法,包括吗替麦考酚酯(MMF)、硫唑嘌呤、环磷酰胺和环孢素,在ITP中的反应率为30%-50%,尽管它们通常耐受性差。有趣的是,对艾曲泊帕(eltrombopag)应答者的 CD8+TEMRA细胞数量减少。艾曲泊帕已被证明对白血病细胞具有抗增殖作用,并抑制CD8+T细胞的增殖。在一小部分难治性ITP患者中,艾曲泊帕与MMF联合治疗获得了更高的缓解率,达到72%,提示二者可能具有协同作用[3]。
GPIb/IX 抗体阳性的患者往往血小板计数更低、对常规治疗反应更差,更易进展为难治或复发性 ITP。研究表明,调节性T细胞(Treg)可以用于调节免疫微环境并治疗自身免疫性疾病。在此基础上,推测工程化的嵌合抗原受体 (CAR)-Treg 细胞可通过抑制 B 细胞抗体分泌、效应 T 细胞增殖和抗原呈递细胞活性来提供全面的免疫调节。
TCR多样性及克隆扩展
为了探讨这一概念,研究者设计了一种靶向 GPIbα 的嵌合自身抗体受体(CAAR),该受体的外部配体结合域包含自体抗原。通过流式细胞术分离人类初始Treg细胞,并使用慢病毒载体将CAAR构建体转导到这些细胞中。抑制性功能实验证实,GPIbα-CAAR-Treg细胞在体外表现出选择性抗原特异性激活,并且展示了特异性和非特异性的抑制作用。此外,在造血杂交瘤模型中,这些细胞有效抑制了CAAR-效应T细胞对GPIbα杂交瘤细胞的细胞毒活性,为其在ITP中的新型治疗潜力提供了实验依据[9]。
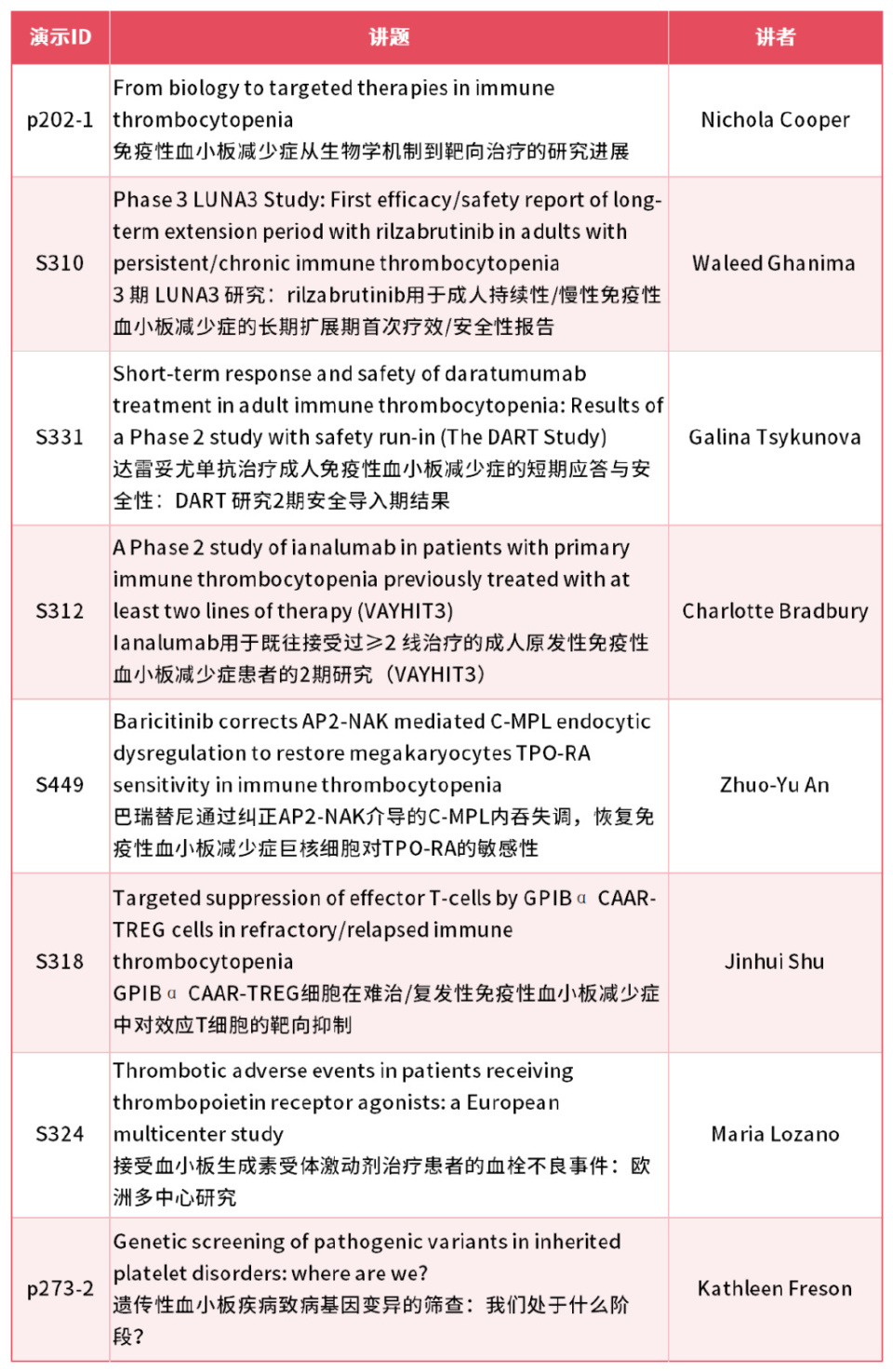
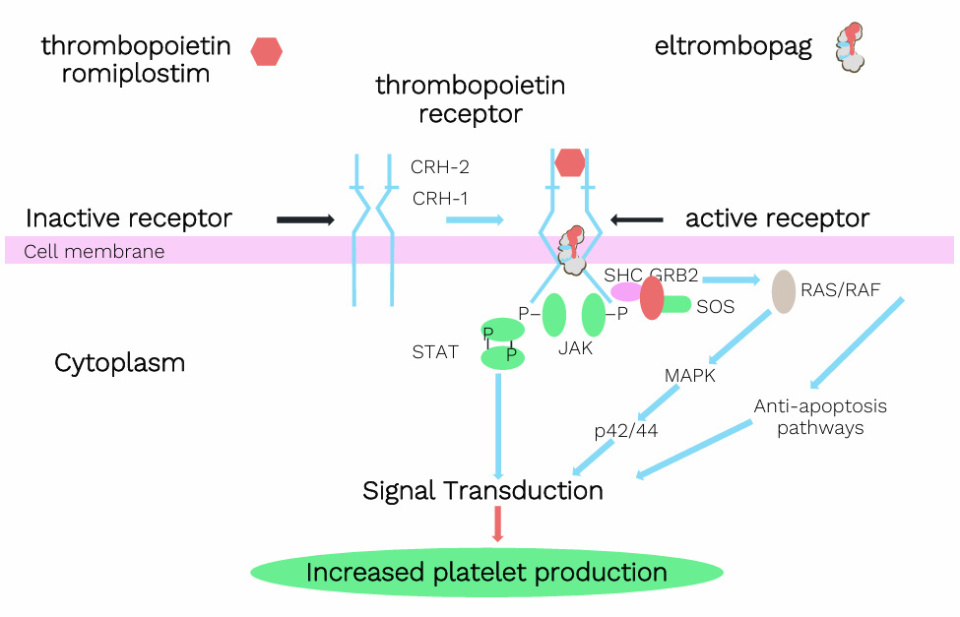
TPO-RA 治疗患者血栓性不良事件的预测因素
ITP是一种复杂的自身免疫性疾病,通常会导致出血,但也可能引发血栓形成,使得该疾病的治疗面临更大挑战。继发性ITP和使用血小板生成素受体激动剂(TPO-RA)是血栓形成的最强独立预测因素。
在EHA 2025上,分享了Vertex 3 研究的数据[10]。该研究旨在评估接受TPO-RA治疗的ITP患者中血栓性不良事件的发生率、特征及风险因素,从而为潜在的预测因素和优化安全性的策略提供参考。共分析了417个TPO-RA治疗疗程,包括首个疗程267个、第二个疗程113个和第三个疗程37个。结果显示,根据每100个TPO-RA疗程,首个疗程的血栓事件发生率为8.2%,第二个或第三个疗程的发生率为7.3%。治疗期间血栓形成的关键预测因素包括既往血栓事件、诊断时的高血压以及治疗开始时的高血压。其他预测因素包括治疗期间的最高血小板计数、6个月时的血小板计数以及对TPO-RA的快速反应。大多数病例得到缓解,44%停止治疗的患者后来恢复了TPO-RA治疗。这些发现强调了对接受TPO-RA治疗患者进行仔细监测和风险分层的重要性,但也指出,仍需进一步研究以优化该患者群体中的血栓风险管理。
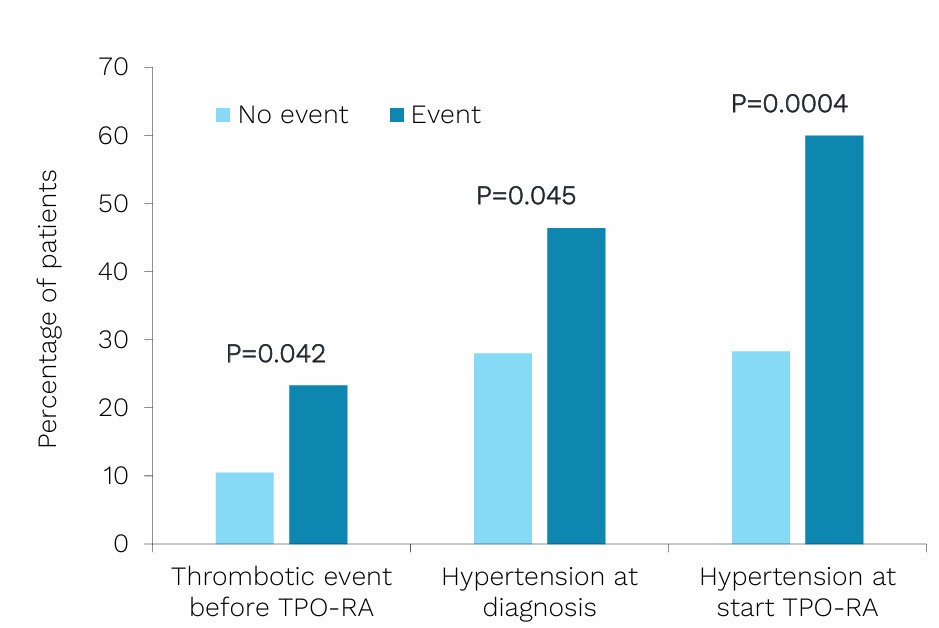
TPO治疗期间血栓事件发生的患者特征差异
总之,EHA 2025 展示了针对ITP复杂发病机制多个环节的新兴治疗模式的显著进展。
遗传性血小板疾病的致病变异基因筛查
迄今为止,已在68个基因中发现了与遗传性血小板疾病相关的致病变异。相比单纯血小板功能障碍,更多基因与伴有功能缺陷的血小板减少症相关。在临床实践中,通常采用基因panel和靶向测序方法进行该类疾病的基因诊断。
根据美国医学遗传学与基因组学学会(ACMG)和美国分子病理学协会(AMP)发布的 19 项指南,基因变异被分为五类:致病、可能致病、意义未明变异(VUS)、可能良性或良性[11]。目前,正投入大量工作,包括通过家系共分离研究、详细表型分析、功能实验及蛋白建模等,对 VUS 进行重新分类[12]。
计算机辅助工具(如Franklin)越来越多地用于变异分类。Franklin整合了多套预测软件(包括 dbscSNV、Splice AI、Primate AI、FATHMM、AlphaMissense 和 REVEL),以生成变异致病性的综合预测。然而,没有任何单一工具可以独立完成判断;预测结果必须与表型数据进行佐证,并与 ClinVar 等现有数据库交叉比对,以确认该变异是否已在其他患者中报道[13]。
参考文献:
[1]Cooper N, et al. Immune thrombocytopenia (ITP) World Impact Survey (I-WISh): Impact of ITP on health-related quality of life. Am J Hematol. 2021;96(2):199-207.
[2]Provan D, Semple JW. Recent advances in the mechanisms and treatment of immune thrombocytopenia. EBioMedicine. 2022;76:103820.
[3]Cooper N. From biology to targeted therapies in immune thrombocytopenia. Abstract p202-1 presented at EHA2025.
[4]Garzon AM, Mitchell WB. Use of Thrombopoietin Receptor Agonists in Childhood Immune Thrombocytopenia. Front Pediatr. 2015;3:70.
[5]An ZY. Baricitinib corrects AP2-NAK mediated C-MPL endocytic dysregulation to restore megakaryocytes tpo-ra sensitivity in immune thrombocytopenia. Abstract S449 presented at EHA2025.
[6]Ghanima W. Phase 3 LUNA3 study: First efficacy/safety report of long-term extension period with rilzabrutinib in adults with persistent/chronic immune thrombocytopenia. Oral abstract s310 presented at EHA2025.
[7]Tsykunova G. Short-term response and safety of daratumumab treatment in adult immune thrombocytopenia: results of a Phase II study with safety run-in (DART study). Oral abstract S331 presented at EHA2025.
[8]Bradbury C. A Phase 2 study of ianalumab in patients with primary immune thrombocytopenia previously treated with at least two lines of therapy (VAYHIT3). Oral abstract s312 presented at EHA2025.
[9]Shu J, et al. Targeted suppression of effector T cells by GPIBΑ CAAR-TREG cells in refractory/relapsed immune thrombocytopenia. Oral abstract s318 presented at EHA2025.
[10]Lozano M, et al. Thrombotic adverse events in patients receiving thrombopoietin receptor agonists: A European multicenter study. Abstract S324, presented at EHA2025
[11]Richards S, et al. Standards and guidelines for the interpretation of sequence variants: a joint consensus recommendation of the American College of Medical Genetics and Genomics and the Association for Molecular Pathology. Genet Med. 2015;17(5):405-424.
[12]Ramanan R, et al. Implementation and clinical utility of multigene panels for bleeding, platelet, and thrombotic disorders. J Thromb Haemost. 2025:S1538-7836(25)00277-6.
[13]Freson K. Genetic screening of pathogenic variants in inherited platelet disorders: where are we? Oral presentation P273-2 presented at EHA2025.