编者按:近日,EHA 2025大会报告(EHA Perspectives Congress Reports)正式发布,分为恶性血液学和非恶性血液学两大部分。报告全面梳理了大会期间公布的重大科研成果与临床进展,为全球血液学专业人士提供了深入了解领域前沿动态的权威参考。本期特整理非恶性血液学报告中关于“血小板疾病的新治疗方式”的专题内容,分布上下两部分(本文为上),旨在为大家提供富有价值的临床与科研洞见。
精选演讲概览
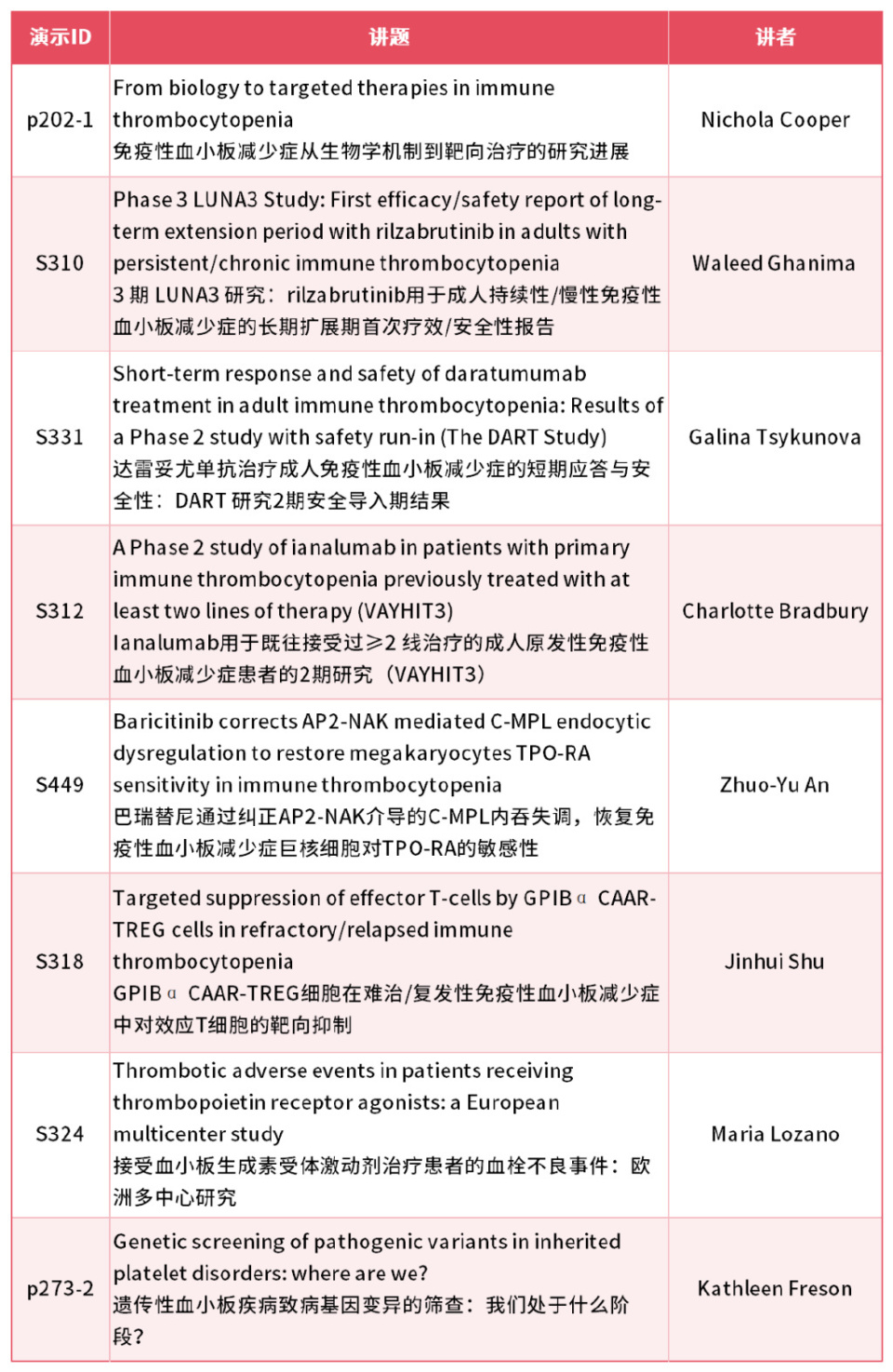
免疫性血小板减少症(ITP)的靶向治疗
ITP 是一种血液系统自身免疫性疾病,其特征为血液中血小板计数减少(<100×109/L)[1]。
血小板生成素受体激动剂(TPO-RAs)
在ITP患者中,尽管血小板计数明显降低,但血小板生成素(TPO)水平却正常或仅略有升高。这是由于血小板清除增加所致,即使造血过程仍保持正常。内源性TPO与TPO受体的胞外结构域结合。TPO-RAs通过结合TPO受体的细胞外结构域(如罗普司亭)或跨膜区域(如艾曲泊帕和阿伐曲泊帕),模拟天然TPO的作用[2]。研究显示,大约58%的患者在接受艾曲泊帕或罗普司亭治疗后获得良好的血小板反应;然而,仍有多达42%的患者需要其他替代疗法[3]。
c-MPL受体是内源性TPO及合成激动剂的主要靶点。其正常功能依赖于正确的膜表面表达以及通过JAK2/STAT3通路的信号转导,而SOCS蛋白可对该通路进行负向调控[4]。过度的c-MPL内吞可能通过减少可利用的膜表面受体数量,导致对TPO-RAs的耐药[5]。
siRNA敲低实验发现,AP2和GAK是促进c-MPL内吞的因子。GAK抑制剂巴瑞替尼能够抑制c-MPL 的内吞,并通过显著下调SOCS1的转录表达,恢复JAK2/STAT3 信号传导。在ITP小鼠模型中,巴瑞替尼治疗可显著提高外周血血小板计数。同时,巴瑞替尼还可下调骨髓中异常升高的SOCS1 蛋白水平,并增强JAK2与STAT3的磷酸化。这些结果表明,巴瑞替尼通过纠正AP2-NAK介导的c-MPL内吞失调,恢复ITP患者巨核细胞对TPO-RA的敏感性[5]。
B细胞靶向治疗
在EHA 2025大会上,ITP领域最新的B细胞靶向治疗进展得以全面展示。
抗CD20单克隆抗体利妥昔单抗(rituximab)在ITP患者中的应答率为30%-50%。该药物总体耐受性良好,若在发病首年应用,尤其是在女性患者中,疗效更佳。尽管复发常见,但大多数患者对再次治疗仍有反应[3]。
福坦替尼(Fostamatinib)是一种脾酪氨酸激酶抑制剂,可靶向巨噬细胞介导的血小板破坏。临床试验显示,对于多重难治性ITP患者,福坦替尼的总应答率为43%,稳定应答率为18%。真实世界数据提示,其疗效可能更高,尤其是在疾病早期或联合TPO-RAs应用时。
Rilzabrutinib是一种Bruton酪氨酸激酶抑制剂,可抑制B细胞增殖和巨噬细胞介导的血小板清除。II期临床试验显示其应答率为30%-40%,并在改善疲劳和生活质量方面表现出明显获益。LUNA是一项III期研究,旨在评估rilzabrutinib在成人和青少年持续性或慢性原发性ITP患者中的安全性和有效性(NCT04562766)。在EHA 2025上公布的长期扩展(LTE)数据显示,54%的患者达到完全缓解。在LTE期间,rilzabrutinib进一步改善了身体疲劳和出血评分。所有与治疗相关的不良事件均为1-2级,最常见的为恶心(7%)、腹泻(4%)和上腹痛(2%),其余不良事件均仅在单个患者中出现[6]。
当前正在探索的新型B细胞靶向药物包括针对CD38和BAFF-R的药物,这两类药物在EHA 2025上均展示了令人鼓舞的结果[3]。
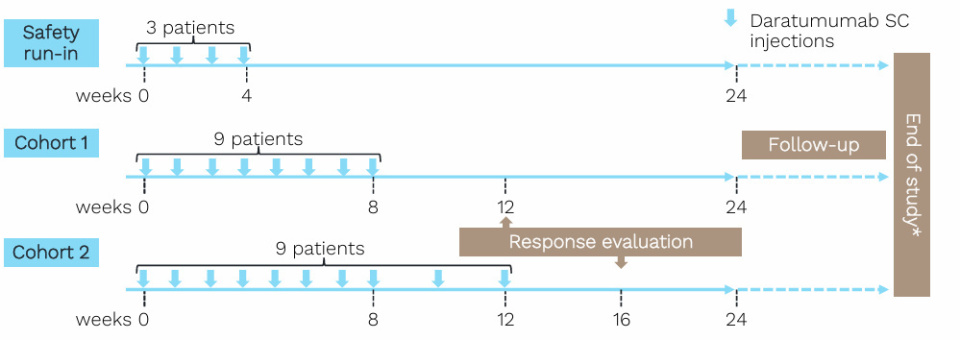
DART是一项开放标签、多中心、II期由研究者发起的研究(NCT04703621),旨在评估抗CD38单克隆抗体达雷妥尤单抗(daratumumab)在成人原发性ITP患者中的安全性和有效性。研究设计包括安全性导入阶段,随后进入两个队列。主要疗效终点(定义为间隔24小时以上测量,连续两次血小板计数>50×109/L)。在总人群中,该终点的达成率为48%,在队列1和队列2中均为44%。尽管起效迅速,但疗效随时间减弱,持续应答率整体为38%,其中队列1为44%,队列2为33%。主要安全性终点为≥2级治疗相关不良事件(TEAEs)的发生率和严重程度。结果显示,4.7%的患者发生2级感染,9.5%的患者发生2级腹泻(被认为与治疗相关)。感染是最常见的TEAE,发生率为38%[7]。
Ianalumab是一种在研的全人源化单克隆抗体,靶向B细胞活化因子受体(BAFF-R)。VAYHIT3是一项II期研究(NCT05885555),旨在评估短疗程静脉注射Ianalumab在大量治疗后的原发性ITP患者中的疗效与安全性。初步结果显示,44%的患者获得确证的血小板应答,中位应答时间为6周;24%的患者获得稳定反应;在18例应答者中,有56%(10/18)在第25周时血小板计数维持正常,其中9例达到完全缓解。Ianalumab总体耐受性良好,大部分不良事件与研究药物无关,未发生因不良事件导致的治疗中止。输注相关反应和感染多为1-2级,仅报告1例3级感染[8]。
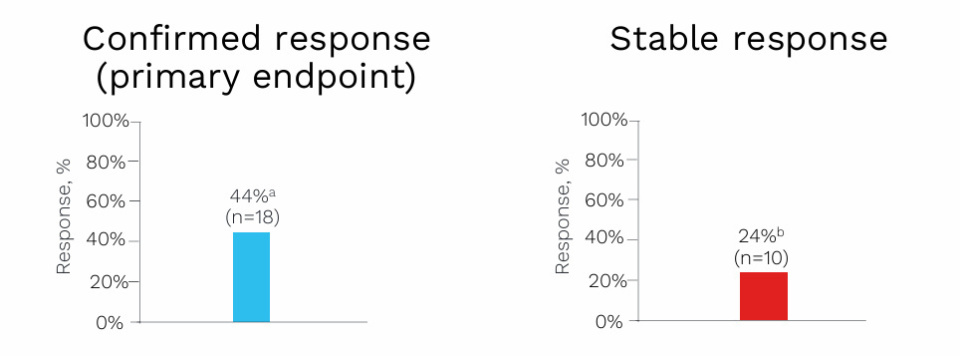 确证应答(Confirmed response)与稳定应答(Stable response)
确证应答(Confirmed response)与稳定应答(Stable response)
B细胞靶向治疗的应答率仅为30%-50%,这引发了关于治疗时机、是否需要更广泛的B/浆细胞清除,或是否存在其他驱动血小板破坏的免疫通路等问题的思考。(未完待续......)
参考文献:
[1]Cooper N, et al. Immune thrombocytopenia (ITP) World Impact Survey (I-WISh): Impact of ITP on health-related quality of life. Am J Hematol. 2021;96(2):199-207.
[2]Provan D, Semple JW. Recent advances in the mechanisms and treatment of immune thrombocytopenia. EBioMedicine. 2022;76:103820.
[3]Cooper N. From biology to targeted therapies in immune thrombocytopenia. Abstract p202-1 presented at EHA2025.
[4]Garzon AM, Mitchell WB. Use of Thrombopoietin Receptor Agonists in Childhood Immune Thrombocytopenia. Front Pediatr. 2015;3:70.
[5]An ZY. Baricitinib corrects AP2-NAK mediated C-MPL endocytic dysregulation to restore megakaryocytes tpo-ra sensitivity in immune thrombocytopenia. Abstract S449 presented at EHA2025.
[6]Ghanima W. Phase 3 LUNA3 study: First efficacy/safety report of long-term extension period with rilzabrutinib in adults with persistent/chronic immune thrombocytopenia. Oral abstract s310 presented at EHA2025.
[7]Tsykunova G. Short-term response and safety of daratumumab treatment in adult immune thrombocytopenia: results of a Phase II study with safety run-in (DART study). Oral abstract S331 presented at EHA2025.
[8]Bradbury C. A Phase 2 study of ianalumab in patients with primary immune thrombocytopenia previously treated with at least two lines of therapy (VAYHIT3). Oral abstract s312 presented at EHA2025.
[9]Shu J, et al. Targeted suppression of effector T cells by GPIBΑ CAAR-TREG cells in refractory/relapsed immune thrombocytopenia. Oral abstract s318 presented at EHA2025.
[10]Lozano M, et al. Thrombotic adverse events in patients receiving thrombopoietin receptor agonists: A European multicenter study. Abstract S324, presented at EHA2025
[11]Richards S, et al. Standards and guidelines for the interpretation of sequence variants: a joint consensus recommendation of the American College of Medical Genetics and Genomics and the Association for Molecular Pathology. Genet Med. 2015;17(5):405-424.
[12]Ramanan R, et al. Implementation and clinical utility of multigene panels for bleeding, platelet, and thrombotic disorders. J Thromb Haemost. 2025:S1538-7836(25)00277-6.
[13]Freson K. Genetic screening of pathogenic variants in inherited platelet disorders: where are we? Oral presentation P273-2 presented at EHA2025.