编者按:近日,EHA 2025大会报告(EHA Perspectives Congress Reports)正式发布,分为恶性血液学和非恶性血液学两大部分。报告全面梳理了大会期间公布的重大科研成果与临床进展,为全球血液学专业人士提供了深入了解领域前沿动态的权威参考。本期特整理非恶性血液学报告中关于“镰状细胞病的全球负担:如何将普遍可及性与最新基因治疗相结合?”的专题内容,分为上下两部分(点击此处查看上部分内容),旨在为大家提供富有价值的临床与科研洞见。
精选演讲概览
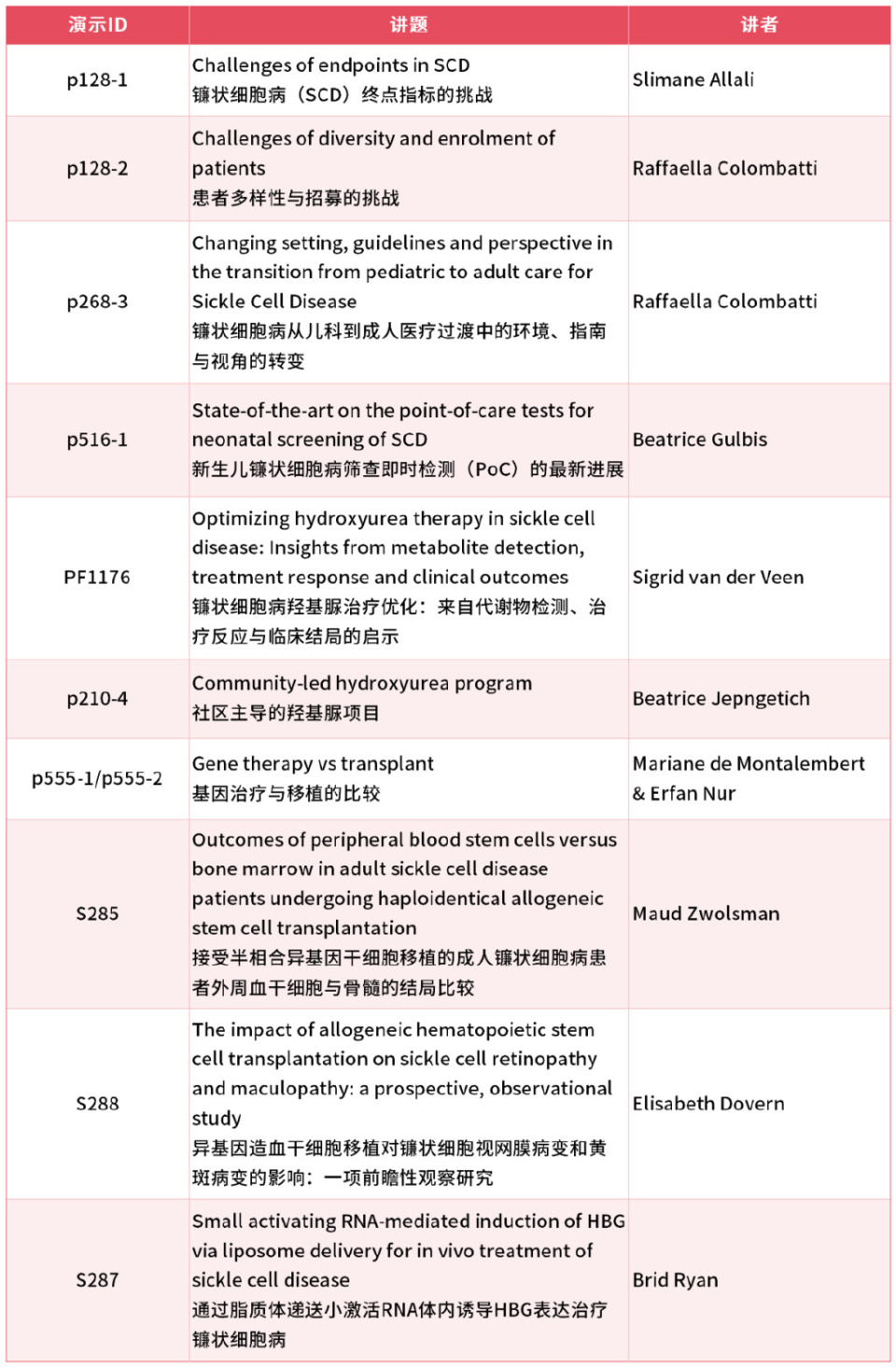
基因治疗 vs. 造血干细胞移植(HSCT)在镰状细胞病(SCD)中的应用
SCD患者的生存率令人担忧,81%的患者无法存活到50岁。若能治愈,患者便可摆脱恐惧,真正为未来做打算。目前有两种潜在的治愈性治疗方案:一是已相对成熟的造血干细胞移植(HSCT),二是新兴的基因治疗。在EHA 2025大会上,一场主题辩论对这两种疗法进行了正面交锋[7-8]。
Mariane de Montalembert博士支持基因治疗,并指出其优势包括:早期基因治疗方案已取得良好疗效,并且该领域进展迅速。与HSCT相比,基因治疗需要的动员周期更少、脱离骨髓抑制的时间更短,同时能诱导高水平的胎儿血红蛋白(HbF)生成。其安全性似乎与自体HSCT的风险相当。总体来看,基因治疗为患者带来了彻底治愈的希望。
对此,Erfun Nur博士则提出HSCT依旧是有效、普遍可及且相对经济的选择,其移植物抗宿主病(GVHD)风险较低。在儿童中效果尤佳,总生存(OS)率超过95%,无事件生存率达到92%。此外,HSCT适用于各个年龄段,几乎可为所有患者提供治疗机会。
然而,两种治疗方式都面临各自的挑战。对于基因治疗而言,一些患者无法进行动员,且自体造血干/祖细胞的功能可能受损。此外,还存在关于髓系恶性肿瘤、脱靶效应以及长期安全性的担忧。基因治疗目前仅在少数专科中心可及,且费用远高于自体移植。HSCT的挑战在于找到合适供者的概率较低,而在半相合HSCT中排斥风险更高。从患者角度看,该治疗复杂且负担较重,并且对部分人群而言,移植后的生活质量(QoL)提升并未达到预期。
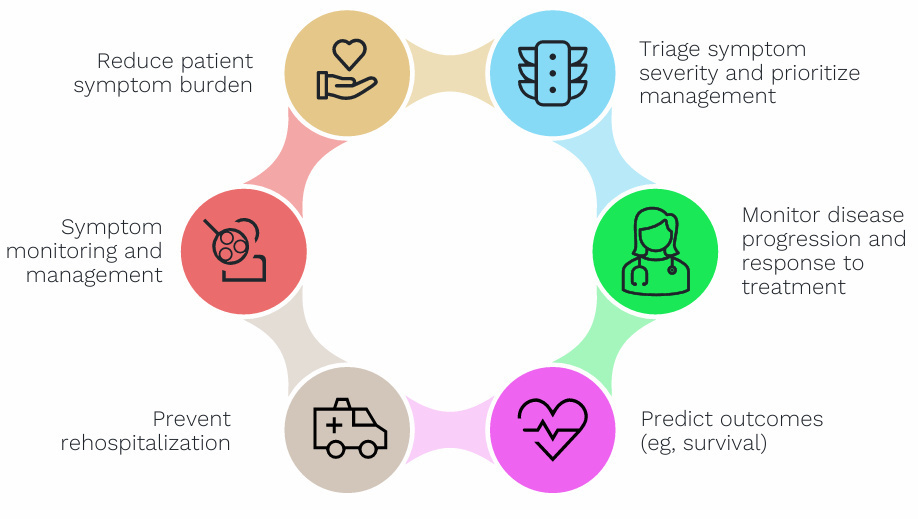 SCD临床试验中患者报告结局的重要性
SCD临床试验中患者报告结局的重要性
HSCT治疗镰状细胞病(SCD)的真实世界新数据
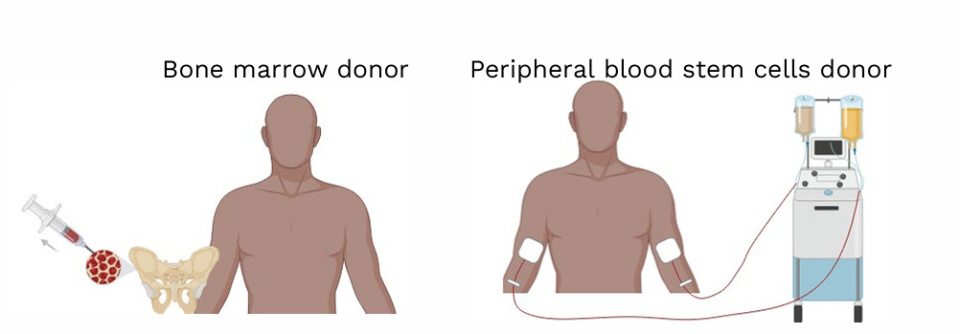
对于缺乏全相合供者的成年SCD患者,半相合HSCT是一种确切的治疗方式[12]。一项回顾性多中心队列研究探讨了与单独使用骨髓(BM)干细胞相比,单用外周血干细胞(PBSC)或联合使用 PBSC+BM 能否在不显著增加移植物抗宿主病(GvHD)风险的前提下,提高无事件生存率。
研究共纳入41例患者,其中26例接受了BM,15例接受了PBSC。结果显示,BM组出现3例死亡和1例植入失败,而PBSC组未发生此类事件。PBSC组1年无事件生存率估计为100%,而BM组为85%。与BM相比,PBSC并未增加急性或慢性GVHD的发生率,且中性粒细胞恢复速度明显更快。研究者认为,PBSC是一种创伤更小、可行性较高的半相合HSCT干细胞来源。
另一项摘要聚焦于SCD相关的眼部并发症,利用前瞻性观察研究的数据,评估HSCT是否能够阻止镰状细胞视网膜病变(SCR)和黄斑病变(SCM)的进展,并预防新的眼科并发症发生[13]。研究共纳入89例SCD患者,其中32例接受HSCT,57例为对照。所有患者均在移植前及移植后至少1年接受眼科评估。结果显示,HSCT组的视网膜病变进展率和黄斑变薄发生率显著低于对照组。玻璃体出血、视网膜脱离及激光治疗在对照组更为常见。研究者总结认为,非清髓性HSCT能够降低成年SCD患者SCR和SCM的进展速度。
HbF诱导可缓解SCD症状
胎儿γ-珠蛋白的表达及随后形成的HbF四聚体,可以在很大程度上消除镰状细胞病(SCD)相关的大多数并发症。即便是HbF水平的小幅升高,也与患者预后显著改善相关。目前已获批的HbF诱导剂包括羟基脲和基于CRISPR的基因治疗,但仍存在未被满足的临床需求,即寻找一种安全且特异的诱导剂,能够在大多数患者中达到具有转化意义的HbF水平。
一种新型小激活RNA(saRNA)已被开发,可在体内特异性提升γ-珠蛋白的表达至治疗相关水平。研究显示,候选药物MT011391在以人类健康供者BM来源的CD34细胞为基础的原代红系祖细胞模型中,能够剂量依赖性诱导γ-珠蛋白RNA和蛋白的泛细胞水平表达。在羟基脲敏感和非敏感供者细胞中均能实现γ-珠蛋白上调,HbF诱导率达62%。在非人灵长类模型中也观察到了药效活性,并通过高效的脂质体递送实现[14]。每月一次静脉给药即可刺激保护性HbF水平,目前该候选药物已进入新药临床试验申请阶段。
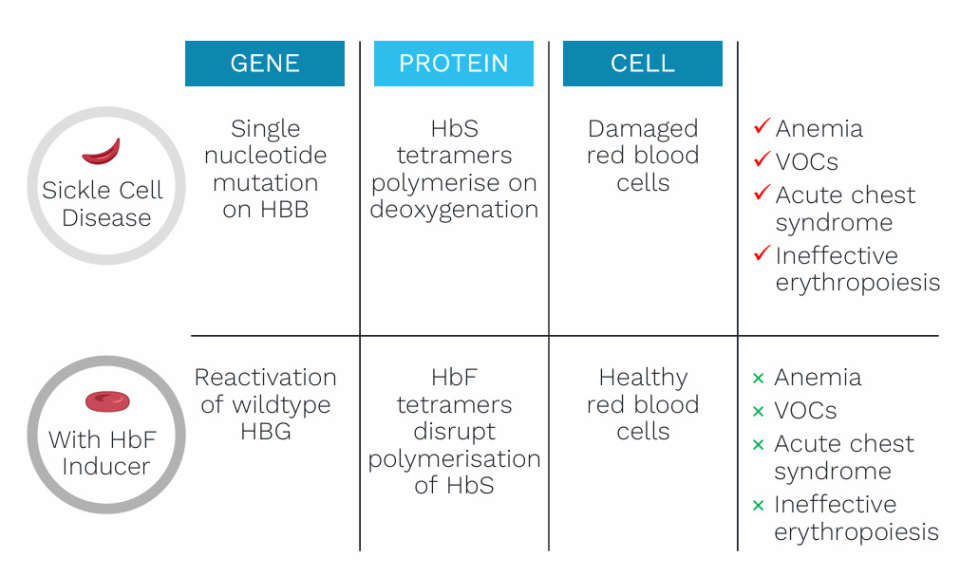 HbF诱导通过抑制HbS聚合来纠正SCD表型
HbF诱导通过抑制HbS聚合来纠正SCD表型
总 结
EHA 2025大会通过大量研究摘要和专题会议展示了SCD领域的最新进展。围绕基因治疗与羟基脲的讨论强调,虽然基因治疗为部分患者带来巨大希望,但对大多数患者而言,优化现有治疗仍然至关重要。这种优化包括根据患者依从性、代谢特点、医疗过渡以及新生儿筛查结果,调整羟基脲的用药策略。此外,推动SCD治疗格局发展还需要改进临床结局评估、提高患者参与度,并加强临床试验的招募与留存。
参考文献:
[1]Allali S. Challenges of endpoints in sickle cell disease. Oral presentation s128-1 at EHA2025.
[2]Tambor E, et al. coreSCD: Multistakeholder consensus on core outcomes for sickle cell disease clinical trials. BMC Med Res Methodol. 2021;21:219.
[3]Colombatti R. Challenges of diversity and enrolment of patients. Oral presentation s128-2 at EHA2025.
[4]Gulbis B. State of the art point-ofcare (POC) tests for neonatal screening of SCD. Oral presentation p516-1 at EHA2025.
[5]Colombatti R. Changing setting, guidelines and perspective in the transition from pediatric to adult care for Sickle Cell Disease. Oral presentation p268-3 at EHA2025.
[6]Guarino S, et al. National Alliance of Sickle Cell Centers Consensus Standards for Transition to Adult Care in Sickle Cell Disease. Blood Adv. 2025; doi.org/10.1182/bloodadvances.2025015909.
[7]de Montalembert M. Gene Therapy vs hematopoietic stem cell transplant. PRO: Gene therapy. Thematic debate p555-1 at EHA2025.
[8]Nur E. Gene Therapy vs hematopoietic stem cell transplant. PRO: Transplant. Thematic debate p555-2 at EHA2025.
[9]Pressiat C, A, et al. Impact of renal function on hydroxyurea exposure in sickle-cell disease patients. Br J Clin Pharmacol. 2021;87(5):2274-2285.
[10]Yan J-H, et al. The influence of renal function on hydroxyurea pharmacokinetics in adults with sickle cell disease. J Clin Pharmacol.2005;45(4):434-445.
[11]Jepngetich B. Community-led hydroxyurea programme. Oral presentation p210-4 at EHA2025.
[12]Zwolsman M, et al. Outcomes of peripheral blood stem cells versus bone marrow in adult sickle cell disease patients undergoing haploidentical allogeneic stem cell transplantation. Abstract s285 at EHA2025.
[13]Dovern E. The impact of allogeneic hematopoietic stem cell transplantation on sickle cell retinopathy and maculopathy: A prospective, observational study. Abstract s288 presented at EHA2025.
[14]Ryan B, et al. Small activating RNAmediated induction of HBG via liposome delivery for in vivo treatment of sickle cell disease. Abstract s287 at EHA2025.