2025年,备受瞩目的第30届欧洲血液学协会(EHA)年会在意大利米兰盛大召开。本次会议汇聚了全球范围内的顶尖专家学者,共同探讨血液学领域的基础研究与临床转化的前沿议题。剑桥大学的Daniel Hartson教授就“破译侵袭性淋巴瘤的基因组学”议题发表了精彩演讲,系统阐述了弥漫性大B细胞淋巴瘤(Diffuse Large B-cell Lymphoma, DLBCL)的基因复杂性,并分享了其团队在构建新型功能基因组学模型方面的突破性成果,强调了标准化分子谱分析对于推动未来临床研究和个体化治疗的决定性意义。
弥漫性大B细胞淋巴瘤(DLBCL)作为最常见的非霍奇金淋巴瘤类型,其治疗在过去二十年间进展相对缓慢。尽管靶向药物在临床前研究中层出不穷,但多数大型临床试验未能撼动R-CHOP方案的基石地位,新近获批的R-Pola-CHP方案也仅带来了有限的生存获益。Daniel Hartson教授在报告伊始便尖锐地指出:“我们面临的根本问题是,在未充分了解肿瘤生物学特性的情况下,盲目地使用这些‘精准’的靶向药物。生物学靶向治疗必须精准地靶向生物学本身。”
DLBCL的基因复杂性:远超单基因疾病的挑战
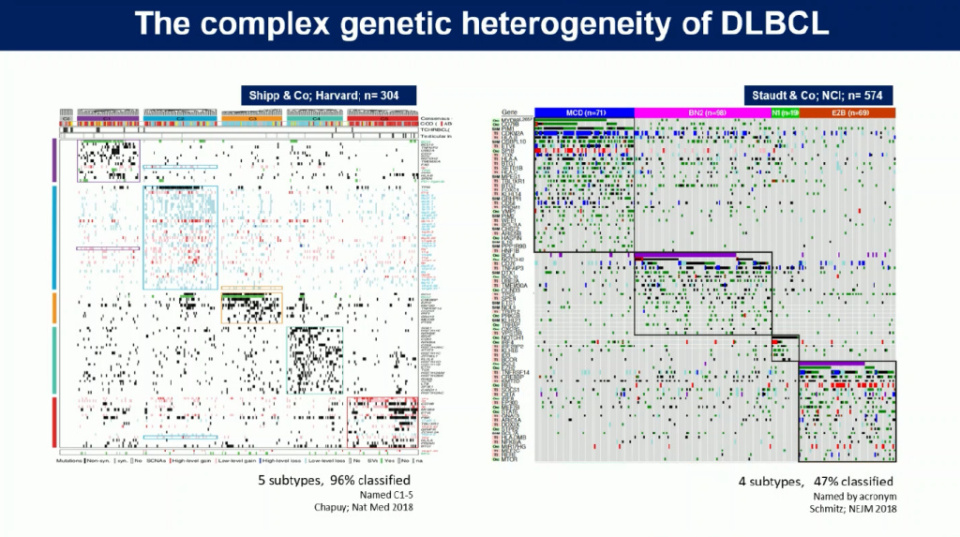
Hartson教授指出,DLBCL在基因层面并非单一疾病,而是由多种疾病构成的复杂综合体。通过回顾多项里程碑式的外显子组测序研究,他强调了DLBCL基因谱的高度复杂性与异质性。“我们讨论的不仅仅是单个基因突变,DLBCL中约有150个反复突变的基因,超过1000种反复出现的具体突变位点,并且每个患者体内通常携带5至15个驱动突变的组合。” 这种“千人千面”的基因特征意味着几乎每位患者的肿瘤都是独一无二的,这给理解突变功能及制定有效治疗策略带来了巨大挑战。
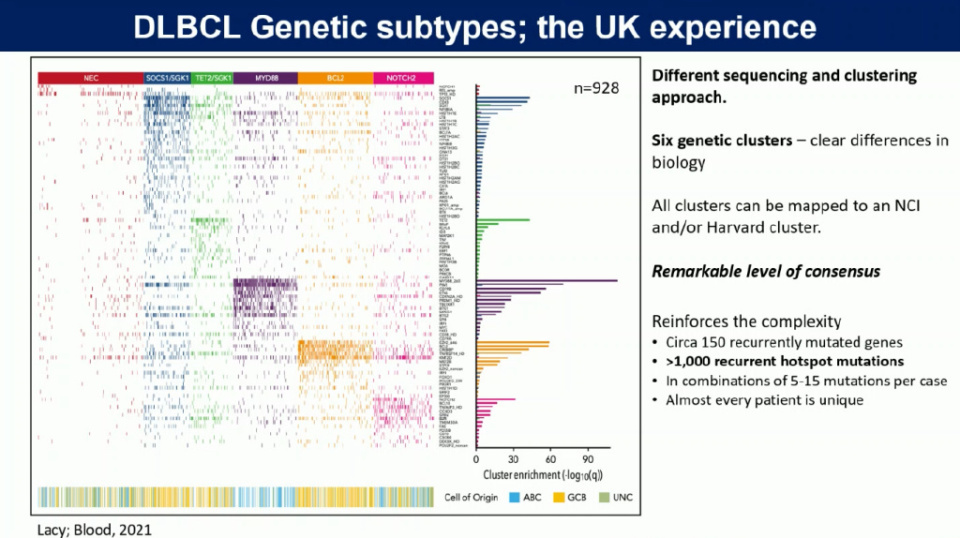
尽管不同研究团队识别出的突变基因列表不尽相同,但他们共同揭示了一个核心规律:DLBCL的基因突变并非随机发生,而是可以根据相似的突变谱将患者聚类成不同的遗传亚型。Hartson教授团队一项涉及近千名患者的大规模测序研究,也独立验证并完善了现有的基因分型体系,进一步证实了DLBCL遗传亚型概念的普适性和重要性。
突破研究瓶颈:新型人源B细胞模型解码突变功能
要阐明上千种突变组合的生物学意义,必须依赖可靠的体外模型。然而,传统淋巴瘤细胞系因长期体外培养已发生显著变异,而基因工程小鼠模型则存在成本高、周期长及物种差异等局限性。Hartson教授分享了其团队如何攻克这一难题。
他的团队成功开发了一套创新的原代人种系中心(Germinal Center, GC)B细胞体外培养与基因编辑系统。该系统的核心突破在于:
模拟微环境:通过构建表达CD40配体和IL-21的永生化滤泡树突状细胞作为“饲养层”,成功模拟了B细胞在淋巴结内的生存微环境,使其能够在体外旺盛增殖。
高效基因递送:针对原代GC-B细胞难以被常规慢病毒转导的问题,团队开发了基于长臂猿白血病病毒(Gibbon Ape Leukemia Virus)包膜的嵌合病毒载体,将基因转导效率提升至接近100%。
“这一平台的建立,使我们能够对来自健康儿童扁桃体的正常人B细胞,进行包括基因过表达、CRISPR敲除乃至单碱基精准编辑在内的复杂遗传学操作。”Hartson教授介绍道。利用该模型,团队成功在免疫缺陷小鼠体内构建了“基因定制”的人源DLBCL模型,这些模型在组织病理学上与临床肿瘤高度相似。
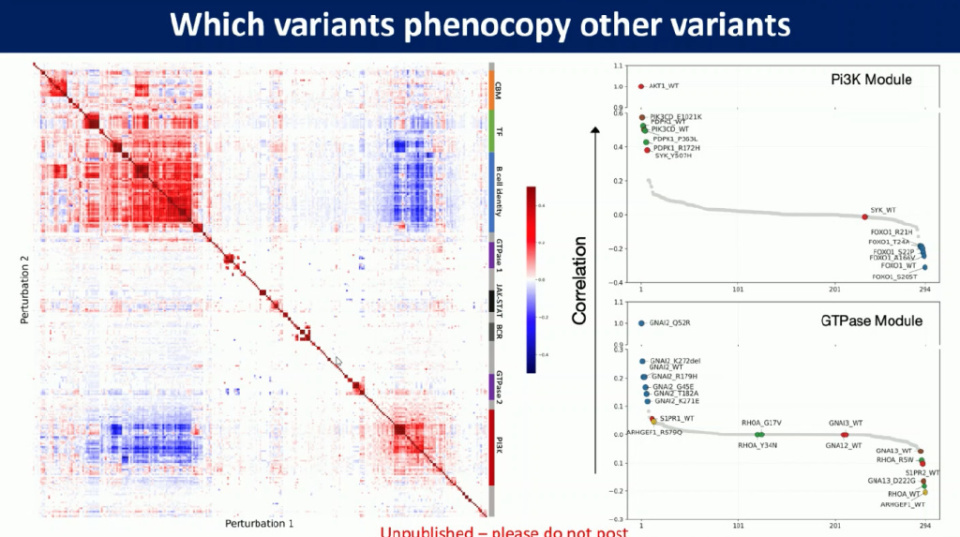
基于此平台,团队开展了一项雄心勃勃的计划:系统性解析DLBCL中每一个热点突变的功能。他们构建了一个包含1200个克隆的开放阅读框(ORF)文库,并通过竞争性适应性筛选和单细胞扰动转录组学(single cell perturbational transcriptomics)技术,成功描绘了345个关键突变对细胞适应性、基因表达网络及信号通路的影响图谱。“我们现在能够清晰地看到,特定的突变(如GNAI2、CARD11的激活突变)比其野生型能赋予B细胞更强的竞争优势,并且我们可以精确识别出它们调控的下游通路。”
从基础到临床:基因分型指导治疗的潜力与挑战
Hartson教授进一步探讨了如何将这些基础研究发现转化为临床实践。他以评估伊布替尼疗效的PHOENIX研究为例,指出尽管该研究在全人群中未达到主要终点,但回顾性亚组分析显示,伊布替尼能显著改善MCD和NOTCH1这两个特定遗传亚型患者的生存。 “这提示我们,许多被判定为‘失败’的临床试验中,可能隐藏着对特定亚型有效的信号。”
此外,其团队对维泊妥珠单抗(靶向CD79B的抗体偶联药物)耐药机制的研究发现,细胞表面唾液酸糖基化修饰是影响药物结合的关键。通过CRISPR筛选,他们识别出调控该通路的关键基因,并证实抑制唾液酸化可将细胞对Polatuzumab的敏感性提高10至50倍。 约10%的DLBCL患者在该通路中存在突变,理论上可能成为Polatuzumab的“超级响应者”。然而,Hartson教授遗憾地表示,由于现有临床试验普遍缺乏全面的分子谱数据,这些极具潜力的科学假设无法得到及时验证。
在演讲的最后,Hartson教授用圣经故事“巴别塔”巧妙地比喻了当前DLBCL研究领域的困境。“我们就像建造巴别塔的人,因为语言不通而失败。在DLBCL领域,不同的研究中心使用不同的基因测序Panel,收集不同的遗传数据,这种缺乏统一标准的局面,严重阻碍了基础科学与临床试验之间的有效对话与数据整合。”
他强调,标准化的、全面的分子谱数据是连接基础研究与临床实践的“通用货币”。他借用《圣经》的典故总结道:“如果我们作为一个整体,对DLBCL进行标准化的、全面的分子谱分析,那么我们计划做的任何事情,对我们来说都将不再是不可能的。” 这一振聋发聩的呼吁,为推动侵袭性淋巴瘤未来研究指明了方向,也引发了与会者的深刻共鸣。Hartson教授的研究不仅为理解淋巴瘤的发病机制提供了全新工具与视角,更重要的是,他为打破研究壁垒、加速精准治疗时代的到来,提出了极具建设性的战略构想。