备受瞩目的ICML大会上,来自全球的顶尖专家汇聚一堂,共同探讨淋巴瘤治疗的最新进展与未来趋势。其中,一项关于深度学习预测嵌合抗原受体T细胞(CAR-T)治疗结局的创新研究引发了广泛关注,该研究由宾夕法尼亚大学的Stephen Schuster教授报告了题为《基于深度学习的FDG-PET/CT影像分析可预测CAR-T细胞治疗12个月的疗效结局》。
CAR-T细胞治疗的挑战与预后预测的紧迫性
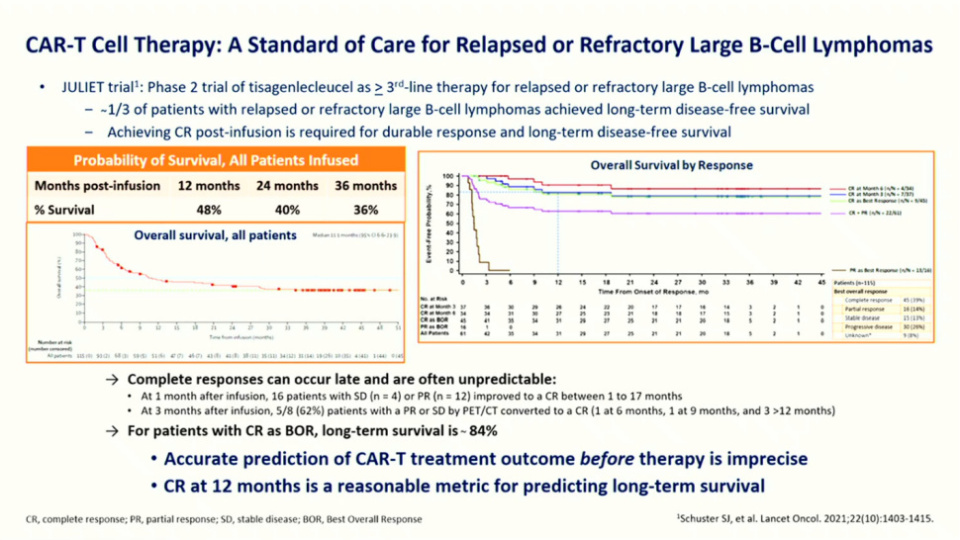
嵌合抗原受体T细胞(CAR-T)疗法已成为复发/难治性大B细胞淋巴瘤(R/R LBCL)患者的标准治疗方案之一。然而,尽管其疗效显著,但并非所有患者都能实现长期缓解。例如,针对CD19的CAR-T疗法Tisagenlecleucel的JULIET注册II期试验显示,在三线或更晚期治疗的患者中,约三分之一的患者实现了长期无病生存。研究数据表明,治疗后获得完全缓解(CR)是实现持久缓解和长期生存的关键,但这些CR的发生时间可能较晚且难以预测。对于在任何时间点达到CR并作为其最佳总体缓解的患者,长期生存率约为84%,且在约12个月时曲线趋于平台。因此,Stephen Schuster教授及其团队认为,将12个月时的完全缓解作为预测长期无病生存的合理指标。
然而,当前临床上在治疗前预测哪些患者能获得持久缓解的能力仍然有限。影像组学(Radiomics)正是一个充满潜力的领域。他强调“图像不仅仅是图片,它们是数据”,这为利用医学影像中隐藏的丰富信息提供了理论基础。
影像组学:从“图片”到“数据”的转变
基于这一理念,Schuster教授团队八年前提出了一个假设:放射影像中包含的详细定量数据,远超我们用于重建人体可识别解剖和功能图像的信息。这些额外的数据可能包含有助于临床决策的预后信息,即存在我们肉眼无法察觉但具有临床意义的特征。该研究旨在从氟脱氧葡萄糖正电子发射断层扫描/计算机断层扫描(FDG PET/CT)或诊断性CT扫描中提取这些与图像表征无关的数据,并结合机器学习方法,将其与患者的治疗结局关联起来。
研究团队选择CAR-T疗法作为切入点,并非因为其独特性,而是因为他们积累了大量经过严格筛选的CAR-T患者影像资料。他们的目标是开发一个计算机辅助决策支持系统,通过重新训练一个公开可用的神经网络——AlexNet,并利用迁移学习和增量机器学习技术来实现。最终,他们希望能够盲法分析治疗前扫描,无需任何临床信息,仅依据模型预测患者的结局,并最终进行前瞻性验证。

深度学习模型的构建与初步验证
Schuster教授详细介绍了模型的开发过程,该过程基于AlexNet神经网络进行再训练和增量学习。研究团队利用宾夕法尼亚大学治疗的CAR-T患者的既往数据,包括诊断性CT(低剂量CT)和单纯的FDG PET图像,来构建模型以预测单个病灶的反应。这一过程极为耗时,共进行了3000多次实验。由于没有3000名不同的患者,研究人员转而分析了39名CAR-T细胞研究患者的770个淋巴结病灶,以开发他们的模型。
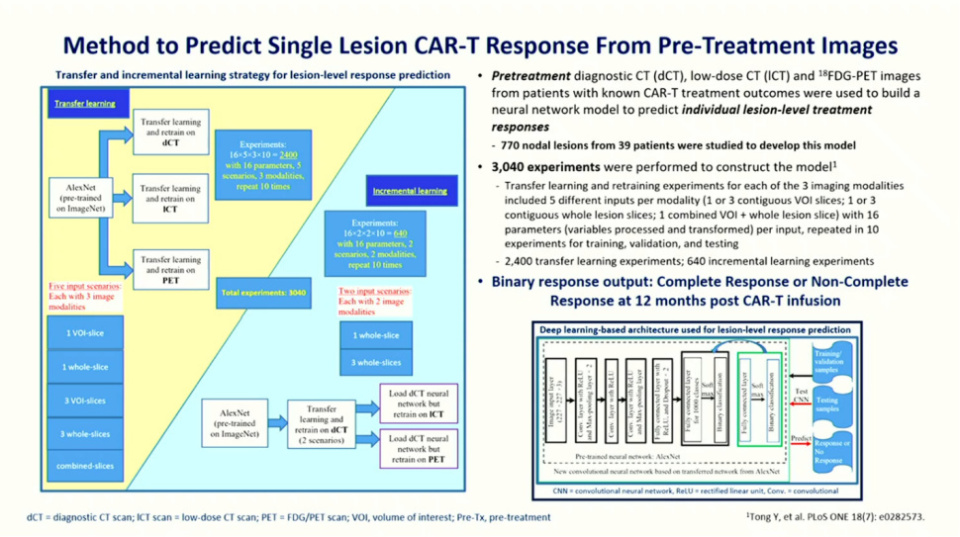
实验中尝试了多种输入方式,包括横轴上完整切片的病灶、病灶中部切片以及中部三层切片等,并不断对计算机进行再训练。模型的目标是输出一个二分类结果:CAR-T治疗后12个月是否达到完全缓解。数据显示,在预测单个病灶对CAR-T治疗的反应方面,无论使用诊断性CT、低剂量CT还是PET扫描,模型的准确率都表现出色,达到约85%至90%。ROC曲线下面积(AUC)高达90%,这充分展示了模型在病灶层面的强大预测能力。
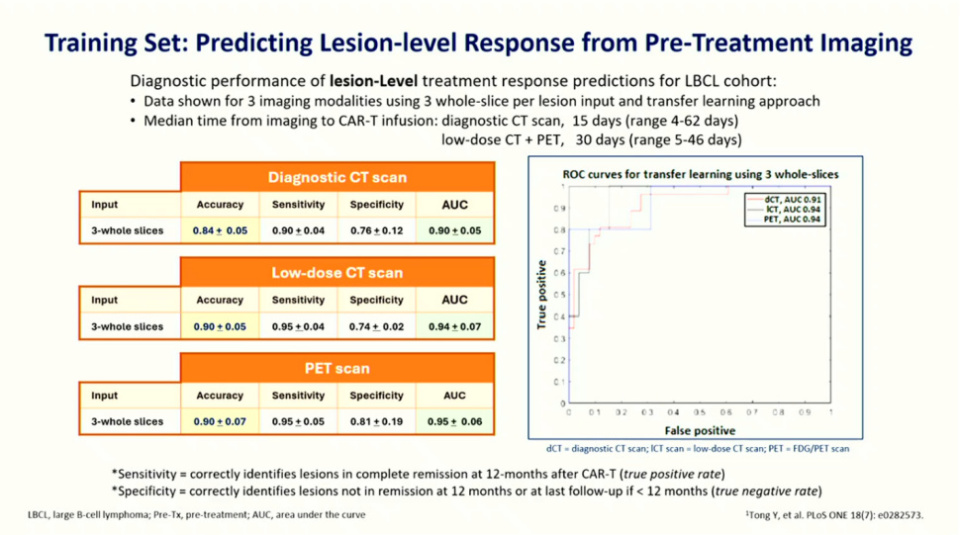
从病灶层面到患者结局的预测:基于规则推理的应用
鉴于临床实践中需要评估的是整个患者而非单个病灶,研究团队引入了“基于规则的推理”(rule-based reasoning),即“少数服从多数”的原则,将病灶层面的预测推广到患者层面的结局预测。他们尝试了不同的多数规则,例如“所有淋巴结都响应”“超过60%的病灶响应”或“至少70%的病灶响应”。通过这种方法,尽管相比于单个病灶的预测,患者层面的准确率有所下降,但仍然达到了可观的水平。例如,在诊断性CT扫描中,采用70%规则时,准确率达到了81%。这一初步结果令Schuster教授深感鼓舞,验证了该方法在临床应用中的潜力。
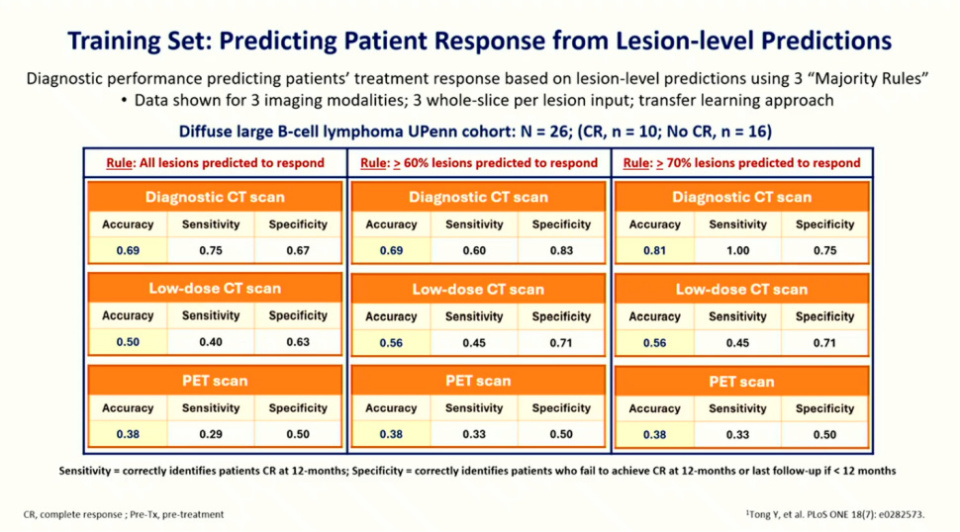
大规模外部验证:模型泛化能力的初步展现
为了进一步验证模型的泛化能力和临床实用性,研究团队获得了JULIET研究中的102份治疗前数据集。这些数据已去除所有宾夕法尼亚大学的患者信息,且研究人员对患者的结局完全盲法。经过筛选,部分病例因图像质量或缺乏离散淋巴结病灶而被排除,最终有62例患者可用于算法评估。值得注意的是,这些影像数据集来源于15种不同型号的扫描仪、3家制造商、27家医院和10个不同的国家,这有力地证明了该模型具有良好的可导出性和泛化潜力。

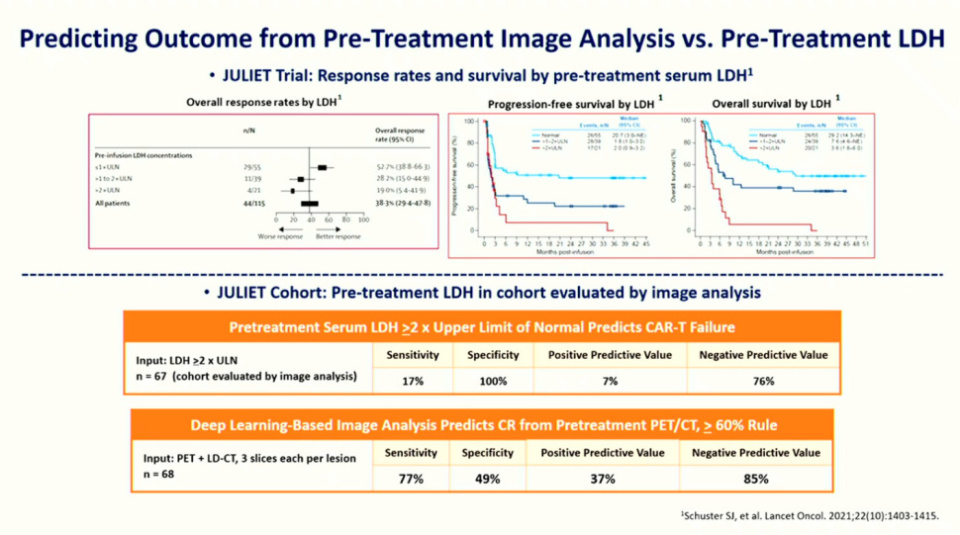
在这次外部验证中,Schuster教授团队主要关注了低剂量CT和PET图像的联合分析(每病灶各三层切片)。结果显示,模型预测CAR-T治疗后12个月达到CR的敏感性为77%,特异性为49%。由于非响应者数量多于响应者,平衡准确率为63%。阳性预测值(PPV)为37%,阴性预测值(NPV)为85%。尽管Schuster教授坦言这仍是一个“未完成的工作”,但高达85%的阴性预测值意味着模型能够以较高的置信度(85%)预测哪些患者可能不会响应,这对于临床决策具有重要的指导意义。

与传统生物标志物的对比与未来优化方向
研究团队还将深度学习模型的预测结果与目前CAR-T治疗中一个最可靠的预后因素——血清乳酸脱氢酶(LDH)水平进行了对比。JULIET试验的多变量分析显示,LDH是唯一两个统计学独立因素之一。Kaplan-Meier曲线显示,LDH升高患者的无进展生存期(PFS)或总生存期(OS)明显更差,甚至低于10%。虽然LDH在预测非响应者方面表现出100%的特异性,因为它没有假阳性,但其敏感性较差,且阳性预测值较低,即许多LDH正常的患者也未能实现缓解。
相比之下,深度学习模型表现出更高的敏感性(77%),这意味着假阴性较少,即能够识别出更多潜在的响应者。尽管特异性(49%)相对较低,导致假阳性略多,但其在早期筛选出非响应者方面的潜力仍不可忽视。Schuster教授指出,这是一项正在进行的工作,未来将继续分析诊断性CT图像并完成所有病例的评估。他相信,通过将LDH、组织学类型(如转化或非转化)、结外病变等临床信息与深度学习提取的影像组学特征相结合,将显著提高模型的预测准确性。
AI在CAR-T预后预测中的价值与展望
Stephen Schuster教授总结道,基于人工智能(AI)的治疗前影像预测CAR-T细胞治疗结局是可行的,且成本低廉,只需患者提供影像光盘即可。目前模型的单个淋巴结病灶预测平均准确率非常高,达到85%~90%,并且通过规则推理可以将其扩展到患者结局的预测。他强调了这项技术的颠覆性潜力,尽管计算机“看到了”什么,人类往往无法理解,因为神经网络可能在16个维度上进行分析,远超人类的三维甚至四维思维能力。
关于模型是否能够预测哪些淋巴结会响应而哪些不会,从而指导放射肿瘤科医生聚焦于未响应的病灶进行局部治疗的问题。Schuster教授指出未来的算法可能具有淋巴瘤特异性和治疗特异性。他坚信,人工智能应用于影像组学和机器学习将彻底改变我们预测治疗结局的能力。如果将LDH等生物标志物纳入模型,平衡准确率有望达到80%~90%,这将是非常出色的成就。
结语与未来展望
Stephen Schuster教授团队的这项研究,为CAR-T细胞治疗的精准预后预测开辟了新途径。通过深度学习对治疗前FDG PET/CT影像进行分析,不仅有望在治疗前筛选出最有可能从CAR-T治疗中获益的患者,也能识别出可能需要其他干预或更密切监测的患者。这项创新性的“无创诊断”策略,无疑将推动CAR-T细胞治疗进入一个更加精准化和个体化的新时代。随着更多临床数据的整合和模型的持续优化,未来有理由期待AI在肿瘤影像分析和临床决策支持领域带来更多突破性成果。